[vu sur le net] Maladie de Parkinson : conférence le 1er avril, salle Tournemine (Landivisiau)
Publié le 28 mars 2016 à 18:33article trouvé sur le site d’Ouest-France
Vendredi 1er, les malades, aidants, professionnels (kinés, psychologues, orthophonistes…) sont invités à une conférence animée par le docteur Amélie Leblanc, neurologue au CHRU de la Cavale-Blanche et à l’hôpital d’instruction des Armées Clermont-Tonnerre de Brest. Cette rencontre, organisée à l’initiative du Clic du Pays de Morlaix et de l’Association des Parkinsoniens du Finistère, se déroulera salle François-de-Tournemine, à 14 h.
pour lire cet article dans son intégralité, suivez ce lien…
1er avril : conférence « Vivre son Parkinson au quotidien » à Landivisiau (CLIC) organisée par le GP29
Publié le 29 février 2016 à 16:22Vendredi 1er Avril 2016, de 14:00 à 17:00
Salle Tournemine
(au dessus des Halles)
Landivisiau
Entrée Gratuite
Conférence animée par :
Docteur AMÉLIE LEBLANC, Neurologue au
CHRU Cavale Blanche de Brest et à l’ Hôpital
d’Instruction des Armées Clermont-Tonnerre
Une femme découvre que la maladie de Parkinson a une odeur
Publié le 28 octobre 2015 à 10:50C’est ce que titre Le Figaro, qui indique qu’« à l’aide de son seul nez, cette Écossaise a été capable de poser un diagnostic correct sur 12 personnes, certaines malades, d’autres pas ».
Le journal relève ainsi que « Joy Milne, 65 ans, a expliqué aux médias britanniques avoir remarqué un changement de l’odeur de son mari plusieurs années avant qu’il ne développe les symptômes de la maladie neurologique dégénérative ».
La Britannique a déclaré : « Son odeur a changé de façon subtile 5 ou 6 ans avant sa mort, c’est difficile à décrire. C’était une odeur musquée. Mais comme il travaillait comme anesthésiste et qu’il peut faire chaud au bloc, je pensais qu’il transpirait juste davantage ».
Le Figaro précise que « Joy Milne s’est rendu compte de la spécificité de cette odeur en la sentant sur d’autres malades rencontrés via la fondation Parkinson UK ».
Le quotidien note que « pour vérifier l’hypothèse, des chercheurs investis dans la fondation ont demandé à Joy de classer 12 tee-shirts qui avaient été portés toute une journée par 6 personnes malades et 6 personnes ‘saines’. À l’issue du test, Joy avait identifié à l’aveugle 5 personnes saines et 7 malades. Joli score, donc, mais pas parfait. Sauf que 8 mois plus tard, la personne saine identifiée comme malade par Joy rappelait l’équipe pour dire qu’elle avait à son tour été diagnostiquée comme parkinsonienne. »
Le Figaro fait savoir que « cette expérience a donné lieu au lancement […] d’un projet de recherche de la fondation Parkinson UK pour établir si la maladie et l’odeur sont liées. Les chercheurs s’interrogent notamment sur une possible modification du sébum causée par la maladie ».
« L’étude portera sur 200 personnes, certaines souffrant de Parkinson et d’autres pas. Leurs prélèvements seront analysés au niveau moléculaire, et « respirés » par Joy Milne et une équipe d’experts de l’odorat issue de l’industrie alimentaire », précise le journal.
Le Figaro rappelle que « baser le diagnostic médical sur l’odorat n’est pas une idée nouvelle. Il a déjà été prouvé que des chiens dressés sont capables de ‘renifler’ une tumeur de la prostate avec beaucoup de précision. De la même manière, plusieurs dispositifs, baptisés ‘nez électroniques’ sont en développement pour détecter des micro-particules volatiles émanant de cancers du poumon, de l’estomac, du côlon ou du sein, émises par le souffle ».
Le Parisien évoque également ces « nouvelles recherches sur Parkinson après la découverte qu’une femme peut ‘sentir’ la maladie ». Le journal observe que « l’odorat pourrait devenir un outil de dépistage de la maladie de Parkinson, si l’hypothèse d’une odeur symptomatique est confirmée ».
Le quotidien cite Arthur Roach, directeur de recherche de la fondation britannique, qui indique que « nous sommes dans les prémisses de la recherche, mais s’il est prouvé qu’il y a une odeur unique associée à la maladie de Parkinson, notamment aux origines de la maladie, cela pourrait avoir un impact énorme. Pas seulement pour les diagnostics précoces. Cela rendrait aussi beaucoup plus facile l’identification des malades et les tests de médicaments ».
lu dans Le Figaro et Le Parisien par Dominique Bonne
Président de l’association de Parkinsoniens du Finistère
[GP29 — vu sur le net] Maladie de Parkinson. Rompre l’isolement
Publié le 17 octobre 2015 à 13:04article trouvé sur le site du Télégramme
Proposée dans le cadre de la Semaine bleue, la conférence sur la maladie de Parkinson a réuni une quarantaine de personnes, hier après-midi, à l’Espace Ti Kastelliz. Animée par François Tosser et quelques membres de l’Association des Parkinsoniens du Finistère, complétée par des témoignages et des échanges, elle a permis de mieux cerner cette maladie neurodégénérative.
pour lire l’article dans son intégralité suivez ce lien…
GP29 — Forum « bien vieillir en pays de Morlaix » — 17 septembre 2015
Publié le 24 août 2015 à 09:43Nous vous invitons à visiter le Forum « bien vieillir en pays de Morlaix », auquel nous participons activement.
de 09:30 à 17:30
Espace Lango
Z.A. Parc Langolvas
Morlaix
Ouvert aux particuliers et aux professionnels — entrée gratuite
Pour tout savoir (plan, programme), Téléchargez le dépliant d’information en suivant ce lien
Parkinson : conférence à Châteaulin
Publié le 08 avril 2015 à 08:27L’Association de Parkinsoniens du Finistère organise lors de la journée mondiale annuelle dédiée à Parkinson, une conférence au Juvénat de Châteaulin, elle sera animée par le Professeur Zagnoli de l’hôpital d’instruction des armées de Brest. Le thème retenu : l’éducation thérapeutique, la gestion des complications dans la maladie et la recherche sur la maladie de Parkinson. Cette conférence aura lieu le 11 avril 2015 de 14h00 à 17h00.
L’Association comptait en 2014, 228 adhérents. Ce chiffre augmente régulièrement. Elle est présente dans tout le Finistère. Son fonctionnement est basé sur le bénévolat.
Ses objectifs sont les suivants : faire connaître la maladie, rompre l’isolement du malade et son entourage, améliorer sa qualité de vie, apporter un soutien constant et amical pour redonner espoir et joie de vivre.
Elle œuvre aussi pour diffuser des informations sur la maladie et recueillir des fonds pour aider la recherche.
Dans notre département nous avons quatre points-rencontre mensuels (Brest, Quimper, Quimperlé, Morlaix), quatre points hebdomadaires de gymnastique adaptée et encadrée par des kinésithérapeutes (Ploudaniel, Brest, Quimper, Plouguerneau) un point marche nordique et sophrologie sur Morlaix, un atelier chant sur Quimper. La liste de ces différents points sera mise à disposition lors de cet après- midi information. Elle est disponible aussi sur notre site internet.
Nous organisons une à deux conférences dans l’année. Lors de ces conférences programmées, nous avons en général 200 à 250 personnes présentes malades, aidants, professionnels de santé.
Nous avons un site internet : www.gp29.org qui est documenté et mis à jour quotidiennement.

Nous avions participé activement en 2009 / 2010 au livre blanc sur Parkinson en partenariat avec d’autres Associations de Parkinsoniens. Les 20 principaux points pris en compte sont :
SORTIR DE L’OMBRE
1. Demander aux pouvoirs publics une enquête pour identifier le nombre de personnes touchées et leurs caractéristiques.
2. Donner aux associations Parkinson les moyens de mieux prendre en compte la détresse des malades (visibilité, accès à des locaux, financement des mises en place de formations experts).
3. Organiser des campagnes d’information et d’image sur la réalité de la maladie et des malades avec un financement des pouvoirs publics.
SOIGNER PLUS EFFICACEMENT ET METTRE FIN AUX INÉGALITÉS
4. Assurer le droit pour tous à un diagnostic précoce et certain par un neurologue.
5. Mettre en œuvre un dispositif d’annonce en deux temps : du neurologue au patient accompagné d’un proche s’il le souhaite, puis vers les autres acteurs médicaux, paramédicaux et sociaux.
6. Faciliter la prise en charge en A. L. D. (affection longue durée) dès le diagnostic (ou après 6 mois de traitement) par le neurologue et avec tacite reconduction.
7. Structurer le système de soins Parkinson avec la création de réseaux territoriaux assurant le suivi coordonné des malades, la formation continue des professionnels, des pôles de référence régionaux pour la prise en charge de cas difficiles comme les jeunes, les opérations, la recherche.
8. Développer la prise en charge pluridisciplinaire avec des professionnels formés à la maladie de Parkinson, la possibilité de rééducations spécifiques collectives (kinésithérapie, orthophonie). Prévoir leur mode de rémunération.
9. Mettre en place un numéro vert pour les professionnels.
10. En urgence établir des recommandations HAS (Haute Autorité de Santé) sur les prescriptions médicamenteuses et leur interaction. Alerter sur les effets secondaires des médicaments.
AIDER A VIVRE AVEC LA MALADIE
11. Mettre en œuvre les dispositions de la loi Hpst (hôpital, santé, patients et territoires) sur l’éducation thérapeutique et développer des actions concrètes.- avec des expérimentations d’infirmières coordonnatrices Parkinson (voir Toulouse)
— la formation de patients experts Parkinson avec la Cnam (extension du programme Sophia du diabète).
12. Donner aux aidants une place mieux reconnue : partenariat thérapeutique avec le médecin, instauration d’un suivi médical et psychologique, formation et valorisation de son action.
13. Aider les jeunes parkinsoniens soit la moitié des personnes diagnostiquées à se maintenir dans l’emploi (formation du médecin MDPH et du travail).
14. Leur permettre d’accéder à la retraite anticipée : dans le secteur privé, rendre le texte pour les handicapés applicables à Parkinson, dans la fonction publique ouvrir droit au congé longue durée.
15. Définir et instituer un label pour les structures d’hébergement et d’accueil temporaires ainsi que les structures d’aide à domicile en prévoyant des formations des personnels. Demander aux Ars d’évaluer les besoins.
16. Expérimenter le guichet unique (dans trois Maia :Méthode d’Action pour l’Intégration des services d’aide et de soins, guichet Parkinson).
17. Créer un Gis (Groupement d’intérêt scientifique)
18. Créer un observatoire pour favoriser le recueil de données épidémiologiques grâce à un échange de données entre Cnam et institutions.
19. Mobiliser les équipes sur une étude de cohorte et postuler à son financement par le grand emprunt.
20. Mettre en œuvre la directive européenne instituant comme priorité la maladie de Parkinson au sein des maladies neurodégénératives.
Nous sommes affiliés au « CECAP » (Comité d’Entente et de Coordination des Associations de Parkinsoniens) qui regroupe 10 départements. Le but du « CECAP recherche » est de financer des jeunes chercheurs, le rôle du CECAP est d’informer le public sur la maladie de Parkinson.
Un journal : « le Parkinsonien indépendant » paraît trimestriellement. Il est alimenté par des nouvelles avancées et informations sur Parkinson et sur les différentes actions des dix départements.
Un rassemblement de Parkinsoniens, aidants, et de professionnels de ces dix départements aura lieu à Plestin Les Grèves début octobre 2015, avec une conférence du Professeur Derkinderen neurologue et chercheur au centre expert du CHU de Nantes Saint-Herblain, présentation de l’hôpital de jour de Paimpol, journée nationale des aidants, initiation au QI GONG
À l’occasion de la conférence, une documentation, « rééducation et maladie de Parkinson » sera mise à la disposition du public. Cet ouvrage, très bien conçu, il reflète les besoins journaliers d’un Parkinsonien. « Être parkinsonien c’est un métier à part entière », il faut constamment travailler sur ses acquis afin de préserver sa mobilité, sa vie, bien connaître sa maladie pour mieux la gérer !
L’entrée est libre et gratuite.
Dominique BONNE
Président Association de Parkinsoniens du Finistère
Contacts au : 0960365168 , 0298725163 , 0298713671 , 0298206185
Conférence du GP29 le 12 octobre
Publié le 08 octobre 2013 à 13:59
la maladie de Parkinson
« ce que l’intestin nous apprend »
par le Professeur DERKINDEREN
du CHU de NANTES
et Monsieur Thomas Clairembault
chercheur du CHU de NANTES
SAMEDI 12 OCTOBRE 2013
à 14h (ouverture des portes à 13h30)
au JUVÉNAT NOTRE DAME
Penn Feunteun –CHÂTEAULIN
Information – documentation
entrée libre
présidence : Mr Dominique Bonne
3 place Glenmor
29260 Lesneven
Tél. : 09 60 36 57 68
dominique.bonne@gmail.com
vice-présidence : Mme Claire Ducros
1 rue fontaine St Pierre
29300 Mellac
Tél : 02 98 71 36 71
acducros@orange.fr
Siège Social et secrétariat : Mme E. Six
Larvor Huella – 29460 Logonna Daoulas
Tel/fax : 02 98 20 61 85
gp29@altern.org
Les « lundis de la santé » de Brest : Parkinson
Publié le 14 mai 2013 à 07:44La conférence des docteurs François Rouhart et Irina Viakhireva du CHRU de Brest avec la participation du GP29 que nous avions annoncée ici
a maintenant été mise en ligne. Suivez ce lien pour la suivre.
Conférence Parkinson à Brest le 15 avril
Publié le 10 avril 2013 à 07:19Lundi 15 avril dans le cadre de la Journée Mondiale de la Maladie de PArkinson (13 avril), le LUNDI DE LA SANTÉ DE LA VILLE DE BREST sera consacré à la maladie de Parkinson.
Interviendront les docteurs François Rouhart et Irina Viakhireva du CHRU de Brest
L’Association de Parkinsoniens du Finistère sera présentée par son président Mr Dominique Bonne
La conférence a lieu de 18h30 à 20 h
à la Faculté de Droit
amphi 500 et 600
12 rue de Kergoat
à Brest
(ligne de bus n° 5 – arrêt Aumale) parking et facilité pour personne à mobilité réduite.
Retrouvez la conférence sur www.forumsantebrest.net
Orthophonie et maladie de Parkinson
Publié le 14 novembre 2012 à 14:53Ceci est le texte de la conférence organisée par le GP29
La prise en charge orthophonique des patients parkinsoniens concerne quatre domaines : les troubles de la parole (dysarthrie), de la déglutition (dysphagie), de l’écriture (micrographie) et les troubles cognitifs (attention, fonctions exécutives : organisation, planification).
Pour lire le texte dans son intégralité, suivez ce lien (format .pdf)…
L’orthophonie — la kinésithérapie : Conférence du GP 29 le 20 octobre 2012
Publié le 10 octobre 2012 à 19:41L’orthophonie — la kinésithérapie. Pour connaitre tous les détails, cliquez sur l’affiche de la conférence du 20 octobre 2012
URGENT : Conférence par le Dr COUSTANS
Publié le 24 avril 2012 à 16:12La maladie de Parkinson en 2012, ses traitements, le point sur la recherche
Une conférence du docteur COUSTANS, neurologue à l’hôpital de Quimper.
Date : samedi 28 avril 2012 à 14 heures
Lieu : Juvénat Notre-Dame, Penn Feunteun, Châteaulin
Entrée libre, venez nombreux !
Conférence organisée par le GP29 le 13 mars 2010
Publié le 02 mars 2010 à 22:32L’Association de Parkinsoniens du Finistère (GP29) organise le samedi 13 mars 2010 une conférence pour faire le point sur les actualités thérapeutiques / recherche, présentée par le professeur Derkinderen du CHU de Nantes.
La conférence aura lieu au Juvénat Notre-Dame, Penn Feunteun, à Châteaulin, début à 14 heures (ouverture des portes à 13:30 heures), entrée libre.
Le GP29 : Adresse présidence : Mme Claire Ducros — Moguel Bras — 29310 Querrien
Tél : 02 98 71 36 71 – e‑mail : acducros@aol.com
Siège Social et secrétariat :Mme E. Six — Larvor Huella — 29460 Logonna Daoulas
tél:/fax 02 98 20 61 85
Conférence du CLIC : « la MALADIE DE PARKINSON »
Publié le 17 juin 2009 à 05:55Le 7 avril 2009 à 20H30 à la salle Yves Bleunven sur la commune du FOLGOËT a eu lieu une réunion d’information sur la Maladie de Parkinson à l’initiative de Mme CONRAD du CLIC de LESNEVEN qui regroupe la communauté des communes (15 communes)
Participaient à cette soirée :
- Le Professeur Fabien ZAGNOLI Neurologue à l’hôpital des armées de Brest, Formateur à la faculté de médecine, Formateur des médecins généralistes
- Odile et Dominique BONNE représentaient le GP29
- Le docteur Broc’h, médecin généraliste de Lesneven
- Le docteur Conrad, médecin gériatre coordinateur à l’hôpital local de Lesneven
- Infirmières, aides-soignants, un médecin de l’hôpital des armées
Le Professeur Zagnoli a présenté la Maladie de Parkinson à l’aide d’un diaporama.
Ses explications ont démontré que la maladie de Parkinson est très complexe à diagnostiquer, qu’il n’y a pas une, mais des maladies de Parkinson.
Le professeur Zagnoli a mis en avant la difficulté de la posologie des médicaments et annoncé quelques avancées, notamment la sortie prochaine de la rasagiline sous le nom d’Azilect. Ce médicament sera présenté sous forme de cachets et devrait être normalement remboursé à partir de septembre. Il y a discussions entre l’agence du médicament et la CPAM.
Ensuite nous avons présenté notre association à l’aide du diaporama GP29, puis Odile a donné son témoignage.
L’émotion était grande dans l’assemblée.
Le Neurologue a repris la parole par une série de questions/réponses avec le public.
Après 2 heures 1/2 de réunion, les personnes étaient toujours à l’écoute !! Comme quoi, le besoin de savoir, était plus fort.
Mme Conrad, vu l’heure tardive, a interrompu le dialogue en remerciant les personnes présentes d’avoir participé si nombreux à cette conférence. (150 personnes)
Odile & Dominique BONNE
L’organisation du traitement dans la Maladie de Parkinson par le Docteur LALLEMENT, neurologue à l’hôpital de St Brieuc
Publié le 16 juin 2009 à 07:45Les trois phases de la Maladie de Parkinson fluctuante
Phase de la lune de miel : le Parkinsonien n’a plus que 30% de neurones dopaminergiques. Il prend des agonistes dopaminergiques (Trivastal,Célance,Sifrol,Réquip) ou de la dopamine, 3 fois par jour. Les neurones présents vont la capter, la stocker et la redistribuer quand nécessaire. Il y a régulation.
Phase des fluctuations : fluctuation entre les symptômes corrigés, corrigés avec dyskinésies, pas assez corrigés. Quand vous avalez un médicament, son absorption par les intestins induit une importante augmentation de son taux dans le sang. Il arrive au cerveau en 30 minutes. Puis il sera détruit par des enzymes et 2 à 3 heures plus tard, son taux dans le sang va redescendre. Quand on est au pic de l’absorption, 1 à 1h30 après la prise, les symptômes ont disparu, mais des mouvements incontrôlés apparaissent. Il n’y a plus régulation mais fluctuation .
Phase de déclin : (30% des cas) elle arrive quand, en plus des neurones de la substance noire, d’autres sont touchés et vont dégénérer. Apparaissent d’autres symptômes insensibles à la dopamine : freezing / instabilité posturale / chutes / festination / dysarthrie / troubles cognitifs / hallucinations.
Amélioration de la prise médicamenteuse à la phase des fluctuations : la modélisation
A chaque prise de médicament, on note son dosage et l’horaire dans un tableau. Une courbe de couleur se trace alors sur un graphique. A la fin de la journée, une courbe noire (synthèse des courbes de couleurs) met en évidence les moments de sur ou sous-dosage. On modulera les doses selon ses besoins. Voici un exemple de 2 courbes prises parmi les 12 que le Dr Lallement a commentées : (travail avec le logiciel de Pierre Le May et son équipe)
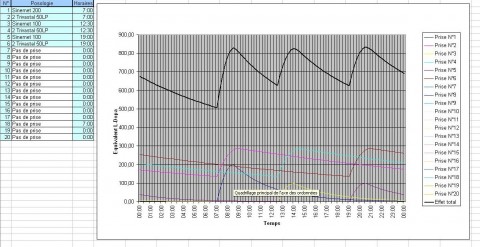
cliquez pour voir l’image en grand
Ce patient avait des symptômes vers 11 – 12 h et de nouveau en fin d’après-midi (graphique 1).On a diminué le Trivastal et augmenté le Sinémet en fractionnant le nombre de prises (6 au lieu de 3). On obtient un taux beaucoup plus régulier. L’amplitude de la fluctuation diminue (graphique 2).
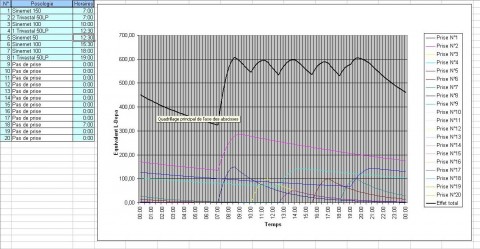
cliquez pour voir l’image en grand
L’estomac du Parkinsonien : Pourquoi y a‑t-il souvent un blocage dans la 1ère moitié de l’après-midi ?
L’estomac a du mal à se contracter pour chasser les aliments vers les intestins. Un médicament pris à 15h sera ralenti dans l’estomac encore plein et ne sera pas absorbé au moment prévu par les intestins. Il n’arrivera au cerveau que beaucoup plus tard. D’où blocage ! Un effet de cumul va se faire avec la prise suivante et il y aura un pic avec mouvements dyskinésiques. Comment pallier à cela ? en ne passant plus par l’estomac.
On peut faire des injections d’Apomorphine, au stylo, qui vont agir en moins de 10 minutes pour une durée d’action de 1 à 1h30. Il y a la pompe à Apomorphine qui régule et la pompe à Duodopa .
Présentation des différentes techniques d’amélioration des patients
La chirurgie : le patient doit passer des tests pour savoir s’il est opérable. La chirurgie nécessite 3 semaines d’hospitalisation : une journée pour l’implantation des électrodes, les autres pour les réglages, la surveillance …
le risque majeur étant celui d’une infection (1%). C’est au patient de décider.
La pompe à Apomorphine : l’Apomorphine va agir à peu près comme la Dopamine. Elle est injectée sous la peau, toute la journée. Elle améliore de 50% les performances motrice mais aussi intellectuelles et le moral des patients.
La pompe à Duodopa : (technique en cours d’évaluation) la Dopamine est amenée directement dans l’intestin où elle est délivrée en continu. Les patients sont améliorés sur le plan des fluctuations motrices, des dyskinésies ou de la dystonie.
Questions / Réponses
Les médicaments corrigent les symptômes mais n’influencent pas le cours évolutif de la MP. On retarde le plus possible la prise de Dopamine parce qu’elle accélère l’arrivée du stade des fluctuations.
Modopar et Apokinon ? le Modopar est en comprimés, l’Apokinon en injection (stylo ou pompe). Mêmes effets mais pas les mêmes délais ni durée d’action. L’injection va soulager beaucoup plus vite le symptôme de la griffe du lever ou le blocage d’après repas.
Sinémet 100 et un LP ? Le Sinémet 100 agit en 30 mn pour une action de 2h30 à 3h00. Le LP agit en 1h pour une action plus longue. Réquip est dans la modélisation, pas l’Apokinon qui a un flux continu.
Dosages : les patients qui prennent le plus de Dopa en ont 2 grammes par jour. Il faut moduler les prises en fonction de chacun. Il vaut mieux garder les mêmes intervalles quand on change d’horaire ( 3h en moyenne ).
Protéines et Dopa : supprimer les protéines à midi peut éviter le blocage. Mais si le blocage est dû à un estomac trop lent ou aux fluctuations quotidiennes des besoins en Dopa ça ne sera pas efficace non plus.
La nicotine : en association avec la Dopa améliore les Pk fluctuants à condition d’en prendre une très grosse dose. (stade expérimental)
L’Exélon peut améliorer la mémoire dans la MP.
Modélisation et analyses de sang ? le taux de Dopa dans le sang est très variable. Il vaut mieux confronter la modélisation à vos symptômes. Mettez vos journées en cases de demi-heure et notez votre état par case.
Les tremblements : symptôme excessivement sensible aux émotions. Augmenter le traitement est inutile.
Le Rivotril peut diminuer l’émotivité mais il est nocif pour la mémoire. Si les tremblements sont intenses et gênent la vie courante, penser à la chirurgie.
Syndrôme extra-pyramidal : terme générique qui regroupe tous les mouvements anormaux incontrôlables.
Les dyskinésies : celle de milieu de dose, au moment du pic, fait bouger le haut du corps. Celle de fin ou début de dose touche plutôt les jambes et sont douloureuses. Aucun remède efficace pour améliorer cela.
Les troubles de l’humeur : l’humeur suit les fluctuations de la motricité (émotivité, anxiété, dépression).
La douleur : induite par une carence en Dopa (tensions, pressions, crispations) elle est corrigée par la Dopa.
Le sommeil : les Parkinsoniens sont très agités pendant leurs rêves.
Salivation : le geste automatique de la déglutition étant plus rare, la salive s’accumule dans la bouche et finit par couler, surtout en phase de sous-dosage. L’orthophoniste apprend à avaler plus régulièrement.
Si vous avez la bouche sèche, la nuit, c’est que vous dormez la bouche ouverte.
Les médicaments : provoquent parfois des nausées, voire des vomissements, surtout en début de traitement
(> Motilium). Reflux gastro-oesophagien possible (brûlures), mais pas d’ulcère à l’estomac.
Autres symptômes subjectifs : la baisse de la Dopa, la nuit, induit diverses sensations : brûlures, impression d’eau qui court sur les jambes … Pour y remédier, prendre un LP le soir et un 2ème dans la nuit.
Maladie de Parkinson ou pas Maladie de Parkinson ?
Plusieurs maladies commencent comme une MP, mais elles répondent mal au traitement et d’autres symptômes apparaissent.
Conclusion
Nous sommes 2 neurologues à pratiquer la modélisation. Nous devons démontrer son efficacité aux autres neurologues qui s’interrogent sur le temps gagné ou perdu en consultation et sur le bénéfice qu’en tireront leurs patients .
Pour moi, la modélisation a une vertu éducative importante : quand je construis les courbes avec un patient, en consultation, il comprend mieux, ainsi que son conjoint, ce qui se passe.
Synthèse de la conférence donnée à Châteaulin, le 18 avril 2009, par le Docteur LALLEMENT, neurologue à l’hôpital de St Brieuc, dans le cadre de la journée mondiale de la maladie de Parkinson .
Synthèse faite par Joëlle Belot, du GP29 (Association de Parkinsoniens du Finistère)
Les deux graphiques avec les courbes, dans « La modélisation du traitement », proviennent du Diaporama fait par le Dr Lallement ( CH Y Le Foll).
Conférence : Samedi 18 avril 2009
Publié le 15 avril 2009 à 14:10Conférence organisée par le GP29, dans le cadre de la 13ème journée mondiale Maladie de Parkinson
La Maladie de Parkinson : l’organisation du traitement
par Mr le Dr Lallement, neurologue, hôpital de de St Brieuc
Samedi 18 avril 2009
au Juvénat Notre Dame
Penn Feunten
Châteaulin
Vous êtes tous les bienvenus, entrée libre
Parkinson : stimuler le cerveau réduit les symptômes
Publié le 28 mars 2009 à 09:38Paru dans LE PARKINSONIEN INDÉPENDANT N°36 – mars 2009
7 janv. 2009
WASHINGTON (AFP) — Des stimulations électriques en profondeur dans le cerveau réduisent les symptômes des personnes atteintes de la maladie de Parkinson mais cette procédure accroît les risques d’effets secondaires potentiellement graves, selon une étude clinique publiée mardi.
Les patients souffrant de Parkinson à un stade avancé à qui on a implanté chirurgicalement des électrodes en profondeur dans le cerveau ont connu, après six mois, une amélioration dans la coordination de leurs mouvements et la qualité de leur vie nettement plus grande que ceux ayant bénéficié d’autres thérapies, expliquent les auteurs de cette recherche parue dans le Journal of the American Medical Association (JAMA) daté du 7 janvier.
Ainsi, 71% des malades de l’étude dont le cerveau a été stimulé par des électrodes ont connu après six mois une amélioration clinique très nette de leurs fonctions motrices avec moins de tremblements et de mouvements incontrôlés contre seulement 32% dans le groupe témoin traité avec des thérapies conventionnelles.
« Toutefois, de récentes informations mettant en lumière des effets secondaires inattendus de la stimulation cérébrale en profondeur indiquent que ce traitement qui améliore les fonctions motrices peut aussi avoir des conséquences indésirables », relève la Dr Frances Weaver, du Hines VA Hospital à Hines dans l’Illinois (nord), principal auteur de cette étude.
Le risque de subir des effets secondaires tels que des infections, des troubles du système nerveux ou des troubles cardiaques ou psychiatriques était 3,8 fois plus élevé dans le groupe ayant des électrodes cérébrales que chez les patients traités avec d’autres thérapies.
C’est ainsi que 45 sujets avec des électrodes implantées dans le cerveau, (soit 40% du total) ont subi 82 effets secondaires graves. Dans le groupe témoin, 15 sujets (11%) ont subi 19 effets secondaires de même gravité.
La prudence devrait être observée pour éviter d’exagérer ou de minimiser les risques de la stimulation du cerveau en profondeur avec des électrodes implantées chez les malades atteints de la maladie de Parkinson, estiment les auteurs de l’étude.
Les médecins doivent continuer à évaluer les risques potentiels à court et long terme de cette procédure par rapport aux effets bénéfiques pour chaque malade, concluent-ils.
Au total, 255 patients souffrant de la maladie de Parkinson à un stade avancé ont participé à cette étude clinique, dont 25% avaient plus de 70 ans.
Les électrodes ont été implantées dans différentes zones du cerveau, variables selon les patients.
Dans un éditorial également publié dans le JAMA, le Dr Günther Deuschl, de l’Universitätsklinikum Schleswig-Holstein à Kiel en Allemagne, juge que « les résultats de cette importante étude ont confirmé de façon convaincante l’efficacité après six mois de la stimulation cérébrale profonde pour les cas de Parkinson avancé dans le plus grand groupe de patients ayant à ce jour participé à un essai clinique ».
Il note toutefois que « cette étude combinée à des recherches antérieures sur cette thérapie, montre que de tels progrès dans le traitement ne peuvent se faire sans un prix en termes d’effets secondaires ».
On estime qu’au moins 500.000 personnes sont atteintes de Parkinson aux Etats-Unis et que 50.000 nouveaux cas sont diagnostiqués chaque année, selon les statistiques des Instituts nationaux américains de la santé (NIH).
Ces chiffres devraient augmenter avec l’accroissement de l’âge moyen de la population.
Les hommes paraissent être légèrement plus touchés que les femmes.
L’âge moyen d’apparition de la maladie, dont les causes restent obscures, est d’environ 60 ans.
Texte trouvé sur Internet Google
Transmis par Henri MINARET et lu par Jean GRAVELEAU graveleau.jean2@orange.fr
Lutter contre les périodes sombres
Publié le 09 janvier 2009 à 06:06Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
Par Johannes KORNACHER, Lu dans le « PARKINSON Suisse » N°88
Chez les Parkinsoniens, le risque de dépression est élevé. Elle a des origines chimiques et psychiques. S’il est aidé par le malade et son entourage, le médecin a les moyens de l’endiguer.
Une fois de plus, Heinz F. a l’impression de tout faire de travers. Aujourd’hui, au volant de sa voiture automatique, il est entré en marche avant dans la porte de son garage, persuadé que la marche arrière était encore enclenchée après un moment d’inattention. « C’est tout moi. Depuis que je souffre du Parkinson, la guigne me colle aux basques », pense-t-il. Heinz F. a le sentiment d’être responsable de tous ses malheurs. Il considère sa maladie comme une punition.
Tout le monde le contredit. Toutefois Heinz F. ne souffre pas seulement du Parkinson. Il est également dépressif. On ne peut rien lui dire ; actuellement, il vit dans ce que l’on appelle une spirale de pensées négatives. Le principe est le suivant : le Parkinsonien pense par exemple : « Je ne peux plus rien faire correctement », puis : « Je préfère ne pas essayer » et enfin conclut en constatant son échec : « Rien ne va plus ». Ces derniers mois, Heinz F. s’est empêtré de plus en plus dans une spirale de pensées négatives. Chez le médecin, il se ressaisit, mais la remarque suivante lui échappe cependant : « Je fais tout de travers ».
Souvent, comme c’est le cas pour Heinz F., les dépressions accompagnant la maladie de parkinson sont d’origine psychoréactive. Il s’agit de réaction à la maladie. Par exemple, alors que les handicaps physiques altèrent la qualité de vie : « on veut continuer à tout faire comme avant », indique Joachim Kohler, ancien neurologue. « En réalité, on n’accepte pas la maladie ». La dépression remplace la colère, la rage ou la tristesse. Souvent on minimise le Parkinson dès la phase de démarrage. On met en doute la gravité de la nouvelle situation et on refuse toute aide. Les spécialistes rapportent qu’au cours de cette phase, cinq pour cent tout au plus des Parkinsoniens acceptent une aide psychologique. Cependant, ils doivent assimiler un point capital : la perte de leur ancien mode de vie.
Près de la moitié des Parkinsoniens développent une dépression. Il ne s’agit d’une réaction émotionnelle à la maladie que pour une partie d’entre eux. Souvent, les symptômes dépressifs accompagnant le Parkinson se manifestent par un déséquilibre de différents messagers chimiques et par la dégénérescence des liaisons nerveuses dans le cerveau. Les dépressions préexistent fréquemment à l’apparition des premiers symptômes visibles du Parkinson. Les médecins le savent depuis longtemps.
Cependant, ces derniers temps, on prête davantage attention aux dépressions. « Auparavant, les problèmes moteurs figuraient au premier plan », déclare le neurologue Stephan Hägele, médecin à l’hôpital cantonal de Saint-Gall. L’objectif thérapeutique principal consistait à éviter les fluctuations des performances motrices et les dyskinésies. « Aujourd’hui, nous savons que les symptômes non moteurs tels que la dépression jouent un rôle encore plus important pour la qualité de la vie ». Entre-temps, les dépressions accompagnant la maladie de Parkinson ont fait l’objet de recherches et l’on dispose désormais de davantage de conclusions certaines, qui sont intégrées au traitement. Le thème de la dépression était-il négligé ? « Souvent, on ne l’a pas discernée car de nombreux symptômes visibles du Parkinson sont identiques à ceux de la dépression, comme par exemple l’expression du visage et le ralentissement », explique le docteur Hägele. Par ailleurs, les patients informent rarement leur médecin de leur état émotionnel. Si celui-ci ne pose pas de questions ciblées, la dépression peut passer inaperçue.
Le dialogue avec le médecin est décisif pour le diagnostic et le traitement. Il en va de même pour le partenaire et pour les proches. Ils peuvent faire part au médecin de leurs observations et de leurs expériences, notamment d’un récent changement de l’expression du visage ou de certaines déclarations du patient, ou lui indiquer au cours de quelle phase les états dépressifs se manifestent, par exemple en phase off. « La contribution des proches peut s’avérer précieuse lors de l’anamnèse », déclare le docteur Hägele. Cependant, le patient peut également s’observer et donner des indications à son médecin. Ce dernier doit alors l’interroger : « Ressentez-vous une sensation de vide ? Vous est-il impossible de vous réjouir véritablement ? Avez-vous déjà vécu des périodes dépressives ? ».
Les dépressions des Parkinsoniens représentent un grand facteur de stress pour leurs partenaires également. Ils doivent trouver le juste milieu, encourager et inciter leur partenaire à s’activer sans toutefois le soumettre à un effort excessif. Parallèlement, ils ne doivent pas se mettre complètement en retrait, mais affirmer leurs besoins et leurs sentiments. Sous la pression, ils peuvent également finir par entrer en dépression. S’entretenir avec des personnes de confiance et des spécialistes peut aider à mieux s’en tirer.
L’aide du partenaire est d’une importance capitale, en particulier pour la stratégie non médicale du traitement ou de la prévention de la dépression. L’activité, la physiothérapie, la distraction, les contacts sociaux, les jeux, la culture : en cas de dépression, tout cela n’a plus grande efficacité. La motivation du partenaire peut activer beaucoup de choses. Le neurologue Stephan Hägele le sait, « Le rafraîchissement mental fait également partie du traitement ». « Une personne qui pratique régulièrement un sport, par exemple, se sent assurément mieux ». Dans le sport, le patient contrôle beaucoup de choses et peut faire ce qui lui plaît. Le bien-être psychique s’en trouve favorisé, car l’autonomie, limitée par la maladie, est renforcée. Malgré le petit nombre d’études à ce sujet, on présume que la physiothérapie aide à lutter contre les dépressions et peut contribuer à briser le cercle vicieux.
Naturellement, le traitement de la dépression peut être médicamenteux. « Il s’agit avant tout d’optimiser l’ajustement dopaminergique », retient M. Hägele. Pour ce faire, on peut avoir recours aux antidépresseurs. Un Parkinsonien dépressif doit cependant faire preuve de patience et se préparer à l’apparition d’éventuels effets secondaires avant l’action antidépressive. « C’est pénible », déclare M. Hägele. L’effet dure au moins trois semaines, parfois plus longtemps. Il recommande vivement de ne pas interrompre trop tôt, mais d’adapter la dose progressivement.
Les dépressions constituent un symptôme typique du Parkinson, déclare M. Hägele : « Nous n’en savons pas encore suffisamment », concède – t‑il. « Cependant nos progrès sont remarquables depuis que nous accordons une plus grande importance à la dépression en cas de Parkinson, qui fait l’objet de davantage de recherches ». Lorsque le patient collabore et parle de ses problèmes avec son médecin, les chances de vaincre la dépression sont grandes. Heinz F. a appris à vivre avec sa maladie au cours d’une psychothérapie par entretien de plusieurs semaines. Depuis il va beaucoup mieux. Malgré ses handicaps, il prend de nouveau plaisir à vivre : « Je suis heureux que la période sombre soit passée ».
Lu par Jean GRAVELEAU
Éditorial
Publié le 08 janvier 2009 à 07:12Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
Pour le dernier numéro de l’année, plusieurs lueurs d’espoir. Et puisque c’est la période traditionnelle des cadeaux, voici le nôtre.
La plus grande nouvelle, vous la trouverez en page 11 : des chercheurs ont pu mettre en évidence la présence, en nombre important, de sites – j’allais dire de « nids » – de cellules souches dans le cerveau et qui permettent le développement de « pièces de rechange », de neurones, venant remplacer ceux qui ont disparu ! Nous avons là une piste essentielle pour de futurs traitements de la maladie et non plus seulement de ses symptômes.
Hasard ou évidence, deux articles viennent vous présenter à peu près les mêmes réflexions sur la dépression inhérente à la plupart des maladies de Parkinson. Ils insistent sur les approches psychologiques aussi importantes – sinon plus – que le traitement des symptômes physiques. « Accepter sa maladie », s’en « rendre maître » et ne plus en « être esclave », relève d’une nécessité vitale pour l’avenir du patient et de son entourage.
Je suis ravi de voir cette approche psychologique de plus en plus retenue par nos partenaires : le docteur Lallement ne dit pas autre chose dans son exposé repris dans cette revue. Elle me permet aujourd’hui d’affirmer qu’il est possible de non seulement « survivre » à cette maladie mais aussi de la faire régresser : notre cerveau a des ressources insoupçonnées qu’il nous faut apprendre à utiliser. Je me permets de l’affirmer avec force m’appuyant sur ma propre expérience. Ceux qui me connaissent ont pu le constater et pour en apporter une preuve supplémentaire, je précise que j’ai commencé à réduire mon traitement suivi depuis déjà presque 15 ans, ceci sans séquelle apparente bien au contraire !
Vous me pardonnerez, je l’espère, cette allusion à mon vécu personnel. Je ne comprends pas tout ce qui m’arrive mais je voudrais vous dire à quel point j’ai le sentiment d’une régression de la maladie et je voulais vous le faire partager. La lecture de l’article sur les cellules souches dans le cerveau m’a rassuré sur mon état mental : je ne rêve pas, je ne fantasme pas. La guérison ou plutôt la rémission est possible : il suffit d’en trouver la clé. Sûrement que mon engagement dans cette lutte de tous les jours et les méthodes diverses utilisées me permettent d’en accélérer la venue !
Je ne suis pas devenu « illuminé » ni engagé dans des dérives irrationnelles ; je suis tout simplement aujourd’hui persuadé que l’on peut battre sur son terrain la maladie qui, si on n’y prend pas garde, nous envahi et nous rend esclave – je le sais pour l’avoir vécu au début comme tout un chacun. Mais je ne veux pas donner de leçon. Chacun se débrouille comme il peut pour vivre avec son Parkinson : c’est un combat de longue durée qu’il faut attaquer le plus tôt possible.
Tous mes vœux à chacun pour trouver son chemin d’espoir pour cette nouvelle année !
La lettre info du GP29 n°42
Publié le 07 janvier 2008 à 13:19Les vœux de la présidente, un article consacré à la nicotinothérapie, des dates à retenir, et de belles idées positives …
Tout ça, c’est là.
Nous étudions en ce moment la possibilité de mettre les archives de la Lettre en ligne.
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.
