Bilan des deux boursières soutenues par CECAP (1/2)
Publié le 27 décembre 2013 à 09:17Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Bilan de la thèse d’Elodie Mathieux : Le rejet suite à la greffe intracérébrale : étude de la réponse humorale et propriétés immunosuppressives des cellules souches.
La maladie de Parkinson est caractérisée par la dégénérescence progressive et sélective des neurones dopaminergiques de la voie nigrostriatale. La destruction des neurones dopaminergiques de la substance noire a pour conséquence une diminution de la sécrétion de dopamine au niveau du striatum.
Actuellement, il n’existe pas de traitement curatif de la maladie, mais différents traitements symptomatiques sont utilisés. L’administration par voie orale de L‑DOPA (lévodopa), précurseur de la dopamine capable de traverser la barrière hématoencéphalique, est l’un des traitements les plus couramment prescrits. Un inconvénient majeur de la prise de L‑DOPA est l’apparition, au bout de quelques années, de dyskinésies (mouvements anormaux). Une autre stratégie basée sur la stimulation électrique du noyau sous-thalamique montre une efficacité sur les troubles moteurs dans la plupart des cas, mais les risques chirurgicaux et les critères d’inclusion en font une opération accessible à un très faible nombre de patients. De plus, de nombreux symptômes ne sont pas corrigés par ces thérapies.
Aussi, il apparaît important de poursuivre les recherches sur les stratégies restauratrices, notamment la greffe intracérébrale de neuroblastes dopaminergiques fœtaux.
Des neuroblastes mésencéphaliques issus de fœtus humains (7 – 9 semaines) et transplantés dans le cerveau de patients parkinsoniens ont conduit à des améliorations cliniques basées, entre autres, sur la production de dopamine par les neurones greffés. Cependant, le recours à des cellules fœtales humaines est freiné par des considérations éthiques et logistiques qui limitent l’accès à ces greffes. Il est apparu alors nécessaire de se tourner vers d’autres sources cellulaires et notamment les cellules d’origine porcine.
En effet, le porc présente de nombreux avantages pour la xénotransplantation : un grand nombre d’embryons à chaque portée, une facilité d’élevage, la possibilité de contrôler la reproduction des animaux et de pouvoir pratiquer des manipulations génétiques. De plus, les neuroblastes issus de fœtus porcins émettent des neurites de longueurs similaires à celles observées chez l’Homme. Une survie des cellules greffées, une réinnervation du striatum ainsi qu’une récupération des fonctions motrices ont été observées lors d’essais cliniques menés chez certains patients parkinsoniens traités par des immunosuppresseurs (molécules permettant de limiter l’activité du système immunitaire). Mais le problème rencontré reste le rejet de ces greffes.
En effet, en l’absence d’immunosuppresseur comme la cyclosporine A, les greffes de neuroblastes porcins dans le striatum de rat sont systématiquement rejetées au bout de 7 – 8 semaines. Les traitements par des immunosuppresseurs prolongent la survie de la greffe, mais de manière transitoire. De plus, utilisés à fortes doses, ceux-ci entraînent des effets secondaires, notamment une toxicité rénale. Il est donc important de comprendre et d’étudier les mécanismes en cause dans le rejet pour envisager une survie à long terme de la greffe.
Diverses études ont mis en évidence un rôle important de la réponse immunitaire cellulaire dans le rejet. En effet, en l’absence d’immunosuppresseur, on observe vers 7 à 8 semaines une forte infiltration de la greffe par des lymphocytes T, des cellules dendritiques et des cellules microgliales activées.
Outre la réponse cellulaire, il a été observé un dépôt d’anticorps et de complément au niveau du greffon. Cette observation suggère une réponse humorale caractérisée par la production d’anticorps dirigés contre la greffe, qui, à ce jour, a été très peu étudiée.
Une partie de mon travail de thèse au sein de l’INSERM U1064 de Nantes a eu pour but de caractériser le rôle de la réponse humorale dans le rejet des xénogreffes intracérébrales.
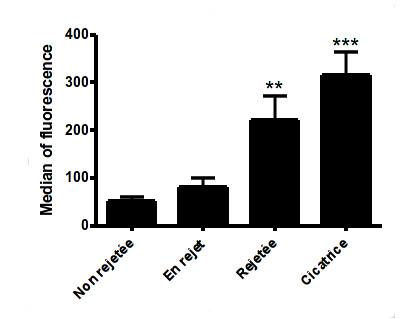
Evolution de la production d’anticorps au cours des différents stades du rejet.
Les anticorps produits suite à la greffe vont venir se fixer sur les cellules porcines du greffon et le détruire. Nous avons pu mettre en évidence que la production d’anticorps augmentait en fonction du délai post greffe et du statut de la greffe. En particulier, une forte concentration d’anticorps est observée dans le sérum de rats pour lesquels la greffe est rejetée. Les anticorps accompagnés d’une activation du complément seraient cependant, en premier lieu, attirés au sein de la greffe avant d’être détectés dans le sérum.
Evolution de la production d’anticorps au cours des différents stades du rejet.
Les anticorps vont préférentiellement venir se fixer sur les neurones et en moindre mesure sur les astrocytes. De plus, la survie des greffes de cellules mésencéphaliques porcines est augmentée chez des rats ne possédant plus d’anticorps. Ces résultats suggèrent un rôle important de la réponse humorale dans le rejet des xénogreffes intracérébrales.
Afin de limiter le rejet des greffes intracérébrales, une autre partie de mon travail a été d’étudier les propriétés immunosuppressives des cellules souches et en particulier des cellules souches neurales (CSN). Les CSN sont des cellules multipotentes capables d’auto-renouvellement et de prolifération. Elles peuvent générer les trois types cellulaires principaux du système nerveux central que sont les neurones, les astrocytes et les oligodendrocytes. Les CSN vont pouvoir être cultivées sous forme de neurosphères.
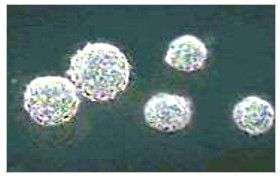
Cellules souches neurales de rat sous forme de neurosphères.
Nous avons pu démontrer que les CSN de rat inhibaient la prolifération des cellules T de rat de manière dose dépendante. Les CSN agissent alors par l’intermédiaire de facteurs solubles dont l’hème oxygénase.
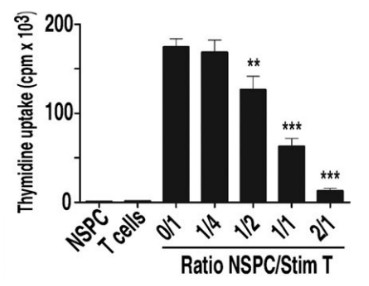
Inhibition de la prolifération des cellules T de rat par les cellules souches neurales de rat de manière dose dépendante.
Les CSN possèdent donc des propriétés immunosuppressives qui permettraient de limiter le rejet lors de greffes intracérébrales tout en diminuant l’utilisation d’immunosuppresseurs systémiques.
L’ensemble des résultats de ma thèse ouvre des nouvelles perspectives pour parvenir à contrôler le rejet de xénogreffes intracérébrales. En l’occurrence, on pourrait espérer qu’une immunosuppression locale, basée sur la transplantation de cellules souches associées à une administration systémique d’immunosuppresseurs ciblant les réponses humorales et cellulaires, soit suffisamment efficace pour assurer la survie à long terme de cellules neurales xénogéniques dans un cerveau.
Je tenais à remercier tous les membres de l’association CECAP pour leur soutien tout au long de ma thèse.
Rédigé par Elodie Mathieux
Pas encore de Commentaires Cliquer ici pour laisser un commentaire
Laisser un commentaire
Flux RSS des commentaires de cet article. Rétrolien URI
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.