La Xénogreffe de neurones porcins, vers une future thérapie de la maladie de Parkinson ?
Publié le 25 juin 2008 à 12:28Paru dans LE PARKINSONIEN INDéPENDANT n°33 – juin 2008
La maladie de Parkinson est une maladie neurodégénérative caractérisée par la perte bilatérale et progressive des neurones dopaminergiques de la voie nigro-striée. Ces neurones prennent naissance dans une petite zone du cerveau, la substance noire. Ils se projettent ensuite dans une région centrale du cerveau appelée le striatum. Ils y libèrent une substance, la dopamine, qui intervient dans les processus de désir, de plaisir et sur le bon fonctionnement des mouvements. La destruction de ces neurones caractérisant la maladie de Parkinson a pour conséquence une diminution du taux de dopamine au sein du striatum. Cette perte entraîne un déséquilibre dans la balance des molécules cérébrales et a pour conséquence l’apparition d’une triade de symptômes, caractéristique de la maladie, à savoir une akinésie (perte des mouvements), un tremblement de repos et une rigidité des membres.
La transplantation cellulaire est une des approches prometteuses dans le cadre du traitement des maladies neurodégénératives particulièrement pour la maladie de Parkinson. Des essais cliniques de greffes de neurones prélevés sur des fœtus humains ont déjà été réalisés chez l’homme. Malgré des résultats encourageants cette approche reste limitée par une barrière éthique quant à l’utilisation de matériel foetal humain. Les neurochirurgiens sont confrontés également à un problème de disponibilité en tissus foetal. En effet, la greffe d’un patient parkinsonien nécessite un apport de 7 à 8 fœtus. Ces barrières éthiques et logistiques impliquent donc la recherche et la mise au point de nouvelles sources cellulaires pour le futur traitement des malades.
La xénotransplantation correspond à une greffe réalisée d’une espèce à une autre. Dans notre cas, le porc semble être une espèce appropriée du fait de la similitude de taille d’organe ainsi que du développement embryonnaire très proche. Cependant, la réalisation d’une telle greffe pose rapidement des problèmes immunitaires. En effet, bien que le système nerveux central ait été considéré comme un site immunologiquement privilégié, ce n’est pas le cas car les xénogreffes de neurones sont systématiquement rejetées. L’administration systémique d’immunosuppresseurs est souvent très efficace pour le maintien de greffons dans les tissus périphériques mais de tels traitements pour maintenir des greffes intracérébrales provoquent de sérieux effets secondaires, notamment au niveau rénal, et ne fait que retarder le rejet cellulaire. Aussi, avons-nous comme objectif de développer des stratégies immunosuppressives locales.
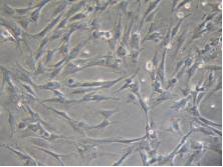
Les cellules souches mésenchymateuses (MSCs) (Fig. 1), cellules souches de la moelle osseuse chez l’adulte découverte à la fin des années 1960 par l’équipe de Friedenstein, possèdent de nombreuses caractéristiques intéressantes dans notre cas. Elles sont notamment connues pour libérer, après transplantation intracérébrale, quelques facteurs neurotrophiques connus pour leur protection sur les neurones dopaminergiques. Une deuxième propriété intéressante des MSCs, décrite par l’équipe d’Aggrwal, concerne leur capacité dite hypo-immunogène. En effet, ces cellules sont capables de sécréter des facteurs pouvant limiter les actions inflammatoires du système immunitaire.
Contrairement aux cellules fœtales (neuroblastes), les MSCs greffées survivent très longtemps dans un cerveau. Des MSCs humaines ont été observées jusqu’à 120 jours post implantation dans le cerveau de rats non traités. Nos travaux expérimentaux ont confirmé cette observation (J. Rossignol et L. Lescaudron de notre laboratoire). La capacité des MSCs à prévenir le rejet immunitaire après transplantation a déjà été reportée.
Outre les propriétés immunosuppressives des MSCs, nous avons récemment observé une forte activité neurotrophique des MSCs de rat. En effet, l’addition de MSCs issues de la moelle osseuse de rat à une culture de neuroblastes porcins augmente leur survie et leur transformation en neurones matures.
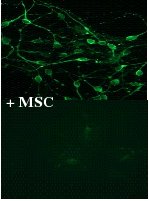
Sur la figure 2 (Fig. 2) nous visualisons qu’en présence de MSCs la survie des neurones porcins est plus importante.
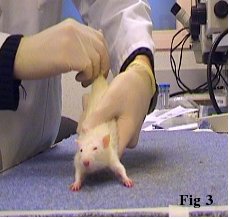
Enfin, dans le but de vérifier si la greffe de neurones porcins permet d’induire une récupération fonctionnelle, différents tests sont réalisés sur des rats lésés à la 6- Hydroxy-dopamine (un des modèles animaux de la maladie de Parkinson). L’injection de cette toxine dans le cerveau des rats induit la destruction spécifique des neurones dopaminergiques. Ces rats ont ensuite subi une co-greffe de neurones porcins et des cellules souches mésenchymateuses de rats. Les tests permettent de mesurer une possible récupération motrice des animaux. Le test du stepping par exemple permet de visualiser le nombre de redressements posturaux de chaque patte antérieure afin de quantifier l’akinésie des rats (Fig. 3).
La recherche s’est ainsi orientée ces dernières années sur la mise en place d’une thérapie cellulaire de la maladie de Parkinson. Elle suscite un grand espoir du fait notamment des résultats très encourageants observés lors d’essais cliniques chez l’homme. L’utilisation d’une nouvelle source cellulaire issue d’une espèce différente pour remplacer les neurones détruits au cours de la maladie semble être une bonne alternative. Nous fondons ainsi de réels espoirs sur les futures possibilités thérapeutiques d’une xénogreffe de neurones.
Rédigé par Xavier LEVEQUE
Doctorant INSERM u 643 de Nantes
Pas encore de Commentaires Cliquer ici pour laisser un commentaire
Laisser un commentaire
Flux RSS des commentaires de cet article.
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.