Pesticides : la maladie de Parkinson d’un ex-employé arboricole Reconnue d’origine professionnelle
Publié le 22 juillet 2019 à 08:54Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
Il n’existe aucune donnée statistique publique, à l’échelle nationale, sur les maladies professionnelles liées aux produits phytosanitaires.
Marcel Geslin, un ancien employé arboricole mort en 2018 à 74 ans, a obtenu lundi 11 mars la reconnaissance par la justice de l’origine professionnelle de sa maladie de Parkinson. « Ce n’est pas qu’une victoire pour l’honneur. Nous souhaitons qu’elle contribue à faire évoluer la législation sur les maladies professionnelles liées aux produits phytosanitaires, afin que ce qui est arrivé à mon frère n’arrive plus », a commenté Michel Geslin, frère et tuteur de Marcel, qui a mené le combat administratif pour obtenir cette reconnaissance devant le tribunal des affaires de Sécurité sociale (TASS) du Maine-et-Loire.
Employé pendant trente-sept ans dans la même entreprise arboricole à Loiré, à l’ouest d’Angers, où il a passé toute sa vie, Marcel Geslin était préposé à l’entretien des vergers, la taille, l’éclaircissage, la cueillette… « Il ne manipulait pas lui-même les produits phytosanitaires. Mais comme tous les employés à l’époque il travaillait dans les rangs pendant et après les traitements », rapporte Michel Geslin.
Apparus en 2008 après son départ en retraite, ses troubles ont été diagnostiqués « de type Alzheimer » avant d’être requalifiés en « maladie de Parkinson » quelques années plus tard, entraînant l’ouverture d’une demande de reconnaissance en maladie professionnelle provoquée par les pesticides.
« Cette reconnaissance nous a été refusée une première fois en 2017 parce que le certificat initial de son médecin traitant n’avait fait mention que de “troubles de mémoire”. Alors même que la MSA [Mutualité sociale agricole] disposait de tous les avis des spécialistes », regrette Michel Geslin. Un deuxième refus a été opposé à la famille en 2018 pour des questions de délai d’instruction. C’est l’avis du Comité régional de reconnaissance des maladies professionnelles de Bretagne, où le cas de Marcel Geslin a été délocalisé, qui s’est révélé décisif.
« C’est un cas emblématique car il montre que les organismes de protection sociale agricole, bien que parfaitement informés, préfèrent laisser filer. Pour qui veut faire reconnaître sa maladie, c’est un parcours du combattant », assure Michel Besnard, porte-parole du Collectif de soutien aux victimes des pesticides de l’Ouest, lequel revendique 14 reconnaissances auprès des TASS de la région depuis sa création il y a quatre ans.
A l’échelle nationale, il n’existe aucune donnée statistique publique sur les maladies professionnelles liées aux produits phytosanitaires. En 2017, Patrice Heurtaut, directeur de la santé et de la sécurité au travail de la MSA avait expliqué qu’elles représentaient « 2 % des maladies professionnelles déclarées au titre du régime agricole ». Phytovictimes, autre association d’aides aux victimes professionnelles, a recensé 429 dossiers depuis sa création, en 2011, dont 92 pour des maladies de Parkinson.
Lire aussi Agriculture : « Comprendre pourquoi l’usage de produits chimiques ne baisse pas »
Le Monde avec AFP Publié le
Transmis par Emilienne Six
Lu par Françoise Vignon
Parkinson : une étude confirme que la VR peut aider les malades
Publié le 19 juillet 2019 à 10:12Article paru dans LE PARKINSONIEN INDÉPENDANT n°7t
Selon une étude menée par des chercheurs de l’université de l’Utah, la réalité virtuelle aide véritablement les malades atteints de Parkinson à retrouver l’équilibre. L’équipe a observé un gain significatif sur des patients ayant suivi un programme de six semaines.

Qui a dit que la réalité virtuelle n’est réservée qu’aux “Gamers” avec une arobase ? Une nouvelle fois, une étude scientifique vient prouver les bénéfices de cette technologie d’un point de vue médical.
Des chercheurs de l’Université de l’Utah, aux États-Unis, l’ont utilisé pour voir ses effets sur des patients atteints de la maladie de Parkinson. Pour rappel, celle-ci provoque des tremblements des membres, mais surtout un déséquilibre constant qui entraîne régulièrement des chutes. La vie quotidienne empire en même temps que la maladie attaque les muscles.
Parkinson : une rééducation en réalité virtuelle
Les scientifiques ont donc mis au point un système de réalité virtuelle de type CAVE. Celui-ci leur offre un espace sécurisé afin d’améliorer leur contrôle musculaire et leur équilibre. L’appareil bénéficiait notamment d’une protection antichute. Évidemment, le fait d’essayer la VR ne suffit pas. Ce sont 10 patients qui ont profité d’un programme étalé sur six semaines.
Pendant trois séances de 30 minutes, ils devaient marcher sur un tapis roulant tout en évitant des obstacles dans le monde virtuel. Plus, ils contournaient les objets, plus ceux-ci grossissaient lors du tour suivant. Grossièrement, il faut s’imaginer le jeu du navigateur Google Chrome quand il est hors ligne, mais projeté sur un écran incurvé au sol et au plafond.
Contrairement à ce que l’on pourrait penser, les chercheurs ont remarqué l’effet bénéfique cette thérapie VR sur les malades de Parkinson. Au lieu de perdre l’équilibre comme certains, eux ont amélioré leur réactivité musculaire ainsi que leur maintien. Les observateurs ont noté une plus grande amplitude des mouvements de la hanche et de la cheville. Cela leur permet d’éviter plus facilement les chutes.
L’avenir : adapter la technologie à des casques VR
Cette recherche a été présentée entre les 6 et 9 avril, lors de la réunion annuelle de l’American Association of Anatomists, en Floride. Les chercheurs espèrent que le dispositif permettra aux patients de diminuer le nombre de chutes. Bien conscients que Parkinson est une maladie progressive, ils considèrent qu’une telle technologie améliorerait la vie des personnes concernées.
Par ailleurs, les scientifiques ne veulent pas se limiter à l’utilisation d’un système CAVE. En effet, cet environnement virtuel performant coûte cher et demande une logistique particulière. Ils comptent adapter leur outil à des casques VR, plus facile à déployer auprès des patients dans des centres de soins.
Enfin, les experts veulent maintenant comparer les progrès des malades de Parkinson ayant effectué le programme VR avec ceux qui bénéficient d’une autre méthode de rééducation, et ceux qui n’en ont pas du tout.
Pourquoi le vieillissement cérébral ?
Publié le 17 juillet 2019 à 10:55Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
Les conséquences
La première réponse à cette question de la dégénérescence du cerveau du « Parkinsonien » et de « l’Alzheimerien » est la constatation de la diminution des neurones et cellules gliales situées dans la substance noire, locus Niger pour la première pathologie, le stress cellulaire qui forment les fibrilles en régions temporale et de l’hippocampe, pour la seconde. Certains parkinsoniens ont malheureusement le risque de développer aussi cette diminution avec la dégénérescence neurofibrille. Le stockage mnésique est perturbé puis bloqué par les plaques Amyloïdes qui entravent les connexions et l’hippocampe est privé de communications ainsi que la perte des neurofibres. La cellule intrinsèque sera remplacée un temps par la protéine Amyloïde puis béta-Amyloïde puis la plaque du même nom faisant écran. Un éclairage supplémentaire sur l’Alzheimer, cette pathologie chez les anglo-saxons est appelée diabète type 3, simple à comprendre et nous met tout de suite « la puce à l’oreille » par un excès de certains nutriments et le manque d’élimination vont occasionner un stock cytotoxique.
Le scénario des causes au commencement de la maladie de Parkinson est quasi identique à l’Alzheimer même si la frontière paraît encore floue pour de nombreux spécialistes car ils se focalisent sur l’origine physiologique des symptômes, à mon humble avis le commencement n’est pas aux premiers signes mais bien avant, pourquoi ? Les zones touchées sont seulement différentes par le fait du hasard. Les récepteurs dopaminergiques ne sont plus réceptifs, une carence en dopamine progressive, car le cellulaire se meurt par l’inclusion des intrus (ex : excès de calcium d’origine mammifère). Les cellules dopaminergiques ont moins de protection. Les cellules du mouvement sont défaillantes comme les cellules nerveuses de la mémoire. Il faut noter que ce scénario est « joué » avec une grande variabilité d’un sujet à l’autre avec une réponse de « gravité » à « sévère ».
Les causes
La seconde réponse rarement développée vient étayer la première car, en moyenne le désordre apparait 40 à 50 ans après l’adolescence, suite d’une consommation déséquilibrée en nutriments essentiels et sans équilibre ACIDO-BASIQUE. Pour les officiels : « nous vivons plus longtemps qu’autrefois, [et ces maladies sont le] résultat d’une fatalité du vieillissement ». Cela plaît aux politiques et arrange bien les lobbies de l’agroalimentaire qui doucement nous empoisonnent par profits. Les années ont passé, la qualité nutritive des légumes et des fruits s’est appauvrie par les croisements, la productivité.
Une pomme d’un verger à grand rendement a 100 fois moins de vitamine C que la même variété produite il y a 50 ans. Sans vous détailler les pesticides, fongicides et engrais chimiques pour ces deux groupes. Le lait de vache (sauf lait cru bio) sous toutes ses formes, après la puberté est à bannir, car responsable de nombreux troubles.
Eviter l’alimentation acidifiante et oxydante, les barbecues, viandes grillées du week-end « carbonées = molécules de Maillard », alcool, cigarettes et les boissons avec ajout de gaz carbonique qui se balade dans le sang et ne sera pas expectoré en totalité. L’acidose que génèrent les barres sucrées chocolatées caramélisées. (Contenant bien souvent des nano particules d’aluminium, pour exemple : la mini surface de la coupe d’un cheveu représente équivalent de cent nano particules).
Quand l’acidose tissulaire devient chronique
Il faut impérativement équilibrer la consommation d’aliments acides oxydatifs par d’autres basiques alcalins (Ex : aliments antioxydants : Goyave, cassis, fraises, orange, citron, poivron rouge, betterave, brocoli, chou-fleur, noix, noisette, épinard, carotte, patate douce, tomate crue (de saison), foie de veaux, bœuf rôti ou cru, blanc de poulet, œuf, gingembre, cacao, thé vert… ). Dans toute pathologie le pH(pH Potentiel Hydrogène, facilement contrôlable avec des languettes de papier dédiées, vendues en pharmacie.) urinaire est acide, alors que pour le bien portant le pH est neutre, proche du pH sanguin. L’acidose tissulaire complexe peut se définir comme l’évidence de l’intoxication des tissus et de l’encrassage de l’organisme surtout d’origine alimentaire, ainsi que la production excessive d’acides endogènes, comme l’acide lactique produit par un effort sportif intense.
Les acides sont libérés par la fermentation dans l’intestin due à la consommation excessive de protéines animales et de produits laitiers génératrice d’acide sulfurique. L’excès de ce mauvais calcium sur les neurones dopaminergiques agit comme un empoisonnement, ils deviennent donc plus vulnérables à l’oxydation. La caséine, les peptides et débris bactériens dans l’intestin vont perturber le système immunitaire, celui-ci va donc fabriquer des anticorps, or ces anticorps vont finir par faire la confusion avec les structures de l’individu, et vont se retourner contre elles créant ainsi une affection auto-immune.
La gravité même, puisque ces cellules blanches vont s’attaquer à certains organes et empêcher l’absorption de minéraux. D’autres acides viendront amplifier le problème. Mais il existe la parade, l’équilibre se maintient par l’apport normalement de ions alcalins, comme le potassium ou le magnésium provenant des légumes et des fruits d’une bonne qualité nutritive. Or l’alimentation dite moderne n’apporte plus suffisamment de micronutriments, comme les minéraux alcalinisant ainsi que toute la panoplie des vitamines et enzymes. En revanche, le Bio est notre salut ainsi que le jardin potager sans ajout, dit phytosanitaire, sans oublier les maraîchers engagés dans l’agriculture dite responsable.
Le corps devient un producteur d’acides pour le cerveau bien que l’acidose soit métaboliquement régulée par tout un système tampon (Glutathion), l’organisme s’acidifie avec les années et ne s’alcalinise que très rarement pour les raisons expliquées plus avant. Les catalyseurs activateurs des enzymes sont carencés en vitamines et micronutriments, les acides aminées ne parviennent plus aux cellules de notre cerveau, ces acides ne sont pas évacués car non reconnues ; ils se fixent sur les fibres des tissus conjonctifs – la structure tissulaire de soutien de tous les organes – empêchant une bonne oxygénation et l’alimentation des cellules.
Cette fixation des déchets bloque les échanges indispensables avec les cellules des organes. L’acidification tissulaire provoque un enraidissement généralisé bloquant en partie les échanges de la nutrition : des fibrilles, des corps de Lewy, des protéines Tau, vont former une enveloppe de gel qui tend à se rigidifier plus ou moins hermétiquement, bloquant en partie les échanges de la nutrition, et privant ainsi le cerveau de « carburant protéines glucose ». Avec les années, le déroulement de ce scénario provoque une diminution du cerveau : la sénilité en sera malheureusement la fin.
Conclusion : Il se produit, alors, petit à petit un état de souffrance des organes avec anoxie, malnutrition, auto-intoxication cellulaire qui aboutissent à cette mort cellulaire des neurones et cellules nerveuses. Pour une explication plus simple nos cellules baignent dans une lymphe toxique acidifiée avec déchets. C’est le processus de dégénérescence, le mécanisme du vieillissement accéléré (sénescence), Alzheimer, Parkinson, Sclérose en Plaques, douleurs articulaires, arthrose, maladies auto-immunes, asthme, allergies, diabète type 1, 2, 3 ! Etc.
Et notre patrimoine génétique alors ?
Le patrimoine génétique a une infime part de « responsabilité de protection ou pas » la grande majorité de personne est protégée, en fonction de la susceptibilité du génome, qui va retarder au maximum le déséquilibre de cette inflammation chronique, à condition de ne pas abuser d’une mauvaise hygiène de vie. Il existe une exception que je qualifie de malheureuse : « les sujets porteurs d’une mutation monogéniques de la maladie de Parkinson, la mutation dite PARK2 sur le gène d’une protéine du nom de parkine et de la mutation PARK6 protéine du nom de PINK1. Dans ces deux cas la maladie à un début très précoce, vers la vingtième année, l’évolution est très lente et répond bien à la L‑Dopa », (Professeur A. Nieoullon).
Une seule solution nourrissez bien votre cerveau.
Un nouveau traitement à l’essai
Publié le 11 juillet 2019 à 08:35Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
Des personnes souffrant d’un stade avancé de la maladie de Parkinson retrouvent espoir grâce à un nouveau traitement développé par des chercheurs de la Western University de Londres, en Ontario (Canada).
Les scientifiques ont testé sur un petit nombre de patients un implant chargé d’envoyer une impulsion électrique au niveau des vertèbres thoraciques afin de stimuler la colonne vertébrale. Le professeur Mandar Jog de la Western University a expliqué à la BBC que l’ampleur de ce nouveau traitement allait « au-delà de ses rêves les plus fous ».
Lorsque l’on se déplace, le cerveau envoie les instructions aux jambes. En retour, celui-ci reçoit le signal une fois que le mouvement a été réalisé. Le professeur Mandar Jog explique que la maladie de Parkinson affaiblit le signal retour, « cassant la boucle » et empêchant ainsi le patient de continuer à se déplacer. Ce phénomène est appelé le freezing.
Le stimulus électrique semble contrer, ou du moins réduire, ce blocage, en améliorant le mécanisme de retour vers le cerveau des informations sensorielles issues de jambes. Cette avancée rejoint les progrès réalisés par la stimulation cérébrale profonde, une technique développée dans les années 1990 par des Français et qui a déjà aidé de nombreuses personnes atteintes de la maladie de Parkinson.
Une avancée porteuse d’espoir
Surpris de leur trouvaille, les chercheurs ont aussi découvert que les effets bénéfiques de l’implant persistaient même après l’arrêt de la stimulation de la moelle épinière. Autre point positif : un regain de confiance chez les patients dans leur capacité à marcher.
Il s’agit bien là d’une avancée, qui pourrait effectivement se traduire par une amélioration de l’état de certains malades”, souligne André Nieoullon, professeur de Neurosciences à l’Université d’Aix-Marseille, interrogé par le site d’information Atlantico.
L’ancien président du Conseil scientifique de France-Parkinson tempère : « Bien que les résultats soient encourageants, il ne s’agit pour le moment que d’études pilotes, sur un très faible nombre de malades. » En France, près de 160.000 personnes sont atteintes de la maladie de Parkinson, et environ 8.000 nouveaux cas sont détectés chaque année.
Journal le HUNTINGTON POST 24/04/2019
Par Martine Delmond
La démence à corps de Lewy est l’un des syndromes parkinsoniens atypiques. Elle est caractérisée par une attention fluctuante, des troubles moteurs et des hallucinations.
Publié le 08 juillet 2019 à 21:46Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
La démence à corps de Lewy (DCL) se manifeste par un déclin des fonctions cognitives qui interfère avec la vie sociale ou professionnelle. Des troubles de la mémoire peuvent être présents au stade précoce ou terminal de la maladie. Ils sont parfois associés à des troubles de l’attention et à des troubles des fonctions dites « exécutives » (qui permettent de gérer les situations complexes ou imprévues), ainsi qu’à des difficultés à traiter des informations visuelles dans l’espace.
Un syndrome parkinsonien généralement peu sévère, akinéto-rigide et tremblant, peut se manifester au début ou en fin de maladie. Souvent précédé de chutes inopinées sans raison apparente, il répond partiellement à de faibles doses de dopamine. D’importantes fluctuations de l’attention et instabilités psychiques, parfois au cours d’une même journée ou sur plusieurs jours, accompagnées d’une confusion intermittente voire de périodes de quasi-absence, distinguent la DCL de la maladie d’Alzheimer.
Citons également les critères de distinction suivants : hallucinations visuelles précoces, récurrentes, bien formées et détaillées, dans certains cas interprétations délirantes comme le syndrome de Capgras (le conjoint n’est pas le conjoint mais un sosie), dysperceptions, besoin de sommeil accru, troubles du comportement du sommeil paradoxal présents depuis plus de dix ans (cris, paroles, rires, ou agression du conjoint en raison d’un défaut d’inhibition des mouvements générés par les rêves), fortes variations de la tension artérielle, sensations de vertiges au lever, incontinence, anxiété fluctuante et épisodes dépressifs avec apathie. On observe souvent des réactions paradoxales à certains médicaments (par exemple neuroleptiques).
On peut la diagnostiquer grâce à des procédés d’imagerie comme la tomographie par émission de positons (PET scan FDG), qui met en évidence une diminution du signal plus postérieure que celle de la maladie d’Alzheimer (pariétooccipitale préservant le cortex cingulaire postérieur). En cas de DCL, la scintigraphie de type DaT-scan ou le SPECT au bêta-CIT révèlent une perte globale de la captation de la dopamine dans les noyaux gris. L’examen du cerveau des patients parkinsoniens révèle que les corps de Lewy, observés essentiellement dans le tronc cérébral, le système végétatif et les viscères, sont diffus dans tout le cerveau. Une forme mixte associée à la maladie d’Alzheimer et une variante d’évolution très rapide sont également décrites.
Traitement :
Le traitement consiste à administrer de faibles doses de dopamine et des inhibiteurs de la cholinestérase (rivastigmine en premier choix), plus efficaces qu’en cas de maladie d’Alzheimer. Les hallucinations, les délires et les troubles comportementaux sont traités par quétiapine ou clozapine. Compte tenu d’une éventuelle hypersensibilité, ces médicaments doivent toutefois être utilisés avec parcimonie. Les troubles du comportement du sommeil paradoxal sont traités par clonazépam, gabapentine ou mélatonine.
Prof. Dr méd. Joseph-André Ghika
Membre du comité consultatif de Parkinson Suisse, est le médecin-chef du service de neurologie à l’Hôpital du Valais.
Lu dans « Parkinson Suisse »
N° 132 décembre 2018
Par Jean Graveleau
La maladie à corps de Lewy, colloque 8 janvier 2019
Publié le 07 juillet 2019 à 11:16Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
Elle est la seconde maladie neurodégénérative à impact cognitif la plus fréquente après la maladie d’Alzheimer. La maladie à corps de Lewy (MCL) est une maladie complexe qui remprunte certains symptômes à la maladie d’Alzheimer et d’autres à la maladie de Parkinson. Elle est donc difficile à reconnaître ou à diagnostiquer. Moins connu que la maladie d’Alzheimer ou la maladie de Parkinson, la maladie à corps de Lewy atteint pourtant plus de 200 000 personnes en France et l’on estime à ce jour que 67% des personnes malades ne sont pas, à ce jour, diagnostiquées.
S’il est une caractéristique de la maladie à corps de Lewy c’est bien le phénomène des fluctuations dont il s’agit. Ces fluctuations sont des changements imprévisibles dans la concentration, l’attention, la vigilance et l’éveil. Ils peuvent apparaître d’un jour à l’autre ou même d’une heure l’autre. Une personne atteinte de la MCL peut regarder dans le vide pendant une longue période ou sembler somnolente ou léthargique et passer beaucoup de temps à dormir. Les idées peuvent être confuses sans logique apparente ou aléatoires. Mais à d’autres moments, la même personne sera alerte, capable de mener une conversation lucide, rire d’une blague ou même suivre un film. Bien que ces fluctuations soient courantes, elles ne se produisent généralement pas en présence d’un professionnel de santé, ce qui peut rendre le diagnostic encore plus difficile.
Face à la complexité de la maladie, à ses manifestations cliniques particulières, comme les fluctuations mais aussi les hallucinations ou les troubles du sommeil paradoxal les professionnels de santé eux-mêmes sont parfois démunis. En collaboration avec le ministère de la Santé, France Alzheimer et maladies apparentes s’est naturellement associée à France Parkinson et au réseau des aidants de la maladie à corps de Lewy pour organiser le premier colloque sur la maladie. Il s’est tenu le 8 janvier 2019 dans les locaux du ministère de la Santé regroupant : experts de la maladie, psychiatre, neurologue, gériatre, médecin généraliste, kinésithérapeute, orthophoniste et expert psychologue mais aussi personnes malades et proches aidants ont apporté leur concours à cette journée exceptionnelle.
Un dépliant résumant les symptômes et les démarches à faire face à cette maladie à corps de Lewy est actuellement à disposition de chacun auprès de France Parkinson : faites-en la demande.
Actes du colloque lus
par jean Graveleau
Qu’est-ce que la maladie de Parkinson (Par Parkinson Suisse du mois de décembre 2018)
Publié le 06 juillet 2019 à 13:26Article paru dans LE PARKINSONIEN INDÉPENDANT n°77
Epidémiologie du Parkinson
Fréquence
Le syndrome parkinsonien (maladie de Parkinson) figure parmi les neuropathologies les plus fréquentes. On dénombre près de 6,3 millions de patients dans le monde. Selon différentes études, leur nombre passera à près de 8,7 millions d’ici 2030. Plus de 15 000 parkinsoniens vivent en Suisse. Le Parkinson frappe environ 1 % des plus de 60 ans et 3 % des plus de 80 ans. Un patient sur cinq est âgé de moins de 60 ans lors du diagnostic. Les hommes et les femmes sont presque autant touchés les uns que les autres.
Transmissibilité
La maladie est héréditaire dans 5 à 10% des cas, pour lesquels la cause réside dans la déficience d’un certain gène. Pour autant, les facteurs de risque génétique jouent également un rôle dans la forme non héréditaire du Parkinson.
Espérance de vie
L’espérance de vie des parkinsoniens est presque aussi élevée que celle des personnes en bonne santé.
Ce qui se passe dans l’organisme
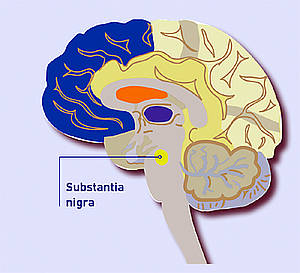
Le Parkinson est une maladie neurodégénérative qui provoque la disparition progressive des neurones dans le cerveau. Au cours des premières années de la maladie, c’est la destruction des neurones responsables de la production de dopamine (neurotransmetteur) dans la substantia nigra (substance noire, située dans le cerveau moyen) qui figure au premier plan. La carence en dopamine qui en résulte est à l’origine de divers troubles de la motricité.
Ces derniers peuvent être traités de manière adéquate par administration de L‑Dopa, le précurseur de la dopamine. Toutefois, relativement tôt dans l’évolution de la maladie, des neurones qui n’ont rien à voir avec la production de dopamine meurent dans d’autres régions du cerveau. Ce processus génère une série de symptômes (par ex. troubles végétatifs, douleurs, troubles du sommeil, symptômes psychologiques) qui deviennent de plus en plus pénibles pour les patients au fur et à mesure que la maladie progresse. Malheureusement, les possibilités thérapeutiques pour lutter contre ces symptômes sont encore très limitées.
Causes du Parkinson
Bien que la maladie de Parkinson ait été décrite pour la première fois en 1817 par le médecin anglais James Parkinson, et malgré les importants efforts déployés par la recherche, ses causes restent inexpliquées. Il semble néanmoins qu’elle résulte d’une combinaison de facteurs environnementaux et d’une prédisposition génétique. Jusqu’à présent, aucun facteur particulier n’a pu être identifié comme étant le seul déclencheur. Il est possible d’en atténuer les symptômes, mais à ce jour rien ne permet de ralentir ou de stopper sa progression.
Les symptômes du Parkinson
Les symptômes de la maladie de Parkinson varient considérablement d’une personne à l’autre. De même, la maladie ne progresse pas au même rythme chez toutes les patientes et tous les patients. Chacun est atteint de « son » Parkinson, caractérisé par une symptomatologie unique.
- Ralentissement des mouvements (bradykinésie, akinésie) Les successions de mouvements fluides sont de plus en plus difficiles. Ce sont principalement les automatismes primaires comme la marche ou l’écriture – que les personnes en bonne santé effectuent sans réfléchir – qui défaillent, mais la motricité fine est également affectée. Cette akinésie augmente au fur et à mesure que la maladie progresse.
- Rigidité (raideur) La maladie de Parkinson accroît en permanence la tonicité des muscles, notamment dans les bras et les jambes. Les patients ont l’impression que leurs membres sont « paralysés » et souvent, ils souffrent de crampes douloureuses. Leur position voûtée est elle aussi une expression de la raideur musculaire accrue.
- Tremblements de repos Les tremblements de repos, qui se manifestent chez près des deux tiers des parkinsoniens, sont souvent plus prononcés d’un côté aux stades précoces de la maladie. Les bras sont généralement plus fortement touchés que les jambes. Les tremblements disparaissent lors des mouvements ciblés.
- Instabilité posturale L’équilibre est assuré par un système de régulation complexe, dans lequel les réflexes automatiques posturaux et stationnaires jouent un rôle central. Aux stades avancés de la maladie de Parkinson, sa perturbation peut entraîner des chutes dangereuses.
- Autres symptômes Parmi les autres symptômes fréquents de la maladie de Parkinson, on compte les problèmes psychologiques (par ex. les dépressions), les troubles du rythme circadien veille-sommeil et les troubles du système nerveux végétatif (régulation de la tension artérielle, digestion et régulation de la température). Aux stades avancés, les troubles cognitifs ne sont pas rares.
Évolution du Parkinson
L’atrophie cellulaire dans la substantia nigra progressant constamment, les symptômes se multiplient également. Les foulées rapetissent. Les tâches de précision (se laver les dents, fermer des boutons, écrire, bricoler) sont de plus en plus pénibles, la voix devient souvent plus basse et elle perd de son intelligibilité. La mimique diminue, le corps a parfois tendance à se courber vers l’avant. Il faut savoir que la progression de la maladie et sa symptomatologie sont très personnelles.
Son évolution et son degré de gravité varient considérablement selon les patients. Les deux à cinq premières années de la maladie, pendant la phase dite de « lune de miel », le traitement antiparkinsonien médicamenteux est simple, fiable et efficace ; la plupart des patients peuvent vivre quasiment normalement. Au cours de cette première phase, l’action médicamenteuse est très équilibrée pendant la journée ; les fluctuations sont rares, voire complètement absentes,
Malheureusement, à mesure que la maladie progresse, l’effet des médicaments s’affaiblit. Le contrôle des symptômes devient plus difficile et varie pendant la journée. Les mouvements excessifs involontaires (dyskinésies), qui alternent avec des phases d’immobilité marquée, constituent une conséquence des fluctuations d’action. À ce stade, il n’est pas rare que les symptômes non moteurs (dépressions, troubles cognitifs, troubles de la digestion, fluctuations de la tension artérielle, etc.) augmentent également
Compte tenu des variations d’action, les intervalles entre les prises de médicaments doivent être réduits. Il est également possible d’utiliser les médicaments en association avec des substances qui prolongent leur action. Afin d’optimiser le réglage, les neurologues traitants doivent laisser à la personne concernée suffisamment de temps pour décrire ses symptômes et le moment de leur apparition. Une étroite collaboration entre le médecin et le patient est indispensable.
Aux stades avancés, il peut s’avérer utile de procéder à des bilans stationnaires dans un centre Parkinson spécialisé. Au cours du séjour, l’effet des médicaments et les symptômes peuvent être contrôlés précisément sur une plus longue période et le traitement peut être adapté en conséquence. Par ailleurs, la neuroréadaptation (logopédie, ergothérapie et physiothérapie) est essentielle. Les programmes d’exercices et de traitement ciblés qui sont élaborés peuvent aider les parkinsoniens à mieux gérer leur quotidien
Quand les médicaments par voie orale ne permettent plus de contrôler les symptômes de manière satisfaisante, les thérapies par pompe (apomorphine ou Duodopa®) ou les méthodes chirurgicales (stimulation cérébrale profonde) peuvent être envisagées. Ces traitements invasifs ont fait la preuve de leur efficacité.
Aujourd’hui, les patients ont une espérance de vie presque normale et leur qualité de vie peut être stabilisée très longtemps à un bon niveau ou tout au moins à un niveau acceptable.
Diagnostic du Parkinson
La maladie de Parkinson commence presque toujours par des phénomènes d’indisposition physique. Ils ne sont pas caractéristiques et ils ne se précisent que peu à peu. Au cours de cette phase, le médecin traitant est l’interlocuteur privilégié. Il est essentiel d’observer les changements et les symptômes sur une longue période, tout en les consignant dans un « journal » qui sera ensuite présenté au médecin. En effet, ce dernier a besoin du plus grand nombre d’informations possible. Plus le diagnostic est établi rapidement, mieux c’est.
À l’heure actuelle, le diagnostic du syndrome parkinsonien idiopathique est principalement clinique. Il repose sur les antécédents symptomatiques et les investigations neurologiques. Les examens complémentaires tels que l’IRM crânienne, la tomographie par émission de simples photons (TEMP) et l’échographie apportent une confirmation.
Pour établir le diagnostic clinique, la bradykinésie et au moins un autre symptôme (par exemple les tremblements ou la raideur) doivent être présents. La réaction à la L‑Dopa est un important critère d’aide pour diagnostiquer la maladie de Parkinson.
Syndromes parkinsoniens atypiques
Quatre parkinsoniens sur cinq souffrent du syndrome parkinsonien idiopathique (ou maladie de Parkinson). Beaucoup plus rares, les autres syndromes parkinsoniens atypiques sont moins connus. De nombreux syndromes parkinsoniens atypiques (SPA) gravitent dans l’orbite de la maladie de Parkinson, c’est-à-dire du syndrome parkinsonien idiopathique, forme la plus fréquente et la plus connue. Ils se différencient difficilement les uns des autres. On distingue : l’atrophie multi-systématisée (AMS), la paralysie supranucléaire progressive (PSP), la dégénérescence cortico-basale (DCB), la démence à corps de Lewy (DCL)
Pour diagnostiquer à coup sûr un syndrome parkinsonien atypique (SPA), seul le diagnostic pathologique du tissu cérébral (par biopsie ou autopsie) est fiable. Il est impossible de le réaliser sur des patients en vie. Aussi, de nos jours le diagnostic repose-t-il uniquement sur des critères cliniques – et le taux d’erreur peut atteindre 30 %. L’existence de plusieurs listes de critères pour un même groupe de symptômes dans le cas de différents syndromes parkinsoniens atypiques prouve l’incertitude qui prévaut lors de l’établissement du diagnostic.
Il en va de même des révisions internationales récurrentes des critères de diagnostic clinique en vigueur (DCB, PSP). À ce jour, jamais ces critères n’ont été validés de manière prospective ni confirmés sur le plan clinique-pathologique pour chaque SPA. En outre, les études publiées ces dernières années ont révélé un élargissement du champ des symptômes et troubles cliniques possibles, ce qui accroît la complexité du diagnostic précoce de tous les SPA.
La différenciation des différents SPA entre eux et par rapport au syndrome parkinsonien idiopathique (SPI) est cruciale, surtout aux stades précoces de la maladie. Il serait en effet possible d’établir plus aisément un pronostic et de mettre en place un traitement adéquat. Par ailleurs, un diagnostic précoce univoque est fondamental pour le progrès scientifique et une meilleure connaissance des causes de la maladie, ainsi que pour la recherche de nouvelles options thérapeutiques. Malgré plusieurs décennies de recherche, l’étiologie et les mécanismes pathologiques des SPA restent incertains. Sur le plan thérapeutique, les possibilités actuelles sont encore très limitées
Les procédés d’imagerie médicale (IRM) et les méthodes de diagnostic de laboratoire disponibles actuellement ne permettent guère d’établir un diagnostic précoce fiable. En conséquence, la recherche s’oriente vers de nouveaux biomarqueurs (mesures spécifiques à un SPA). Ils sont par exemple intégrés dans des analyses génétiques ou des méthodes d’essai en laboratoire permettant l’examen du sérum ou du liquide céphalo-rachidien. On les utilise aussi dans des procédés d’imagerie fonctionnelle spécifiques
Prof. Dr méd. Mathias Sturzenegger
Numéro 132 du Parkinson Suisse décembre 2018
Jean Graveleau
Evaluation des technologies santé : un règlement européen à corriger
Publié le 03 mai 2019 à 08:24Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
En janvier 2018, la Commission européenne a publié un projet de règlement très offensif vis-à-vis de l’activité d’évaluation des technologies de santé (médicaments et certains dispositifs médicaux) telle que réalisée par exemple en France par la Commission de la transparence de la Haute autorité de santé (HAS). Pourquoi ?
Accélérer l’accès des firmes au marché -
La Commission européenne propose de rendre obligatoire, via ce règlement, une évaluation commune à l’ensemble des agences d’évaluation des technologies de santé nationales, et d’interdire les réanalyses au niveau national. (1)
Le Commissaire européen concerné et certaines associations de patients justifient cette proposition par le fait que le travail des agences nationales entraînerait des retards inacceptables pour l’accès des patients à « l’innovation » et des inégalités entre patients d’un pays à l’autre. (2 – 3)
Erreur d’analyse et vraie motivation -
L’obstacle principal et grandissant à l’accès aux nouveaux médicaments n’est pas la lenteur des agences d’évaluation des technologies de santé, mais le prix exorbitant des médicaments, demandé par les firmes. Face au grand laxisme de l’Agence européenne du médicament (EMA) dans la procédure d’autorisation de mise sur le marché (AMM), certaines agences nationales d’évaluation des technologies de santé sont parfois les seuls acteurs officiels à publier des informations critiques sur les médicaments plus dangereux qu’utiles. Neutraliser ces agences s’intègre dans la stratégie de ceux qui rêvent d’un accès sans entrave à « l’innovation » quel que soit son intérêt sanitaire …
Exiger des essais comparatifs -
Les « lenteurs » des agence nationales d’évaluation des technologies de santé tiennent avant tout à la piètre qualité de l’évaluation des nouveaux médicaments, rendant difficile la détermination de leur valeur thérapeutique ajoutée. Pour faciliter l’accès aux progrès thérapeutiques, le règlement européen pourrait améliorer le service aux patients : en demandant aux firmes de fournir aux agences d’évaluation des technologies de santé les données comparatives dont celles-ci ont besoin, et cela dès le dépôt du dossier de demande d’AMM.
Les députés européens auront à se prononcer à l’automne 2018 sur ce projet de règlement. Ils ont le pouvoir de le rendre vraiment utile aux patients en incitant les firmes à davantage chercher des progrès thérapeutiques tangibles, et non à accéder encore plus vite et plus facilement au marché.
Extraits de la veille documentaire Prescrire
1- Proposition de règlement du Parlement européen et du Conseil concernant l’évaluation des technologies de la santé et modifiant la directive 2011/24/U – 2018/0018 (CDO) 31 janvier 2018
2- « O&R : Proposition de la Commission concernant l’évaluation des technologies de la santé – Fiche d’information » Commission européenne 31 janvier 2018
3- « Transparency and Health Technology Assessment cooperation as proposed by the Regulation are the only real antidote to secrecy and political games » Eurordis mars 2018
Article relevé dans Prescrire d’août 2018
Par Françoise Vignon
Comité interministériel du handicap (CIH)
Publié le 29 avril 2019 à 10:14Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Cap 2018 – 2019 -
- Elargir l’accès aux plateformes d’intervention départementale pour l’accès aux soins et à la santé aux personnes en situation de handicap afin de mieux orienter et accompagner les personnes en s’appuyant sur le développement de partenariat et l’utilisation de base de données.
- Fusionner la CMU‑C et l’aide au paiement d’une complémentaire santé (ACS) permettant aux personnes bénéficiant de l’AAH, de bénéficier d’une couverture santé sans reste à charge.
- Engager la révision de la liste des produits et prestation remboursables (LPPR) par l’ Assurance Maladie qui intègre des dispositifs médicaux pour traitements et matériels d’aide à la vie, aliments diététiques et articles pour pansements, des orthèses et prothèses externes, des dispositifs médicaux implantables et des véhicules pour les personnes handicapées et actualiser l’arrêté fixant les tarifs de la prestation de compensation du handicap (PCH) concernant les aides techniques, en cohérence avec les évolutions de la LPPR et l’évolution des besoins.
- Clarifier les frontières des activités de soins des établissements médico-sociaux et l’utilisation des soins de ville, afin de ne pas pénaliser les personnes en situation de handicap dans leur accès aux soins.
- Intégration d’un module « Handicap » dans la maquette de la formation initiale des médecins (1re année d’internat)
- Inscription de l’objectif d’amélioration de l’accès aux soins des personnes en situation de handicap dans la Stratégie nationale de santé (2018 – 2022), décliné au sein des nouveaux Plans Régionaux de Santé (PRS)
Priorités fixées lors du CIH du 25 Octobre 2018 -
- Le Gouvernement s’engage à faciliter la vie des personnes en situation de handicap en leur permettant notamment de bénéficier de droit à vie en déclarant une seule fois leur handicap. C’est une simplification pour les personnes et pour leurs aidants, dans le quotidien, mais aussi pour les Maisons départementales des personnes handicapées départementales des personnes handicapées (MDPH) qui pourront ainsi libérer leur temps pour d’avantage de conseil et d’accompagnement des personnes, un soutien de proximité pour faciliter les parcours. Cette simplification, c’est également un nouveau contrat de confiance entre les citoyens, les MDPH, les administrations.
- L’accès aux soins : pour le CIH, l’accès aux soins est une priorité pour 2018 – 2019. Parmi les mesures majeures : l’accès pour tous aux complémentaires santé.
- Développer les nouvelles technologies : le développement des nouvelles technologies et l’essor de l’intelligence artificielle seront les atouts importants pour le quotidien des personnes en situation de handicap. Il convient de mettre en les liens les start-ups et les développeurs de projets avec les personnes en situation de handicap, pour développer des produits innovants adaptés, les tester, les référencer, assurer leur prise en charge financière.
Extrait du Communiqué de presse Handicap Infos du 26/10/18
Article relevé par Françoise Vignon
Trois nouvelles pistes pour stimuler le cerveau
Publié le 25 avril 2019 à 15:40Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Surveiller sa vue protège le cerveau :
- De plus en plus d’études tendent à relier la baisse d’acuité visuelle au déclin cognitif. Les yeux ne sont pas que le miroir de l’âme. Ils sont aussi étroitement connectés au cerveau puisque 80% des informations perçues par ce dernier viennent des yeux. On sait aussi que les personnes touchées par la maladie d’Alzheimer présentent d’importantes atteintes au niveau du nerf optique et de la rétine et que le risque d’être affecté par une perte de l’acuité visuelle est 2 à 3 fois plus élevé chez les personnes souffrant d’un dysfonctionnement cognitif.
- Selon les dernières découvertes, les problèmes visuels précéderaient l’apparition de problèmes cognitifs et pourraient ainsi se poser en marqueurs précoces des maladies d’Alzheimer et Parkinson. Notamment en cas d’amincissement élargi du centre de la rétine, (mesurable par une technique d’imagerie 3D dite TCO : Tomographie en Cohérence Optique), lequel serait observé dès les premiers stades de ces maladies.
- Si ces conclusions sont confirmées, cet examen utilisé pour dépister glaucome et DMLA pourrait devenir un outil de diagnostic cognitif. Faire surveiller étroitement sa vue est donc primordial pour bien voir mais aussi prendre en charge au plus tôt les pathologies neuro-dégénératives.
Bien mastiquer stimule le cerveau :
- On savait la mastication essentielle à la bonne digestion et au maintien de l’équilibre pondéral. Plusieurs études suggèrent qu’elle est également impliquée dans la stimulation du cerveau. Statistiquement, la perte de la dentition et donc la diminution de la mastication ainsi que le manque de soins dentaires, sont d’ailleurs associés à un grand nombre de maladie d’Alzheimer (maladie plurifactorielle).
- Différents paramètres expliqueraient ces liens. L’absence de mastication limiterait la stimulation sensorielle (c’est en étant broyés que les aliments libèrent leur goût), un des facteurs de la stimulation de la mémoire. Elle limiterait aussi l’apport de glucose vers le cerveau, ce qui aurait un effet sur la mémoire immédiate et les facultés de calcul. Par ailleurs, l’imagerie médicale montre que la mastication est corrélée à la stimulation de certaines zones du cerveau (celles liées à l’exécution du mouvement et de l’attention) ainsi qu’à la stimulation de l’hippocampe, zone de la mémoire à long terme.
- Veiller à sa santé bucco-dentaire est donc essentiel pour le cerveau. Car outre le défaut de mastication (pour qu’elle soit efficace il faut au moins une vingtaine de dents) qui entraîne aussi une dénutrition délétère, une mauvaise hygiène de la flore buccale lui est aussi dommageable.
Préserver son microbiote agit sur le cerveau :
- On sait désormais que notre intestin, qualifié de « deuxième cerveau » possède près de 200 millions de neurones et communique en permanence avec notre système nerveux central et ses 100 milliards de neurones. On sait aussi que les milliards de bonnes bactéries qui composent notre microbiote intestinal influent sur notre santé si certaines viennent à manquer et d’autres à dominer. Le lien entre 1er et 2ème cerveau est maintenant clairement établi.
- Parkinson, Alzheimer … Les maladies neuro-dégénératives ont pour point commun la mort des neurones, notamment associée à une accumulation de protéines dites amyloïdes. Or, les dernières recherches ont démontré que ces agrégats protéinés sont initialement produits au niveau de l’intestin (parfois 20 ans avant le diagnostic de la maladie) avant de migrer et d’affecter le système nerveux central…
- Plusieurs hypothèses expliquant ce cheminement font actuellement l’objet d’études. Mais il est certain que la santé du cerveau étant intimement liée à celle du microbiote intestinal, il faut tout mettre en œuvre pour préserver son équilibre bactérien (manger sain, varié, équilibré). Et en cas de déséquilibre (mauvaise hygiène alimentaire, excès d’antibiotiques) vous pouvez le réensemencer par une alimentation riche en probiotiques (yaourt, choucroute crue…) ou, sur avis médical via une supplémentation.
Article de Magali Quent relevé dans Notre Temps du20 février 2019
Par Françoise Vignon
Davantage de génériques sur vos ordonnances
Publié le 23 avril 2019 à 14:54Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Moins chers, aussi performants que les médicaments « princeps » dont ils sont issus, les génériques sont remis en avant dans le projet de loi. A compter de 2019, votre médecin vous en prescrira encore plus, sauf justification médicale « étayée » (en cas d’intolérance ou d’allergie par exemple). Il n’apposera plus la mention « non substituable » devant le nom des médicaments de marque sur l’ordonnance, ce qui obligeait jusqu’ici le pharmacien à vous délivrer le médicament original. Vous pourrez, bien sûr, continuer à demander le médicament original mais un malus est instauré. A compter du 1er janvier 2020, votre remboursement sera aligné, non pas sur le prix du médicament princeps, mais sur celui de son équivalent générique… Il sera donc plus faible puisque le générique reste environ 40% moins cher que le médicament de marque.
Un cercle vertueux avec à la clé pour la Sécurité Sociale de substantielles économies.
Article relevé dans Notre de Temps de Septembre 2018
Par Françoise Vignon
La santé bucco-dentaire : les gestes à effectuer
Publié le 21 avril 2019 à 09:06Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
La santé bucco-dentaire est une composante essentielle de la santé générale, définie par un état de bien-être physique, moral et social. Cette définition s’applique pleinement à la santé bucco-dentaire qui contribue à l’amélioration de la qualité de vie.
La santé orale concerne la santé bucco-dentaire, les fonctions de l’oralité ainsi que la dimension psychique de l’oralité dans une approche pluridisciplinaire et pluriprofessionnelle. La santé bucco-dentaire s’intéresse aux dents, à leur position, aux tissus de soutien des dents (le parodonte), aux muqueuses de la cavité buccale, aux os des mâchoires (le maxillaire et la mandibule), aux articulations temporo-mandibulaires, etc…
Chez la personne en situation de handicap, de dépendance ou de vulnérabilité on peut observer des anomalies (dysmorphoses) dentaires et osseuses, un encombrement dentaire, une macroglossie (volume lingual important) rendant l’abord de la cavité orale délicat. Cette personne a tendance à développer plus facilement des pathologies dentaires (caries) et parodontales (maladie des gencives) qui peuvent être à l’origine de douleurs, d’infections, de perte prématurée des dents, et parfois du trouble du comportement.
Le maintien d’une bonne santé orale permet :
- La prévention de complications infectieuses ou chroniques parmi lesquelles nous pouvons citer les pneumopathies.
- La prévention de complications fonctionnelles de l’oralité : troubles de la mastication, de la déglutition, de la phonation et de la respiration.
- La prévention de la dénutrition liée à la perte des dents ou à des douleurs aggravées par la mastication.
- La prévention de douleurs aiguës ou chroniques, de gênes ou d’inconforts
- Le maintien d’une bonne estime de soi. Le respect de la dignité
- Le maintien de la relation sociale et familiale en améliorant le regard porté sur la personne en situation de handicap par l’entourage.
Le brossage est la seule manière d’éliminer la plaque dentaire et les débris alimentaires de manière efficace, d’éviter l’apparition de caries et de problèmes gingivaux, d’assurer une hygiène bucco-dentaire satisfaisante. Un rinçage, même avec un bain de bouche, ne nettoie pas les dents. C’est une alternative occasionnelle. Une vigilance encore plus importante doit être portée à l’hygiène bucco-dentaire quotidienne en cas de pathologies associées (cardiopathie, diabète, etc..).
Technique de soins :
Installer confortablement la personne sur une chaise ou dans son fauteuil roulant, face au lavabo. Prendre en compte les capacités et la coopération de la personne. Eviter de positionner la tête en hyper extension (la basculer vers l’arrière) pour réduire les risques de fausses routes avec la salive ou la mousse du dentifrice. Le brossage doit être doux et non-traumatisant. L’utilisation d’une brosse à dents souple, en effectuant des mouvements circulaires sans force exagérée, permet de nettoyer efficacement les dents et les gencives.
- Ne pas faire ouvrir trop grand la bouche de la personne car cela peut la fatiguer, il lui sera difficile de garder la bouche grande ouverte pendant 3 minutes. Marquer des temps de pause lors du brossage pour permettre à la personne de fermer la bouche
- En cas d’approche difficile du lavabo pour cracher, utiliser un haricot, une petite cuvette. Si la personne ne sait pas cracher, éliminer la mousse du dentifrice déposée sur les dents et les muqueuses avec une ou plusieurs compresses sèches ou brosse à dents rincée à l’eau.
- En cas de dépendance, l’aidant peut s’asseoir face à la personne ou rester debout pour assurer les gestes d’hygiène bucco-dentaire.
Fréquence :
Si possible le brossage est réalisé après chaque repas. C’est celui du soir le plus important, car pendant le sommeil, la quantité de salive diminue. Le pouvoir protecteur de la salive étant plus faible, les bactéries sont plus agressives. En cas de réflexe nauséeux, une rééducation par massages spécifiques conduite par un orthophoniste ou un kinésithérapeute formé aux troubles de l’oralité peut faire reculer ce réflexe, et faciliter le brossage.
Article relevé dans le Guide Hygiène Bucco-Dentaire et Handicap
Par Françoise Vignon
Aide au transfert sans se faire mal
Publié le 16 avril 2019 à 12:11Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Soulevez, porter, déplacer, transférer ou repositionner une personne dépendante sont des gestes quotidiens pour les proches aidants. Ces gestes de manutention (transfert du lit au fauteuil, du fauteuil roulant aux toilettes) vont solliciter votre dos, s’ils sont mal réalisés ils génèrent fatigue et mal de dos. Forcer trop, forcer mal, forcer sur la colonne vertébrale signifient que l’aidant n’a pas adopté les bonnes postures. Ces mouvements incorrects sont dangereux et peuvent créer des pathologies.
Le proche aidant doit adapter son niveau d’assistance en fonction des besoins et des capacités du proche. Si la personne est capable de réaliser seule un déplacement ou une manœuvre, alors il est recommandé de la laisser faire le plus possible d’actions par elle-même, à son rythme, même si cela demande plus de temps. Laisser faire c’est stimuler les capacités résiduelles, c’est respecter l’autonomie de la personne, tout en soulageant les efforts de l’aidant.
Pour ne pas vous faire mal :
- Garder les pieds écartés et fermement plantés au sol lorsque vous soulevez une personne dépendante
- Prenez toujours votre temps et ne chargez jamais le poids de la personne avant de vous sentir parfaitement à l’aise
- Votre dos doit rester bien droit pendant toutes ces manœuvres. Ce sont vos bras et vos jambes qui font le travail
- Evitez absolument les torsions qui sont la cause principale du mal de dos.
- Contractez les abdominaux : élément essentiel de la protection du dos, ils enlèvent jusqu’à 80% du poids qui s’exercent sur les vertèbres.
- Maintenez un contact étroit avec le corps de la personne et expliquez-lui ce qu’elle doit faire. Donner et répéter des consignes claires, verbales et gestuelles. La personne doit être rassurée par le contact visuel et le toucher
Pour ne pas lui faire mal :
- ¤ Lors de tous les mouvements, ne jamais tirer par les bras, vous pourriez fragiliser ses articulations.
- Demandez-lui tout au long de la manœuvre si elle se sent bien : les changements de position peuvent provoquer des vertiges. En particulier, chez les personnes âgées souffrant d’hypertension orthostatique qui occasionne une baisse de la tension artérielle lors du passage de la position couchée à la position debout
- Quand vous utilisez un fauteuil roulant, vérifiez que les freins soient actionnés pour éviter des accidents au moment où la personne s’appuie sur le fauteuil.
Article relevé dans Dimidom
Par Françoise Vignon
Une IRM ultrapuissante pour faire avancer la recherche à Rennes
Publié le 12 avril 2019 à 10:05Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
La plate-forme rennaise de recherche médicale Neurinfo vient de se doter d’une IRM ultrapuissante implantée au CHU de Rennes, depuis le mois de février 2018. Elle va aider à mieux comprendre le fonctionnement du cerveau, du cœur et d’autres organes.
Elle pèse près de 12 tonnes et a coûté la bagatelle de près de 2 millions d’euros. Un petit bijou de très haute technologie fabriqué par Siemens et capable de développer un champs magnétique de trois Teslas, contre 1,5 en moyenne pour une IRM classique.
Si cette IRM va servir à pratiquer des examens sur des patients, sa véritable vocation sera la recherche et plus précisément celle menée par la plate-forme Neurinfo créée en 2009. Cette plate-forme est un partenariat entre : « L’université de Rennes1, l’Institut national de recherche en informatique et en automatique (Inria) de Rennes, le CHU et le centre de lutte contre le cancer, Eugène Marquis » explique Christian Barillot, son directeur. « Elle est à l’imagerie médicale et à la neuroinformatique. » Cette discipline, relativement récente, mobilise des informaticiens et spécialistes du signal qui créent des systèmes et algorithmes permettant de rendre plus lisibles et interprétables les données, notamment dans le domaine des neurosciences. « Elle permet de regarder plus finement, de voir avec une meilleure résolution et de mesurer plus rapidement le fonctionnement d’un cerveau ou d’un cœur » précise Christian Barillot. Des caractéristiques que ne permet pas une IRM dans le domaine clinique classique.
« Par exemple, on peut arriver à mesurer les fibres qui vont connecter une région du cerveau à une autre. On peut caractériser de la microstructure cérébrale. Ce qui était très difficile voire impossible avant. » Des informations très précieuses pour les chercheurs avec toujours le même principe : Plus on comprend le fonctionnement ou les dysfonctionnements d’un organe, mieux on peut trouver des thérapies. « Ce nouvel appareil doit permettre d’améliorer le diagnostic des patients et de manière plus précoce. Il pourra aussi peut-être favoriser demain de nouvelles prises en charge thérapeutiques. » espère Véronique Anatole-Touzet, directrice du CHU.
L’étude clinique de la chélation du fer / L’Agence française de sécurité du médicament (ANSM) juge « pertinent d’autoriser l’usage du cannabis à visée thérapeutique »
Publié le 11 avril 2019 à 07:45Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Des nouvelles de l’étude clinique sur la chélation conservatrice du fer mené au CHU de Lille.
Le projet Fair Park II est un projet européen mené sur 3 ans de 2016 à 2019. Il regroupe 24 centres experts de la maladie de Parkinson, répartis dans 8 pays d’Europe. Il fait suite à une première étude concernant 40 patients. L’étude clinique actuelle concerne 338 patients au début de la maladie (diagnostic inférieur à 18 mois) ne bénéficiant d’aucun traitement. Au 5 décembre 2018, 267 patients ont suivi ou sont en train de suivre l’essai clinique qui dure 9 mois. Il reste donc 71 places. Il est possible d’entrer dans ce protocole jusqu’en juin 2019. Pour participer, il faut répondre à un premier questionnaire sur http://fairpark2.eu/patients. Le patient est ensuite redirigé vers le CHU le plus proche de son domicile. Les différents CHU sont les suivants : Lille, Paris, Clermont-Ferrand, Lyon, Toulouse, Marseille, Bordeaux. Après un entretien avec le neurologue une prise de sang et des examens indolores sont réalisés (IRM cérébral, scintigraphie au DATSCAN, échographie transcrânienne).
Le patient doit ensuite prendre la défériprone matin et soir selon une posologie en adéquation avec son poids. Une prise de sang hebdomadaire puis mensuelle a lieu pour surveiller la NFS (Numération Formule Sanguine) : en cas de chute des polynucléaires neutrophiles, le traitement est suspendu.
C’est le professeur Devos au CHU de Lille qui coordonne cette étude randomisée en double aveugle : ni le patient, ni le médecin ne savent, ni ne sauront si le médicament est la défériprone ou bien un placebo.
Le docteur Devos émet l’hypothèse que la substance noire contiendrait des concentrations élevées en fer. La défériprone qui est un traitement piégeur du fer pourrait diminuer l’excès de fer dans la substance noire, et ainsi limiter la mort neuronale et ralentir la progression des symptômes de la maladie de Parkinson. La molécule est suffisamment petite pour traverser la barrière hémato-encéphalique.
Si les résultats sont probants [et il y a de fortes chances qu’ils le soient puisque ceux du Fair PACK 1 l’étaient NDLR] une dernière étude Fair Park III sera faite au niveau mondial à partir de juin 2020. Cette fois, il sera possible que des personnes sous traitement y participent et il n’y aura plus de placebo. L’étude portera alors sur différents dosages de la défériprone.
C’est donc une étude clinique qui s’intéresse à une cause possible de la maladie.
Synthèse réalisée par Michel David qui participe à cette étude au CHU de Lille depuis novembre 2018.
L’Agence française de sécurité du médicament (ANSM) juge « pertinent d’autoriser l’usage du cannabis à visée thérapeutique »
Le recours au cannabis thérapeutique pourrait être pertinent dans certaines situations cliniques a récemment reconnu un comité d’experts de l’Agence française de sécurité du médicament. A Marseille, une étude sur ses effets dans la maladie de Parkinson va être menée par une équipe de scientifiques.
C’est une première. Car la France n’avait pas, jusqu’ici menée de recherches de ce type. Le centre d’étude Dhune et l’association France Parkinson vont financer une étude « visant à définir les effets du cannabis thérapeutique chez les patients atteints de la maladie de Parkinson. Des études expérimentales suggèrent que certains des composés du cannabis thérapeutique, notamment le Tétrahydrocannabinol et le cannabidiol auraient un potentiel effet neuroprotecteur ainsi qu’un effet sur les symptômes parkinsoniens » explique le site Silvereco.fr
Une étude d’abord menée sur des rats
L’étude qui sera menée ces prochains mois par une équipe de scientifiques à Marseille portera notamment sur les « effets de différentes proportions de cannabinoïdes sur les manifestations motrices et non motrices liées à la maladie » L’étude, menée par l’équipe de chercheurs composée de Jean Philippe Azulay, chef de service neurologie à la Timone, Olivier Blin, responsable de Dhune, et Christelle Baunez, directrice de recherche au CNRS, sera d’abord menée sur des rats. Elle devrait ensuite être étendue à l’homme, une fois les autorisations obtenues.
« Cela ne diffère pas des protocoles classiques, nous devons fournir des informations sur la faisabilité de l’étude, ainsi que sur la sécurité des personnes testées », a expliqué Alexandre Eusebio. S’ils sont concluants, les tests pourraient « ouvrir la voie » à la mise au point d’un nouveau traitement pour les patients parkinsoniens.
En France, la question du recours au cannabis thérapeutique dans certaines situations cliniques fait débat depuis de nombreuses années. Après l’avis favorable du comité d’experts à la mi-décembre 2018, l’Agence du médicament a décidé de mettre en place l’expérimentation du cannabis thérapeutique avant la fin de l’année 2019.
Article relevé dans Ouest-France et dans La Provence du 02/03/2019
Par F. Vignon et J. Graveleau
Le rôle des astrocytes : une piste de recherche
Publié le 10 avril 2019 à 08:44Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
Les chercheurs redoublent d’efforts pour comprendre les mécanismes moléculaires au cœur de cette maladie, et ainsi identifier de nouvelles cibles thérapeutiques potentielles. Récemment, ils ont mis en évidence le rôle méconnu de certaines cellules nerveuses, les astrocytes, dans la maladie.
https://www.frm.org/recherches-maladies-neurologiques/maladie-de-parkinson/maladie-de-parkinson-une-meilleure-comprehension-du-role-des-astrocytes-dans-la-pathologie
Un nouveau réseau cérébral relié à la douleur chronique dans la maladie de Parkinson par l’INSERM de Grenoble
Des chercheurs de l’Inserm et de l’Université Grenoble Alpes ont révélé un nouveau réseau cérébral qui relie la douleur ressentie dans la maladie de Parkinson à une région spécifique du cerveau.
Ces travaux, parus dans la revue eLife, révèlent qu’un sous-ensemble de neurones situé dans une partie du cerveau appelée noyau sous-thalamique serait une cible potentielle pour soulager la douleur dans la maladie de Parkinson, ainsi que dans d’autres maladies comme la démence, la sclérose latérale amyotrophique, la maladie de Huntington, et certaines formes de migraine.
Les personnes atteintes de la maladie de Parkinson font souvent état de douleurs inexpliquées telles que des sensations de brûlure, de coup de poignard, de démangeaisons ou de fourmillements, qui ne sont pas directement liées aux autres symptômes de la maladie. Le traitement par stimulation cérébrale profonde du noyau sous-thalamique peut aider à réduire les symptômes liés aux mouvements dans la maladie de Parkinson. Des études récentes ont cependant montré que ce traitement atténue également la douleur, mais sans pouvoir à ce jour mettre en lumière les mécanismes impliqués. C’est sur cette question que se sont penchés des chercheurs de l’Inserm et de l’Université Grenoble Alpes au sein de l’Unité 1216 Grenoble Institut des neurosciences.
« Dans cette étude, nous avons cherché à déterminer si le noyau sous-thalamique intervient dans la traduction d’un stimulus nuisible (par exemple une lésion) en douleur, et si cette transmission de l’information est altérée dans la maladie de Parkinson, » explique Arnaud Pautrat, doctorant à l’université Grenoble-Alpes et chercheur principal de l’étude.
L’équipe a commencé par utiliser l’électrophysiologie pour mesurer le déclenchement de signaux électriques dans les cellules nerveuses du noyau sous-thalamique de rats recevant un choc dans la patte postérieure. Les cellules nerveuses apparaissaient temporairement activées par cette stimulation. Les chercheurs ont également découvert que les neurones se divisaient en trois catégories de réponses par rapport à la vitesse de déclenchement de base : une hausse, une baisse ou un maintien de la vitesse.
L’équipe a ensuite cherché à savoir si ces réponses provoquaient une modification de la fonction cérébrale. Les rats au noyau sous-thalamique endommagé ont mis beaucoup plus de temps pour montrer des signes d’inconfort que les rats sains. Lorsqu’ils ont élargi leur étude au modèle du rat dans la maladie de Parkinson, les chercheurs ont découvert que les cellules nerveuses du noyau sous-thalamique présentaient des vitesses de déclenchement plus élevées et que les réponses à la douleur étaient plus importantes et plus longues que chez les animaux sains. L’ensemble de ces résultats suggère que la douleur associée à la maladie de Parkinson serait due à un dysfonctionnement des voies du traitement de la douleur dans le noyau sous-thalamique.
Pour comprendre d’où proviennent les signaux de la douleur envoyés au noyau sous-thalamique, l’équipe s’est intéressée à deux structures cérébrales connues pour leur importance dans la transmission de signaux de lésions depuis la moelle épinière : le colliculus supérieur et le noyau parabrachial. En bloquant leur activité, les chercheurs ont observé que ces deux structures jouaient un rôle déterminant dans la transmission des informations de la douleur au noyau sous-thalamique, et qu’une voie de communication directe existe entre le noyau parabrachial et le noyau sous-thalamique. Dans le cas de la maladie de Parkinson, cette voie de communication pourrait donc intervenir dans les effets bénéfiques sur la douleur de la stimulation cérébrale. Ces nouvelles données pourraient aider à orienter la stimulation sur des parties spécifiques du cerveau pour augmenter l’efficacité de ses effets antalgiques.
« Les résultats que nous avons obtenus mettent en évidence que le noyau sous-thalamique est relié de manière fonctionnelle à un réseau de traitement de la douleur et que ces réponses sont affectées dans le syndrome parkinsonien, » conclut Véronique Coizet, chercheuse Inserm et directrice de l’étude. « Il faut maintenant effectuer d’autres expériences pour caractériser précisément les effets, qui ont été observés avec nos modèles expérimentaux, de la stimulation cérébrale profonde sur cette région du cerveau, afin de trouver les moyens d’optimiser cette stimulation en tant que traitement de la douleur induite par la maladie de Parkinson et par d’autres maladies neurologiques. »
https://presse.inserm.fr/un-nouveau-reseau-cerebral-relie-a-la-douleur-chronique-dans-la-maladie-de-parkinson/32316 /
L’optimisation du traitement dopaminergique aux stades les plus sévères de la maladie de Parkinson
L’optimisation du traitement dopaminergique aux stades les plus sévères de la maladie de Parkinson peut réduire les symptômes non moteurs et améliorer la qualité de vie, rapportent ces scientifiques de l’université de Lund dans le Journal of Parkinson’s Disease. Des symptômes non moteurs fréquents au stade avancé, car leur fréquence et leur sévérité augmentent avec la progression de la maladie.
Si la maladie de Parkinson est généralement considérée comme une maladie qui affecte le mouvement, elle implique en effet et aussi un grand nombre de symptômes non moteurs, qui peuvent aussi impacter la qualité de vie. Ces symptômes non moteurs incluent la déficience cognitive, les troubles de l’humeur et la dépression, l’apathie, la somnolence diurne et autres troubles du sommeil, la fatigue et des dysfonctionnements autonomes tels que l’urgenturie, plus généralement l’incontinence et la dysfonction érectile. La fréquence et la gravité de la plupart de ces symptômes augmentent avec la progression de la maladie. De précédentes recherches ont montré que la fréquence et la sévérité des symptômes non moteurs sont les facteurs prédictifs les plus importants de la qualité de vie chez les patients atteints au stade avancé.
Parkinson avancé, un groupe de patients oubliés ? Au cours des 4 à 5 dernières années de la maladie, les patients parkinsoniens « constituent un groupe de patients oubliés », explique l’auteur principal le Dr Per Odin, professeur au département de neurologie de l’université de Lund (Suède). « Il y a des raisons de croire que ces patients à stade avancé sont insuffisamment traités. L’effet du traitement dopaminergique peut ne pas être aussi évident au stade avancé qu’au stade précoce ». Les chercheurs ont donc regardé particulièrement la question du traitement pharmacologique optimal pour ces patients à stade avancé et notamment évalué l’effet du traitement dopaminergique sur les symptômes non moteurs chez 30 patients. L’effet dopaminergique sur la symptomatologie non motrice a été évalué à l’aide de différents tests.
Cette analyse révèle que :
- les symptômes non moteurs sont en effet plus fréquents chez ces patients,
qu’un grand nombre de ces symptômes sont présents chez plus de 80% des patients. - les scores les plus élevés sont observés dans les domaines de l’humeur, de l’apathie et de l’incontinence urinaire.
Les chercheurs soulignent ici l’importance d’optimiser le traitement par la L‑dopa au stade avancé de la maladie pour donner aux patients la meilleure qualité de vie possible : « Nous appelons nos collègues à faire attention à ce que le traitement soit bien optimisé tout au long de la progression de la maladie et à ses stades les plus sévères. Le fait de savoir qu’un traitement dopaminergique suffisant peut avoir des effets importants sur les symptômes moteurs et non moteurs chez les patients parkinsoniens, peut aider les médecins traitants à améliorer la qualité de vie de leurs patients, même au stade avancé ».
Lu sur Santé log Parkinson
Par Martine Delmond
La dopamine est un neurotransmetteur impliqué dans plusieurs traits de comportement et personnalité.
Publié le 08 avril 2019 à 08:30Article paru dans LE PARKINSONIEN INDÉPENDANT n°76
La dopamine est un neurotransmetteur (messager chimique du cerveau) synthétisé par certaines cellules nerveuses à partir de la tyrosine, un acide aminé (composant des protéines de l’alimentation). Comment on mesure la dopamine ? Pour évaluer les taux de dopamine on dose dans le sang, les urines ou le liquide cérébro-spinal la quantité de HVA (acide homovanillique) et DOPAC, des produits de dégradation de la dopamine.
Comment fonctionne le système dopaminergique ?
Les neurones dopaminergiques (plusieurs millions) utilisent la dopamine pour transmettre une information chimique. 80% de la dopamine libérée est récupérée par la cellule émettrice, pour être réutilisée. Le reste est transformé en un produit de dégradation – ou catabolite – l’acide homovanillique (HVA). Pour évaluer votre taux de dopamine on dose à la fois la dopamine et son catabolite.
Les corps cellulaires dopaminergiques sont situés dans le mésencéphale (partie médiane du cerveau), d’où ils irradient jusqu’au cortex frontal et l’amygdale d’une part, le striatum d’autre part (voir schéma).
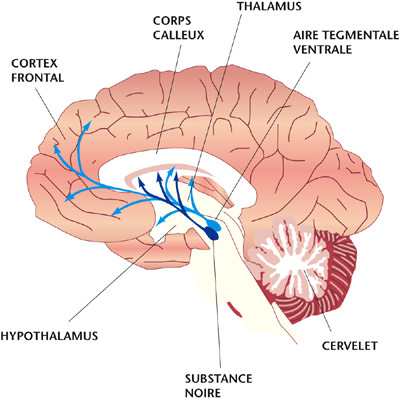
À quoi sert la dopamine ?
Même s’il est un peu caricatural d’attribuer un trait de comportement ou de personnalité à un neurotransmetteur, on considère que les réseaux dopaminergiques sont étroitement associés aux comportements d’exploration, à la vigilance, la recherche du plaisir et l’évitement actif de la punition (fuite ou combat).
Chez l’animal, les lésions de l’aire tegmentale ventrale se traduisent par un désintérêt pour les stimuli de l’environnement et par une diminution du comportement exploratoire. En revanche, lorsqu’on place des électrodes aux sites dopaminergiques et qu’on permet à l’animal de s’autostimuler par déclenchement de chocs électriques, le plaisir et l’excitation sont tels que le cobaye peut en oublier de s’alimenter.
Chez l’homme, la baisse d’activité des neurones dopaminergiques de l’axe substance noire — striatum entraîne une diminution du mouvement spontané, une rigidité musculaire et des tremblements. C’est la maladie de Parkinson.
Des taux de HVA anormalement bas ont également été retrouvés chez des patients toxicomanes souffrant de troubles du déficit de l’attention avec hyperactivité (TDAH) et ayant été négligés durant leur enfance. Ces résultats suggèrent que la négligence des parents pendant l’enfance pourrait avoir un effet sur la fonction dopaminergique à l’âge adulte et contribuer à l’apparition de l’hyperactivité et à une plus grande sensibilité à l’usage de drogues.
On trouve des taux de HVA très bas (signe d’une hypoactivité dopaminergique) dans les dépressions de type mélancolique, caractérisées par une diminution de l’activité motrice et de l’initiative. A l’inverse les produits, les activités qui procurent du plaisir, comme l’héroïne, la cocaïne, le sexe, activent certains systèmes dopaminergiques. Ainsi, les médicaments qui augmentent la dopamine, comme la L‑Dopa ou les amphétamines, augmentent aussi l’agressivité, l’activité sexuelle, et l’initiative.
Les effets de la dopamine sont contrebalancés par ceux de la sérotonine un autre neurotransmetteur important.
En pratique
En cas de dépression de type mélancolique, de baisse d’intérêt pour les activités qui en procuraient, de baisse de la vigilance et de l’attention, toujours consulter un professionnel de santé. Parallèlement, il peut être utile de consommer des aliments riches en tyrosine. Il existe aussi des compléments de L‑tyrosine.
À quand un appareil pouvant détecter, analyser comme pour les diabétiques le taux de dopamine dans le corps d’un malade de Parkinson ? il serait souhaitable qu’une start-up Française s’y intéresse, nous apercevons en tant qu’association que les médecins et neurologues n’ont pas cet outil ; cet appareil pourrait aider dans la pharmacopée d’un malade de Parkinson.
Les niveaux de dopamine faibles peuvent causer la dépression, une perte de satisfaction, des envies, les compulsions, une faible libido et une incapacité à se concentrer. Tyrosine est un autre acide aminé important (un bloc de base des protéines) dans les produits laitiers, les viandes, les volailles et les noix. Il encourage votre cerveau pour libérer de la dopamine et la noradrénaline. Ces neurotransmetteurs agissent comme substances stimulantes pour le cerveau et peuvent vous aider à vous requinquer en vous faisant sentir plus alerte et aiguiser votre pensée.
La dopamine est le précurseur de l’adrénaline et de la noradrénaline, deux hormones qui sont également considérés comme des neurotransmetteurs agissant comme régulateurs de l’humeur, du métabolisme et comme stimulants du système nerveux et de la circulation sanguine.
Une déficience ou un excès en dopamine est relié à des pathologies comme la maladie de Parkinson ou des phénomènes de dépendance aux drogues. « Elle est reliée au sentiment de satisfaction ; connue pour avoir une fonction importante dans la prise alimentaire, c’est un neurotransmetteur qui aide à contrôler les centres de récompense et de plaisance dans notre cerveau. La dopamine contribue également à normaliser le mouvement et à gérer les réactions émotives, et nous permet de percevoir des récompenses et de prendre des mesures pour se déplacer vers eux. »
Il est intéressant de noter que : la dopamine est un neurotransmetteur puissant dans le cerveau. En fait, c’est le produit chimique directement responsable de la motivation et de la concentration du cerveau. Qui ne souhaite pas être plus motivé et concentré ? Ce qu’il y a de vraiment excitant avec la dopamine c’est qu’elle peut être augmentée ! Oui, vous pouvez efficacement améliorer votre motivation, votre concentration et votre humeur en prenant des mesures naturelles permettant d’augmenter les niveaux de cette substance dans le cerveau !
Voici 10 façons d’augmenter les niveaux de dopamine et de stimuler la productivité
1. Faites de l’exercice
On ne peut nous le répéter assez souvent. À maintes reprises on nous rappelle l’importance et les avantages de l’exercice physique, et c’est un détail qui doit de nouveau être ajouté à cette liste. Car non seulement l’exercice nous aide à soulager le stress, atteindre une meilleure santé physique, nous rend plus productif ; mais il stimule notamment cette substance. Plus précisément, l’exercice augmente la production de neurotransmetteurs – la sérotonine et les endorphines, en plus de la dopamine (qui augmente notre sensation de bien-être) reçoit un coup de pouce. Notez que : l’exercice ne doit pas être ardu. Vous promener ou monter des escaliers permettra d’atteindre une montée de ce neurotransmetteur.
2. La purification des toxines
Bien que notre corps soit miraculeux, nous accumulons des toxines et des bactéries qui sont mauvaises pour nous. Les endotoxines peuvent affaiblir notre système immunitaire, et limitent également la production de dopamine. Voici quelques conseils pour aider à nettoyer l’intestin des endotoxines : manger de la nourriture fermentée, dormir suffisamment, et résister aux aliments gras ou sucrés. Peut-être que la meilleure façon de débarrasser notre corps de ces toxines désagréables est de faire une purification des toxines. Jetez donc un coup d’œil à ce processus et décidez si oui ou non ceci est pour vous.
3. Créez quelque chose
Pour nous les écrivains, peintres, sculpteurs, poètes, chanteurs, danseurs et autres artistes, nous pouvons nous identifier à cela. Lorsque nous sommes en phase créative, nous pouvons devenir hyper-engagés. Par conséquent, nous pouvons entrer dans un état particulier de réceptivité. En résumé, la dopamine est la substance chimique libérée par le cerveau lorsqu’un comportement nous permet d’atteindre cet état. Voici la leçon que vous devez retenir : adonnez-vous à un passe-temps ou une activité dans laquelle vous créez quelque chose qui a des effets bénéfiques tangibles. Essayez quelque chose comme les arts, l’artisanat, la réparation automobile, le dessin, la photographie, ou autre chose qui semble intéressant.
4. Ne développez pas une dépendance
Beaucoup de gens développent une dépendance à quelque chose parce que cela leur apporte une sorte de satisfaction instantanée – drogue, alcool, relations intimes, pornographie, shopping, et autres comportements de dépendance auraient l’effet contraire sur les niveaux de dopamine à long terme. Fondamentalement, lorsque nous sommes trop dépendants de quelque chose, « le circuit de récompense » de notre cerveau devient surexcité et nous implore une « solution rapide ». Ce n’est pas une solution viable pour la production de dopamine, qui peut et doit être accomplie naturellement.
5. Augmentez les niveaux de tyrosine.
Cet autre acide aminé est lui un précurseur de l’adrénaline, la noradrénaline, la dopamine et la DOPA. Des neurotransmetteurs et hormones ayant un rôle important au niveau du système nerveux, de l’humeur, de la stimulation du métabolisme, de la régulation de l’appétit et du bon fonctionnement de la glande thyroïde. Une déficience en tyrosine peut être associée à des symptômes tels qu’une basse pression sanguine et un abaissement de la température corporelle. Parmi les substances chimiques qui la produisent, aucune n’est plus importante que la tyrosine. En fait, la tyrosine est considérée comme le bloc de construction pour le neurotransmetteur qui déclenche la dopamine. Par conséquent, il est important que vous consommiez une quantité suffisante de cette protéine. Il y a une grande liste d’aliments qui augmentent la tyrosine : Les amandes, l’avocat, les bananes, le bœuf, le poulet, le chocolat, le café, les œufs, le thé vert, le lait (bio), la pastèque, le yaourt. Il y a un tas de bonnes choses ci-dessus, donc il ne devrait pas être difficile de trouver quelque chose qui va bien servir vos niveaux de dopamine.
6. Établissez une série de victoires.
Comme avec la création d’une liste de tâches, établir une série de victoires est une excellente façon d’augmenter les taux de dopamine. Cela est un rappel visuel du nombre de jours consécutifs où vous avez réalisé quelque chose. Procurez-vous un calendrier précisément dans ce but : écrivez ce qui vous passionne, votre but, et les jours et les mois où vous avez prévu de les faire. Par exemple, si vous travaillez lundi, mercredi et vendredi, marquez ces jours dans le calendrier pour le mois. Lorsque vous effectuez une séance d’entraînement, marquez-le sur le calendrier. En établissant une série de victoires, vous maintenez l’élan de la dopamine.
7. Une liste de petites tâches.
La production de cette substance augmente lorsque nous sommes organisés et que nous accomplissons des tâches – peu importe si la tâche est petite ou grande. Alors, ne laissez pas à votre cerveau se soucier des choses qui doivent être faites. Au lieu de cela, faites une liste de ces tâches puis cochez les points au fur et à mesure. Il a été démontré qu’il est plus satisfaisant pour les niveaux de dopamine dans le cerveau d’élaborer une liste de tâches à accomplir de façon à les énumérer et pour s’en rappeler.
8. Méditez.
Comme avec l’exercice, nous découvrons de plus en plus les avantages de la méditation. De nouveau, nous l’ajoutons à la liste des pratiques. Comme nous en avons parlé, le cerveau humain est sensible à une variété de dépendances. Une autre dépendance que nous avons est la sur-analyse. Au point que certains bouddhistes ont une expression pour cette addiction : « esprit de singe ».
La sur-analyse est non seulement une habitude distrayante, mais aussi une contrainte réelle qui nous laisse dans un état troublant, tout en ayant un effet négatif sur notre développement spirituel. Cependant, les scientifiques sont enfin en train de rattraper ce que les bouddhistes savent depuis des milliers d’années : la méditation et la pleine conscience sont essentielles pour un esprit sain. Il a aussi été démontré que la prière et l’autoréflexion augmentaient les niveaux de dopamine.
9. Consommez des suppléments.
Bien qu’il existe quelques bonnes façons d’augmenter les niveaux de ce neurotransmetteur, parfois nous manquons d’équilibre en matière de gestion. Heureusement, il y a des suppléments naturels sur le marché qui s’avèrent aussi augmenter les niveaux de dopamine. En voici quelques-uns :
- Acétyle-L-tyrosine : Un bloc de construction d’un produit chimique appelé acide aminé : de ce neurotransmetteur. Une bonne dose facilite sa production dans le cerveau.
- Curcumine : Un ingrédient actif de l’épice « curcuma » entrant dans la composition du curry et du curcuma.
- Soupçonné d’augmenter ses niveaux et de la faire circuler dans le cerveau plus facilement. L‑théine : augmente plusieurs neurotransmetteurs dans le cerveau, y compris la dopamine. Le thé vert en est une formidable source.
10. Ecoutez de la musique
Vous êtes-vous déjà demandé pourquoi la musique vous rend heureux ? Nous pouvons avoir le cafard, mais une fois que nous jouons notre morceau préféré, nous retrouvons le sourire … et nous nous sentons plus sûrs de nous aussi ! La raison de ceci est qu’écouter de la musique augmente les niveaux de dopamine. En fait, les scientifiques disent que cela a le même effet que de manger ses aliments préférés ou regarder son émission de T.V. favorite. Donc lorsque vous vous sentez déprimé, écoutez certains de vos morceaux préférés et laissez-vous porter par la musique !
Vu sur le site : https://www.lanutrition.fr/outils/a‑quoi-sert-la-dopamine-
Par Dominique Bonne
56 – ASSOCIATION de PARKINSONIENS du MORBIHAN
Publié le 07 février 2019 à 15:34Article paru dans LE PARKINSONIEN INDÉPENDANT n°75
Pour marquer la rentrée, nous nous retrouvons le 22 septembre au parc aquanature « Le Stérou ». Après un repas copieux, profitant d’un rayon de soleil, nous nous répartissons dans les voiturettes électriques pour un parcours ludique à travers le parc où nous avons pu admirer et photographier cerfs, biches, daims pendant plus d’une heure. Les « pilotes » très attentifs dans leur conduite lors des descentes accidentées, nous ont ramené à bon port. Après la pose et les rafraîchissements, nous reprenons la route, enchantés de cette belle journée.
Nicole Lecouvey – Françoise Vignon

Le 20 septembre à Missiriac en partenariat avec l’Espace Autonomie Seniors de Guer, la CNSA, la CAP Retraite Bretagne, le Pr Derkinderen, nous organisions une conférence « Parkinson, vous connaissez ? » Ce rendez-vous pour informer et sensibiliser tout un chacun, particuliers et professionnels sur cette maladie, a réuni 250 personnes. Deux comédiens ont mis en situation les effets, les difficultés, les réactions occasionnés par la M.P.
Après la présentation de la maladie, des symptômes, des traitements, le Pr Derkinderen nous informa qu’un médicament agissant sur le diabète pourrait avoir un effet sur les cellules gliales et ralentir l’avancée de la maladie. D’autres études sont en cours dans les laboratoires du CHU de Nantes. Un temps d’échange entre le Pr Derkinderen et le public a permis à ce dernier de répondre à des questions plus spécifiques et personnelles.
Avant de clôturer cette rencontre, des adhérents de l’ADPM ont illustré par des témoignages leur quotidien face à la maladie. Pour faire suite à cette réunion d’information, l’EAS de Guer met en place pendant cinq semaines (du 05/11 au 06/12) à l’attention des aidants, plusieurs ateliers animés par des professionnels de la santé et notre association. Ces réunions ont pour objectif de mieux informer l’accompagnant sur la maladie et son évolution, ses droits, ses limites en tant qu’aidant, d’échanger avec les professionnels, d’apporter des conseils en cas de situation problématique, d’éviter l’isolement en rencontrant d’autres personnes confrontées aux mêmes difficultés.
Du 30 septembre au 06 octobre nous assistions à l’A.G. CECAP. Cette année la Loire Atlantique nous accueillait à Piriac. Merci à Annick et à son équipe de nous avoir organisé une agréable semaine de vacances, par le choix des intervenants, des excursions, des soirées très animées. Convivialité et bonne humeur sont toujours au programme!!!
Membre depuis 18 ans, vice-Président de l’ADPM pendant une dizaine d’années, notre ami Collin nous a quitté début octobre laissant un grand vide auprès de tous ceux et celles qui l’appréciaient pour sa gentillesse, son engagement, sa ténacité dans son combat contre la maladie
Le 15 Octobre nous assistions à une conférence pour les aidants : « Prendre soin de soi pour prendre soin de l’autre » proposée par le CCAS de Vannes, CAP Retraite Bretagne, Brain Up. Huit millions d’aidants prennent en charge un proche pendant en moyenne, 16 ans. Ce sont majoritairement des femmes. Au début le plaisir d’aider, d’être présent, avec parfois un sentiment d’obligation se manifeste, puis au fur et à mesure des années les tâches, les responsabilités, les charges deviennent plus lourdes. Face aux premières difficultés, à l’isolement familial, à l’absence de reconnaissance, l’aidant est dépassé, ressent un manque de temps libre pour lui, la fatigue, la solitude. Il ne faut pas hésiter à se faire aider.
Le 18 novembre en l’Eglise Sainte-Thérèse de Kervado à Lorient, une centaine de personnes appréciaient le concert gospel (dédié à la recherche) du groupe AIR ‘nb Gospel dirigé par le chef de chœur Xavier Dival. Les vingt titres proposés et repris par un public connaisseur, mirent une chaude ambiance pendant deux heures. L’ADPM pour clore la soirée et remercier l’assemblée a chanté avec enthousiasme « Bats-toi » soutenue par les applaudissements du public.
A noter : la Galette des Rois le jeudi 17 janvier et l’AG le 19 mars
Souhaits chaleureux pour la saison des fêtes – Bonne Année 2019
50 – ASSOCIATION de PARKINSONIENS de La MANCHE
Publié le 06 février 2019 à 10:22Article paru dans LE PARKINSONIEN INDÉPENDANT n°75
Du 30 septembre au 6 octobre 2018 nous nous sommes retrouvés à Piriac sur mer en Loire Atlantique avec l’equipe ADPLA d’Annick et Philippe où nous avons passé une agréable semaine avec toutes les autres personnes des autres départements avec lesquelles nous avons toujours une certaine joie et émotion de se retrouver. MERCI A TOUS
En 2019 c’est l’équipe de la MANCHE qui vous accueillera avec un programe qui nous espérons va vous convenir et vous plaire à Blainville sur mer au village du Sénéquet sur la côte ouest du Cotentin à 450 métres de la mer dans un parc de 13 hectares. Si vous avez besoin de renseignements complémentaires n’hésitez pas à appeler (visite du mont accessible pour tous fauteuils roulants et autres).
A noter, l’Assemblée Générale de CECAP se tiendra au deuxième trimestre 2019 dans un autre lieu et ne viendra pas couper le déroulement des vacances.
Quand à nous ; nous nous sommes rencontrés le 25 octobre à Saint-Hilaire du Harcouët pour une journée de convivialité et d’informations ou nous avons eu le matin la participation d’une naturopathe. Puis le midi au restaurant nous étions une vingtaine de personnes et après le repas nous avons eu une discussion à bâtons rompus sur plusieurs théme.
L’assemblée générale en 2019 aura lieu le 28 mars 2019 à Coutances détails en temps utiles.
Si vous avez des idées pour les prochaines rencontres dites le nous.
Nous vous souhaitons de joyeuses fêtes et tous nos meilleurs voeux pour 2019 et surtout profitez des bonnes choses qui sont à votre portée et portez vous le mieux possible en attendant notre prochain rendez-vous.
Le bureau Brigitte Leroux
44 – ASSOCIATION de PARKINSONIENS de LOIRE ATLANTIQUE
Publié le 31 janvier 2019 à 15:11Article paru dans LE PARKINSONIEN INDÉPENDANT n°75
« Il faut réduire notre voilure » … Tel a été le leitmotiv qui a animé notre CA élargi du 18 mai dernier. Alors, commençons par notre journal départemental!!!! Il ne comportera, en cette fin d’année, qu’un « recto/verso » accompagné de feuilles volantes qu’il faudra remplir et nous retourner. Ceci nous permettra de pérenniser nos traditionnelles activités.
Les informations médicales sont largement transmises par bon nombre de médias sans oublier notre Parkinsonien Indépendant fort apprécié de tous ses lecteurs. Nous utiliserons désormais notre énergie à privilégier les moments de rencontres et de convivialités.
Les échanges entre malades et aidants répondent à une demande et surement à des besoins. Ils permettent de rester à l’écoute de soi, de ses désirs, de ses angoisses, de les partager et de mieux se comprendre et s’analyser. Souvent, ils permettent d’éloigner une culpabilité latente qui consiste à croire intimement que nous avons « mal fait » ou que nous avons « fait du mal ». Elle peut être profonde, destructrice et même empêcher de connaître le bonheur, la détente ou le plaisir.
Cette année, c’est le 44 qui a organisé une semaine de vacances à Piriac. Quel boulot !!!! Mais aussi quel plaisir nous avons ressenti, malades et aidants, en constatant qu’on pouvait aussi vivre, ne serait-ce que le temps d’une semaine, parmi les rires, les chants, la musique, les promenades, les découvertes, l’humour, la bonne humeur générale. Nous avons réussi à braver le carcan de la maladie.
Un bémol : Les inscrits de la Loire Atlantique n’ont pas été nombreux. On peut le regretter. Nous nous sommes soudainement retrouvés en LOIRE INFÉRIEURE ! un peu d’humour!!! Pour cette nouvelle année, nous avons pensé à des visites, à une journée à bord de la « péniche verte » sur le canal de Nantes à Brest ainsi qu’à des parties de pétanques, des après-midi « jeux de société », un récital de chorale, des pique-niques. Aucune date n’est encore fixée…. Nous attendons suggestions et coordinations.
Bonnes fêtes de fin d’année à toutes et à tous et au plaisir de vous revoir nombreux en Octobre prochain en haut du Mont Saint Michel. Cordiales pensées.
Annick Lebrun présidente
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.
