Bilan des deux boursières soutenues par CECAP (2/2)
Publié le 02 janvier 2014 à 09:56Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Bilan de Julie Meffre : Rôle du Noyau Subthalamique dans la Prise de Décision
A — PROJET DE RECHERCHE
1. Contexte de l’étude
Alors que la maladie de Parkinson a été longtemps abordée sur la base de ses symptômes moteurs, les troubles non moteurs qui lui sont associés font, depuis quelques années seulement, l’objet de recherches plus approfondies. La stimulation à haute fréquence (SHF) du noyau subthalamique (NST), utilisée avec succès pour traiter les troubles moteurs, peut cependant être à l’origine d’effets secondaires cognitifs comme un comportement impulsif ou risqué (tendance au jeu pathologique) chez certains patients. Il a été mis en évidence que la SHF altère la capacité à « freiner » la prise de décision face à une situation conflictuelle, conduisant les patients à prendre une décision hâtive et impulsive (Frank et al. 2007). Parmi les ganglions de la base, le NST semble être impliqué dans le contrôle de l’impulsivité/inhibition comportementale (Frank 2006 ; Eagle and Baunez 2010). La voie hyperdirecte, reliant les aires corticales frontales au NST pourrait être à l’origine de la régulation des processus décisionnels. Le NST semble agir en élevant le seuil de décision dans le cas d’une situation conflictuelle ou ambiguë, conduisant ainsi à différer la prise de décision, jusqu’à ce que suffisamment d’indices aient été accumulés.
2. But de l’étude
Afin de pouvoir améliorer l’anticipation d’éventuels effets secondaires de la stimulation à haute fréquence du NST sur la prise de décision chez les patients parkinsoniens, il est indispensable de bien comprendre le rôle de cette structure dans les processus décisionnels. L’objectif de notre travail de recherche, soutenu par la CECAP, a été de déterminer chez le rat
- comment le NST contribue à la prise de décision grâce à une approche comportementale réalisée chez des rats intacts versus des rats ayant subit une lésion du NST (mimant l’effet de la SHF du NST utilisée chez le patient parkinsonien)
- quelle est l’influence du système dopaminergique dans ce processus, et
- le potentiel thérapeutique d’un traitement visant le système sérotoninergique, système impliqué dans l’inhibition comportementale.
3. Procédures expérimentales utilisées
Animaux : 10 rats mâles Long Evans, maintenus dans un cycle 12h jour/nuit, ont été utilisés pour ces expériences. Ils ont été soumis à une restriction alimentaire, avec un accès à 85% de leur ration quotidienne. L’eau était accessible ad libitum.
Expérience : Mesure de la prise de décision impliquant l’évaluation d’un risque (en terme de probabilité de gain)
Les animaux sont placés dans une boîte opérante comportant trois leviers. Au démarrage de l’essai, seul le levier central est sorti, et les rats ont été entraînés à maintenir leur patte sur le levier central pendant une durée fixe de 1 seconde. 400 ms après le début de l’appui et pendant 600 ms, une combinaison de deux lumières s’allume au-dessus des leviers et indique quelle sera la probabilité d’obtenir 0.1 ml de sucrose 32% en cas de choix du levier correspondant à la récompense en grande quantité mais incertaine. Au bout de 600 ms, un signal sonore retentit, indiquant la possibilité d’aller appuyer sur le levier de gauche ou de droite, au choix, afin d’obtenir une récompense (0.05 ml de sucrose 32 % toujours délivré ou 0.1 ml sucrose 32 % délivré avec une probabilité variable et indicée, respectivement).
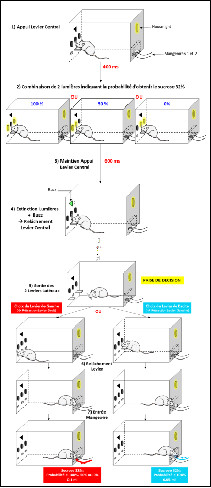
Trois combinaisons de deux lumières sont possibles, aléatoirement. Il existe trois spots lumineux situés au-dessus des leviers :
- Si la lumière de gauche et la lumière de droite s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 100 %.
- Si la lumière de gauche et la lumière centrale s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 50 %.
- Si la lumière de droite et la lumière centrale s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 0 %.
A la fin de la seconde d’appui, le levier central se rétracte et les deux leviers latéraux sortent.
- Si l’animal choisit le levier de droite, il appuie puis peut relâcher immédiatement le levier et une dose de 0.05 ml de sucrose 32 % est délivrée dans la mangeoire dans 100 % des cas.
- Si l’animal choisit le levier de gauche, le résultat de cette action sera incertain, en fonction de la probabilité d’obtenir 0.1 ml de sucrose 32%, indiquée précédemment par la combinaison de lumière.
La condition 100% et la condition 0% permettent de vérifier la bonne compréhension de la tâche par le rat. La condition 50% permet d’évaluer le comportement à tendance risquée ou non de l’animal. Ainsi, si dans la condition où la probabilité d’obtenir la grande récompense est de 50%, le rat choisi préférentiellement le levier associé à cette grande récompense, il sera considéré comme un individu au comportement risqué et joueur.
La moitié des animaux est conditionnée avec cette règle. Pour l’autre moitié, la petite récompense est délivrée lorsque l’animal choisit le levier droit.
Chirurgie : Lésion du NST
Lorsque les animaux ont atteint un niveau de performance stable durant au moins 5 sessions consécutives, ils ont été soumis au protocole chirurgical suivant :
Tous les animaux ont été anesthésiés avec de la kétamine (50 mg/kg, i.m.) et de la médétomidine (0.26 mg/kg, i.m.) et positionnés dans un appareil de stéréotaxie.
Les rats reçoivent une injection bilatérale d’acide iboténique (9.4 µg/µl (53 mM); rats avec lésion du NST) ou de solution contrôle (tampon phosphate, 0.1 M ; rats intacts) aux coordonnées suivantes : antéropostérieur, 3.8 mm (depuis le bregma); latéral, 2.4 mm ; dorsoventral, 8.35 mm (depuis le crâne). Le volume d’injection était de 0.5 microlitres par côté injecté pendant 3 minutes avec une seringue Hamilton fixée sur une micropompe. A la fin de l’injection, les injecteurs ont été laissés en place pendant 3 min pour permettre la diffusion de l’acide iboténique.
Les animaux ont récupéré des suites de l’opération pendant une semaine avant d’être à nouveau soumis au test (dans la même tâche que celle précédent la chirurgie)
B — RÉSULTATS PRÉLIMINAIRES
près apprentissage de la tâche, les animaux ont été soumis au test de prise de décision, et le pourcentage de prise de décision risquée (évaluée par le nombre d’appui sur le levier associé à la grande récompense dans la condition où la probabilité de l’obtenir est de 50%) a été mesuré. Nous avons ainsi mesuré le pourcentage de prise de décision risquée de base chez le rat, avant lésion du NST. Nous avons pu vérifier que les performances moyennes des rats avant l’opération ne présentaient pas de différences significatives, tous les individus choisissant de manière équivalente la petite récompense certaine et la grande récompense risquée.
Les animaux ont ensuite été soumis au protocole chirurgical. Après une période de récupération, ils ont été à nouveau soumis au même test que celui précédent la chirurgie. Après lésion du NST, on observe une modification profonde du comportement des rats, qui choisissent alors préférentiellement la condition risquée (dans 80% des cas environ). Une altération du NST conduit donc à une altération de la prise de décision, favorisant un comportement impulsif et risqué. Ces résultats semblent donc indiquer que les effets secondaires cognitifs de type impulsivité et développement du jeu pathologique chez les patients traités par la SHF du NST pourraient résulter de l’inactivation du NST.
Afin d’évaluer l’influence du système dopaminergique, cible des traitements médicamenteux dans la maladie de Parkinson, dans ce processus, nous avons procédé à une injection intrapéritonéale d’un inhibiteur de recapture de dopamine, 20 minutes avant le début du test. De façon très intéressante, nous avons pu observer que ce traitement conduit, chez les rats intacts, à une très forte augmentation du nombre de prise de décision risquée, celui-ci passant de 40% à 80% environ après traitement pharmacologique aigue avec un inhibiteur de
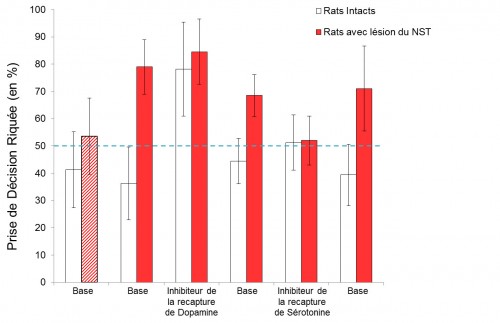
recapture de dopamine. Les rats intacts soumis à ce traitement dopaminergique présentent donc un comportement risqué similaire à celui des rats ayant subit une lésion totale du NST. Il semblerait donc que le système dopaminergique et le noyau subthalamique soient impliqués dans ce processus décisionnel.
Suite à ce traitement, les animaux ont été à nouveau soumis au test avec après avoir subit une injection de solution contrôle (sérum physiologique), afin de vérifier un retour à la normale (niveau de base) de leur performance comportementale.
Il a été mis en évidence que la SHF du NST, de même que les traitements à la L‑DOPA, induisent une diminution du taux de sérotonine, système impliqué dans l’inhibition comportementale et dans la physiopathologie de différents troubles. Afin d’évaluer le potentiel thérapeutique d’un traitement visant ce système, nous avons suivi le même protocole en utilisant cette fois un inhibiteur sélectif de recapture de la sérotonine. Il s’agit de la fluoxétine, antidépresseur couramment utilisé chez l’Homme. La fluoxétine a été administrée par injection aigue intrapéritonéale, réalisée 30 minutes avant le début du test. Nous avons pu observer que ce traitement, conduisant à une augmentation du taux de sérotonine, a pour conséquence de contrecarrer l’effet délétère de la lésion du NST sur la prise de décision : les animaux lésés présentent en effet un comportement semblable au comportement de base des animaux contrôles (c’est à dire un nombre d’appui environ équivalent entre le levier petite et grande récompense). La fluoxétine réduit donc les effets pro-impulsifs induits par l’inactivation du NST. Le système sérotoninergique pourrait donc également être impliqué dans l’altération du processus décisionnel chez les patients parkinsoniens. L’utilisation d’un inhibiteur sélectif de sérotonine, déjà couramment utilisé pour traité la dépression et d’autres troubles chez l’Homme, pourrait donc potentiellement être une perspective thérapeutique envisageable.
C — JUSTIFICATION DE L’ÉTUDE ET PERSPECTIVES
Cette étude nous a déjà permis de clarifier le rôle du NST dans les processus décisionnels chez le rat, puisque nous avons pu montrer que la perturbation de l’activité du NST par lésion de la structure, conduit à un comportement plus risqué.
Afin d’approfondir d’avantage cette étude, nous souhaiterions également étudier l’effet d’un traitement à la L‑Dopa sur cette tâche chez le rat. Ce traitement sera réalisé seul, ou en combinaison avec un antagoniste des récepteurs dopaminergiques, mimant la déplétion dopaminergique présente chez le patient parkinsonien.
Avec pour objectif de confirmer et approfondir nos recherches, nous souhaiterions vérifier la reproductibilité de ces résultats sur un nouveau groupe de rats, qui sont d’ores et déjà en cours d’apprentissage de la tâche permettant de mesurer la prise de décision.
La poursuite de ce projet nous permettrait une meilleure compréhension de l’implication du NST et des différents systèmes de neurotransmission dans les processus de prise de décision altérés chez certains patients parkinsoniens. Pouvoir anticiper et apporter une solution thérapeutique aux troubles cognitifs qui pourraient résulter du traitement chirurgical et dopaminergique chez le patient atteint de la maladie de Parkinson représente un enjeu majeur.
Lu par Jean Graveleau graveleau.jean2@orange.fr
Pas encore de Commentaires Cliquer ici pour laisser un commentaire
Laisser un commentaire
Flux RSS des commentaires de cet article. Rétrolien URI
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.