Comment le cerveau se nettoie pendant le sommeil
Publié le 14 janvier 2014 à 12:31Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Dormir permet au cerveau de se débarrasser des toxines accumulées pendant la période de veille
On savait déjà que le sommeil permet de consolider les données apprises dans la journée. Il semblerait qu’il permet aussi au cerveau de se débarrasser de ses toxines
Des chercheurs américains pensent avoir compris pourquoi l’homme est programmé pour dormir plusieurs heures chaque nuit, alors que le sommeil le laisse vulnérable aux prédateurs. Le repos permettrait au cerveau de se débarrasser des toxines produites pendant les phases d’éveil, explique l’équipe de l’Université de Rochester (Etat de New York) dans un article publié dans la revue Science.
« La nature récupératrice du sommeil résulterait de l’élimination des déchets produits par l’activité neuronale qui s ‘accumulent pendant la période d’éveil », explique le Dr Malken Nedergaard, le principal auteur des travaux.
Le rôle essentiel du sommeil dans l’apprentissage et la mémoire était déjà connu, mais les chercheurs ont cette fois expliqué l’intérêt chimique d’alterner les phases d’éveil et de repos. « Cette recherche a permis de voir que le cerveau a deux états de fonctionnement distincts. Il est soit éveillé et alerte, soit dormant et en mode nettoyage. Comme il ne dispose que de ressources énergétiques limitées, il est contraint d’alterner entre l’un et l’autre ».
Dans le reste du corps, c’est le système lymphatique qui élimine les déchets cellulaires. Mais il n’inclut pas le cerveau, qui reste en vase clos, protégé par un système complexe de portes d’accès moléculaires contrôlant entrées et sorties. Le cerveau utilise lui un système unique appelé « glymphatique » dix fois plus actif pendant le sommeil qu’en éveil, ont montré les chercheurs.
Les chercheurs ont pu observer pour la première fois ce système de nettoyage cérébral grâce à une nouvelle technologie d’imagerie, utilisée sur des souris dont le cerveau est similaire à celui des humains.
Le mécanisme est intégré dans le système sanguin du cerveau. Il pompe le fluide cérébro-spinal à travers les tissus et le renvoie purifié, les déchets étant transportés par le sang jusqu’au foie où ils sont éliminés. De plus, les chercheurs ont découvert que les cellules cérébrales réduisaient leur taille de 60% quand on dort, permettant aux déchets d’être enlevés plus efficacement.
Tout cela permet notamment de nettoyer les toxines responsables de la maladie d’Alzheimer et d’autres pathologies neurologiques.
Article relevé dans le Figaro Santé du 18 Octobre 2013 par F. Vignon
La Levodopa Equivalent Dose (LED), ou comment déterminer la L‑dopa reçue par le malade
Publié le 13 janvier 2014 à 11:37Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Par Claire Smith
Les traitements médicamenteux de la maladie de Parkinson Idiopathique ont pour but de compenser le déficit dopaminergique au niveau du striatum, en administrant :
- soit un précurseur de la dopamine
- soit un agoniste dopaminergique
- ou bien en inhibant les métabolismes de la dopamine MAO‑B et COMT.
Dans un article paru dans Le Parkinsonien Indépendant n°53 de Juin 2013, des conseils d’utilisation des différents médicaments antiparkinsoniens sont donnés aux patients. (Dossier réalisé par l’Agence Nationale de Sécurité du Médicament et des Produits de Santé).
Pour établir la prescription, le neurologue va choisir parmi une panoplie d’une quinzaine de médicaments ceux qui correspondent le mieux au traitement des troubles du patient. Puis, il lui faudra doser chaque médicament, et déterminer l’efficacité globale du traitement. Au final, l’ordonnance journalière se présente comme une liste de plusieurs médicaments (de 3 à 5 par exemple), très souvent à libération immédiate, mais parfois à libération prolongée (LP) avec des dosages de plus en plus variés. Il devient alors peu évident de comparer l’efficacité de deux traitements ou de prévoir la substitution d’un médicament par un autre. C’est ici qu’intervient la notion de LED (Levodopa Equivalent Dose). C’est le sujet de l’article qui suit, rédigé à partir de comptes rendus de travaux réalisés à l’Université de Birmingham (UK) et publiés par Claire Smith.
Définition de la LED :
La LED d’un médicament est définie comme la quantité de ce médicament qui a le même effet antiparkinsonien que 100 mg de Lévodopa à libération immédiate. Dans cet article, le Sinemet 100 constitue la référence. L’effet antiparkinsonien est estimé par mesure de la motricité du patient (section III de l’UPDRS grille déterminant le degré de handicap).
Quelques exemples de Led :
- Led du Sinemet 100 mg : 100 mg
- Led du Sinemet LP 100 mg : 133 mg
- Led du Requip : 5 mg
- Led du Sifrol (sel) : 1 mg
Suite à la réaction de certains lecteurs, il parait nécessaire de fournir des explications complémentaires .Reprenons donc la comparaison entre le Sinemet à libération immédiate et la forme à libération prolongée LP, moins efficace (25 % de perte, selon Claire Smith). Si l’on compare l’effet de 2 comprimés de Sinemet, l’effet antiparkinsonien du comprimé classique est de 100, alors que celui du comprimé LP est de 75. Si on compare les Led de ces deux Sinemet, on notera qu’il faut une dose plus grande de Sinemet LP pour obtenir le même effet qu’avec du Sinemet classique (Led = 100 mg).
La Led du Sinemet LP 100 mg est donc plus grande, soit (100/75) X 100 = 133 mg
Les travaux de l’Université de Birmingham :
Il s’agit de travaux de collecte et de traitement de données sur l’ensemble des médicaments antiparkinsoniens sur le marché, jusqu’en 2009. La démarche suivie consiste tout d’abord, à collecter, à partir de mots clés « levodopa » et « equivalency », toute information de 1980 à 2009 sur l’efficacité des antiparkinsoniens, et cela pour tous les types d’études publiées en anglais. Les données ont fait ensuite l’objet de traitements statistiques (mean et mode), pour aboutir à l’obtention de Led pour tous les antiparkinsoniens.
L’étude a fourni les résultats suivants en Led, exprimés en mg, pour une quinzaine de médicaments antiparkinsoniens. Alors que les auteurs désignent chaque médicament, par le nom de sa molécule (Pramipexole, Ropinirole etc..), nous avons volontairement conservé les dénominations commerciales (Sifrol®, Requip® etc..) plus familières aux lecteurs francophones :
Médicaments à base de Levodopa :
- Sinemet 100 à libération immédiate : 100 mg
- Sinemet 100 à libération prolongée LP : 133 mg
- Modopar 125 à libération immédiate : 100 mg
- Stalevo : 77 mg
- Duodopa : 90 mg
Agonistes dopaminergiques :
- Sifrol (sel) 1 mg
- Requip 5 mg
- Neupro 3,3 mg
- Trivastal 100 mg
- Parlodel 10 mg
- Célance 1 mg
- Dopergine 1 mg
Inhibiteurs :
- Deprenyl 10 mg
- Otracel 1,25 mg
- Azilect 1 mg
- Mantadix 100 mg
Les valeurs fournies par Claire Smith sont commentées et parfois contestées dans la revue NeuroTalk, par des blogueurs qui fournissent par ailleurs quelques informations complémentaires. Signalons aussi que ces valeurs retenues sont corroborées par un tableau d’équivalence de dose fourni par Defebvre et Vérin, à la page 163, de leur livre « La maladie de Parkinson ».
Utilisation de la Led :
Désormais, on connait la Led de chacun des médicaments composant une ordonnance journalière. On peut alors calculer l’équivalent Levodopa pour chaque médicament en appliquant la formule : (Posologie journalière / Led) X 100 en mg. Exemple : pour une prescription de 2 comprimés de Requip 4 mg : 8/5 X 100 = 160 mg. On peut ensuite calculer la dose globale journalière, en additionnant les équivalents Lévodopa.
Soit une ordonnance comprenant :
3 comprimés de Sinemet à 100 mg soit : 100/100 X 300 = 300 mg
1 comprimé de Sinemet LP à 100 mg, soit : 100/133 X 100 = 75 mg
1 comprimé de Azilect 1 mg soit : 1/1 X 100 = 100 mg
1 comprimé de Requip à 8 mg soit : 8/5 X 100 = 160 mg
Soit un total d’équivalent Levodopa par jour de : 635 mg
Il s’agit d’une dose journalière plutôt moyenne. Cette dose peut excéder 1 000, voire 1 500.
Bibliographie :
— Levodopa Dose Equivalency par Claire Smith du Clinical Trials Unit de l’Université de Birmingham (UK).
— Levodopa Dose Equivalency dans la revue NeuroTalk
Traduit et transmis par Jean Pierre Lagadec jpmo5@orange.fr
Ça aussi, c’est bon pour les neurones !
Publié le 07 janvier 2014 à 10:46Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
« Quand le corps soigne l’esprit » Relevé dans Ca m’intéresse de Décembre 2013
Relaxer son corps pour relancer son cerveau :
La relaxation est la capacité du corps à relâcher ses muscles, ralentir le rythme cardiaque et la respiration. Les méthodes sont multiples, partant du corps (relaxation musculaire progressive, respiration profonde) ou de l’esprit (méditation, visualisation).
Elle permet de s’opposer aux effets du stress et de l’anxiété, améliore le sommeil ainsi que les performances cognitives lors de tâches simples. Ses effets passeraient par une modification de l’expression de certains gènes. Une étude parue en 2013 montre ainsi que ceux qui pratiquent la relaxation, même novices, expriment moins certains gènes impliqués dans le stress et l’inflammation, et d’avantage d’autres gènes, engagés dans le métabolisme énergétique.
Mobiliser les muscles du sourire pour se sentir joyeux :
Une étude de juin 2012 de l’Université du Kansas l’a confirmé : sourire déstresse et rend heureux. Ce simple mouvement d’environ 17 muscles faciaux a suffi à déclencher dans le cerveau des participants, bien qu’ils soient plongés dans une activité stressante, des modifications biochimiques libérant les tensions. Il favoriserait la production d’endorphines. « Sourire envoie un message positif à notre cerveau, qui nous transmet en retour une sensation de bien être », renchérit le Dr Nathalie Rapoport-Hubschman. Ces vertus n’ont pas échappé aux maître yogis et taoïstes qui recommandent la pratique du « sourire intérieur ». Il suffit de visualiser une situation positive, ce qui se solde par un mouvement vers le haut de la commissure de nos lèvres.
Déstresser en se faisant masser :
Circulation sanguine, oxygénation du cerveau… Les études du Touch Research Institute de Miami prouvent qu’un massage de quinze minutes bihebdomadaire chez les adultes, diminuent le stress ressenti au travail. « Le taux de cortisol, hormone du stress, chute tandis que l’ocytocine (hormone de la confiance et du bien-être, ndlr) augmente » précise Isabelle Bachelet, praticienne en massage tuina. L’interaction entre peau et cerveau s’explique, selon le Pr Didier Anzieu car « tous deux proviennent d’un tissu unique, l’ectoderme, qui se forme au 21ième jour de l’embryon ».
S’hydrater pour irriguer ses méninges :
On sait qu’il est nécessaire d’hydrater régulièrement notre corps, composé à 60% d’eau. Notre cerveau, lui, en compte 80%. Certaines études concluent qu’une perte d’eau sévère (équivalente à 5% ou d’avantage du poids corporel) ou plus modéré (2%) mais rapide (qui s’installe en quelques heures) altérerait les fonctions cognitives, entraînant une confusion, des difficultés à se concentrer, des céphalées, une plus grande irritabilité. Ces effets seraient particulièrement perceptibles chez les enfants et les personnes âgées. Des études ont montré que des enfants de 6 à 9 ans étaient moins performants pour effectuer des exercices faisant appel à la mémoire et l’attention s’ils n’avaient pas assez bu.
par Soizic Vignon soize.vignon@orange.fr
Le Dipraglurant® Une arme contre les dyskinésies
Publié le 03 janvier 2014 à 09:25Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Depuis plusieurs années, la firme pharmaceutique Suisse Addex Pharmaceuticals (SIX:ADXN), spécialisée en « modulation allostérique », travaille sur l’étude et le développement de molécules destinées à traiter les dystonies et les dyskinésies chez les patients Parkinsoniens.
C’est le cas du Dipraglurant® pour des patients souffrant de dyskinésie induite par la L‑dopa dans la maladie de Parkinson. La dyskinésie induite par la L‑dopa est un trouble moteur débilitant engendré par l’administration à long terme de traitements contenant de la L‑dopa, thérapie standard de référence pour la maladie de Parkinson.
L’étude conduite en parallèle aux Etats-Unis et en Europe est financée en partie par une subvention de la Fondation Michael J. Fox pour la Recherche contre la maladie de Parkinson.
Les dyskinésies :
Le Dipraglurant® ayant pour indication le traitement des dyskinésies Parkinsoniennes, rappelons pour les nouveaux lecteurs, de quoi il s’agit. Les dyskinésies font partie des mouvements anormaux (ou involontaires), dont peuvent être victimes les Parkinsoniens. Elles peuvent être décrites comme des mouvements soudains, incontrôlables, souvent désordonnés. Elles affectent les membres, la tête, les lèvres, et la langue. Elles sont en général, dues à un surdosage de la L Dopa. Or, il n’y a pas de produit pouvant remplacer la L Dopa avec les mêmes avantages.
Cela a des conséquences fâcheuses :
- Le patient (souvent en présence de son entourage ou en public) subit des crises dévalorisantes et fatigantes.
- A mesure que la maladie s’aggrave, il est de plus en plus difficile pour le neurologue d’ajuster la prescription afin d’éviter périodes de blocage et périodes de dyskinésie, l’espace thérapeutique étant de plus en plus réduit. Cette difficulté a justifié la réalisation de logiciels d’optimisation des traitements, à partir de données pharmacocinétiques (cf. article sur le Led ci-dessus et feuille de calcul présentée dans le P. I. n°32).
- Pendant de nombreuses années (après le consensus de Mars 2000), on a essayé dans certains cas bien définis de différer le début de prise de la L‑dopa pour retarder les survenues de dyskinésies.
Sait-on traiter les dyskinésies ? On reparle actuellement d’un médicament ancien, le Mantadix. On parle aussi de chirurgie à partir de la stimulation du globus pallidum. Mais les solutions les plus séduisantes seraient obtenues par l’arrivée sur le marché de 3 nouvelles molécules. L’une d’elles est le Dipraglurant®.
Changer la stratégie thérapeutique :
Si les essais cliniques à venir confirment les résultats déjà obtenus et après obtention de l’Autorisation de Mise sur le Marché (en 2014), le Dipraglurant® pourrait constituer une arme efficace contre les dyskinésies, dont il pourrait pallier, en tout ou partie, les inconvénients que nous avons évoqués précédemment. Il serait alors plus facile d’utiliser la L‑Dopa, qui est le médicament de référence pour la maladie de Parkinson.
Par ailleurs, l’arrivée sur le marché de produits contre les dyskinésies, comme le Dipraglurant®, constitue un argument en faveur du changement de la stratégie thérapeutique qui avait été définie dans le consensus 2000. On pourra en effet traiter à la L‑dopa, précocement dans la phase initiale de la maladie, si on a moins ou pas de risques de dyskinésies à long terme.
Rédigé par Jean Pierre Lagadec jpmo5@orange.fr
Bilan des deux boursières soutenues par CECAP (2/2)
Publié le 02 janvier 2014 à 09:56Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Bilan de Julie Meffre : Rôle du Noyau Subthalamique dans la Prise de Décision
A — PROJET DE RECHERCHE
1. Contexte de l’étude
Alors que la maladie de Parkinson a été longtemps abordée sur la base de ses symptômes moteurs, les troubles non moteurs qui lui sont associés font, depuis quelques années seulement, l’objet de recherches plus approfondies. La stimulation à haute fréquence (SHF) du noyau subthalamique (NST), utilisée avec succès pour traiter les troubles moteurs, peut cependant être à l’origine d’effets secondaires cognitifs comme un comportement impulsif ou risqué (tendance au jeu pathologique) chez certains patients. Il a été mis en évidence que la SHF altère la capacité à « freiner » la prise de décision face à une situation conflictuelle, conduisant les patients à prendre une décision hâtive et impulsive (Frank et al. 2007). Parmi les ganglions de la base, le NST semble être impliqué dans le contrôle de l’impulsivité/inhibition comportementale (Frank 2006 ; Eagle and Baunez 2010). La voie hyperdirecte, reliant les aires corticales frontales au NST pourrait être à l’origine de la régulation des processus décisionnels. Le NST semble agir en élevant le seuil de décision dans le cas d’une situation conflictuelle ou ambiguë, conduisant ainsi à différer la prise de décision, jusqu’à ce que suffisamment d’indices aient été accumulés.
2. But de l’étude
Afin de pouvoir améliorer l’anticipation d’éventuels effets secondaires de la stimulation à haute fréquence du NST sur la prise de décision chez les patients parkinsoniens, il est indispensable de bien comprendre le rôle de cette structure dans les processus décisionnels. L’objectif de notre travail de recherche, soutenu par la CECAP, a été de déterminer chez le rat
- comment le NST contribue à la prise de décision grâce à une approche comportementale réalisée chez des rats intacts versus des rats ayant subit une lésion du NST (mimant l’effet de la SHF du NST utilisée chez le patient parkinsonien)
- quelle est l’influence du système dopaminergique dans ce processus, et
- le potentiel thérapeutique d’un traitement visant le système sérotoninergique, système impliqué dans l’inhibition comportementale.
3. Procédures expérimentales utilisées
Animaux : 10 rats mâles Long Evans, maintenus dans un cycle 12h jour/nuit, ont été utilisés pour ces expériences. Ils ont été soumis à une restriction alimentaire, avec un accès à 85% de leur ration quotidienne. L’eau était accessible ad libitum.
Expérience : Mesure de la prise de décision impliquant l’évaluation d’un risque (en terme de probabilité de gain)
Les animaux sont placés dans une boîte opérante comportant trois leviers. Au démarrage de l’essai, seul le levier central est sorti, et les rats ont été entraînés à maintenir leur patte sur le levier central pendant une durée fixe de 1 seconde. 400 ms après le début de l’appui et pendant 600 ms, une combinaison de deux lumières s’allume au-dessus des leviers et indique quelle sera la probabilité d’obtenir 0.1 ml de sucrose 32% en cas de choix du levier correspondant à la récompense en grande quantité mais incertaine. Au bout de 600 ms, un signal sonore retentit, indiquant la possibilité d’aller appuyer sur le levier de gauche ou de droite, au choix, afin d’obtenir une récompense (0.05 ml de sucrose 32 % toujours délivré ou 0.1 ml sucrose 32 % délivré avec une probabilité variable et indicée, respectivement).
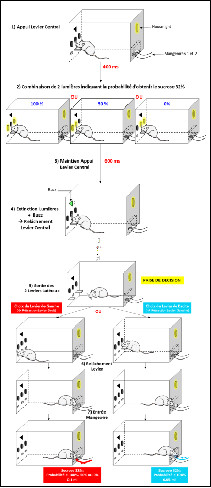
Trois combinaisons de deux lumières sont possibles, aléatoirement. Il existe trois spots lumineux situés au-dessus des leviers :
- Si la lumière de gauche et la lumière de droite s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 100 %.
- Si la lumière de gauche et la lumière centrale s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 50 %.
- Si la lumière de droite et la lumière centrale s’allument, la probabilité d’obtenir 0.1 ml de sucrose 32 % en choisissant le levier de droite est de 0 %.
A la fin de la seconde d’appui, le levier central se rétracte et les deux leviers latéraux sortent.
- Si l’animal choisit le levier de droite, il appuie puis peut relâcher immédiatement le levier et une dose de 0.05 ml de sucrose 32 % est délivrée dans la mangeoire dans 100 % des cas.
- Si l’animal choisit le levier de gauche, le résultat de cette action sera incertain, en fonction de la probabilité d’obtenir 0.1 ml de sucrose 32%, indiquée précédemment par la combinaison de lumière.
La condition 100% et la condition 0% permettent de vérifier la bonne compréhension de la tâche par le rat. La condition 50% permet d’évaluer le comportement à tendance risquée ou non de l’animal. Ainsi, si dans la condition où la probabilité d’obtenir la grande récompense est de 50%, le rat choisi préférentiellement le levier associé à cette grande récompense, il sera considéré comme un individu au comportement risqué et joueur.
La moitié des animaux est conditionnée avec cette règle. Pour l’autre moitié, la petite récompense est délivrée lorsque l’animal choisit le levier droit.
Chirurgie : Lésion du NST
Lorsque les animaux ont atteint un niveau de performance stable durant au moins 5 sessions consécutives, ils ont été soumis au protocole chirurgical suivant :
Tous les animaux ont été anesthésiés avec de la kétamine (50 mg/kg, i.m.) et de la médétomidine (0.26 mg/kg, i.m.) et positionnés dans un appareil de stéréotaxie.
Les rats reçoivent une injection bilatérale d’acide iboténique (9.4 µg/µl (53 mM); rats avec lésion du NST) ou de solution contrôle (tampon phosphate, 0.1 M ; rats intacts) aux coordonnées suivantes : antéropostérieur, 3.8 mm (depuis le bregma); latéral, 2.4 mm ; dorsoventral, 8.35 mm (depuis le crâne). Le volume d’injection était de 0.5 microlitres par côté injecté pendant 3 minutes avec une seringue Hamilton fixée sur une micropompe. A la fin de l’injection, les injecteurs ont été laissés en place pendant 3 min pour permettre la diffusion de l’acide iboténique.
Les animaux ont récupéré des suites de l’opération pendant une semaine avant d’être à nouveau soumis au test (dans la même tâche que celle précédent la chirurgie)
B — RÉSULTATS PRÉLIMINAIRES
près apprentissage de la tâche, les animaux ont été soumis au test de prise de décision, et le pourcentage de prise de décision risquée (évaluée par le nombre d’appui sur le levier associé à la grande récompense dans la condition où la probabilité de l’obtenir est de 50%) a été mesuré. Nous avons ainsi mesuré le pourcentage de prise de décision risquée de base chez le rat, avant lésion du NST. Nous avons pu vérifier que les performances moyennes des rats avant l’opération ne présentaient pas de différences significatives, tous les individus choisissant de manière équivalente la petite récompense certaine et la grande récompense risquée.
Les animaux ont ensuite été soumis au protocole chirurgical. Après une période de récupération, ils ont été à nouveau soumis au même test que celui précédent la chirurgie. Après lésion du NST, on observe une modification profonde du comportement des rats, qui choisissent alors préférentiellement la condition risquée (dans 80% des cas environ). Une altération du NST conduit donc à une altération de la prise de décision, favorisant un comportement impulsif et risqué. Ces résultats semblent donc indiquer que les effets secondaires cognitifs de type impulsivité et développement du jeu pathologique chez les patients traités par la SHF du NST pourraient résulter de l’inactivation du NST.
Afin d’évaluer l’influence du système dopaminergique, cible des traitements médicamenteux dans la maladie de Parkinson, dans ce processus, nous avons procédé à une injection intrapéritonéale d’un inhibiteur de recapture de dopamine, 20 minutes avant le début du test. De façon très intéressante, nous avons pu observer que ce traitement conduit, chez les rats intacts, à une très forte augmentation du nombre de prise de décision risquée, celui-ci passant de 40% à 80% environ après traitement pharmacologique aigue avec un inhibiteur de
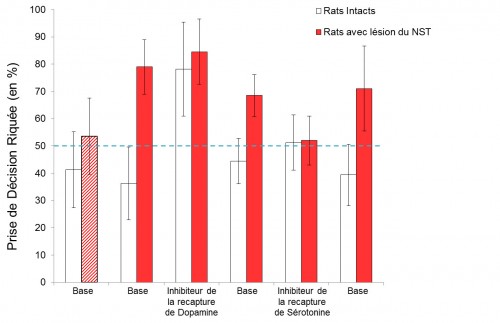
recapture de dopamine. Les rats intacts soumis à ce traitement dopaminergique présentent donc un comportement risqué similaire à celui des rats ayant subit une lésion totale du NST. Il semblerait donc que le système dopaminergique et le noyau subthalamique soient impliqués dans ce processus décisionnel.
Suite à ce traitement, les animaux ont été à nouveau soumis au test avec après avoir subit une injection de solution contrôle (sérum physiologique), afin de vérifier un retour à la normale (niveau de base) de leur performance comportementale.
Il a été mis en évidence que la SHF du NST, de même que les traitements à la L‑DOPA, induisent une diminution du taux de sérotonine, système impliqué dans l’inhibition comportementale et dans la physiopathologie de différents troubles. Afin d’évaluer le potentiel thérapeutique d’un traitement visant ce système, nous avons suivi le même protocole en utilisant cette fois un inhibiteur sélectif de recapture de la sérotonine. Il s’agit de la fluoxétine, antidépresseur couramment utilisé chez l’Homme. La fluoxétine a été administrée par injection aigue intrapéritonéale, réalisée 30 minutes avant le début du test. Nous avons pu observer que ce traitement, conduisant à une augmentation du taux de sérotonine, a pour conséquence de contrecarrer l’effet délétère de la lésion du NST sur la prise de décision : les animaux lésés présentent en effet un comportement semblable au comportement de base des animaux contrôles (c’est à dire un nombre d’appui environ équivalent entre le levier petite et grande récompense). La fluoxétine réduit donc les effets pro-impulsifs induits par l’inactivation du NST. Le système sérotoninergique pourrait donc également être impliqué dans l’altération du processus décisionnel chez les patients parkinsoniens. L’utilisation d’un inhibiteur sélectif de sérotonine, déjà couramment utilisé pour traité la dépression et d’autres troubles chez l’Homme, pourrait donc potentiellement être une perspective thérapeutique envisageable.
C — JUSTIFICATION DE L’ÉTUDE ET PERSPECTIVES
Cette étude nous a déjà permis de clarifier le rôle du NST dans les processus décisionnels chez le rat, puisque nous avons pu montrer que la perturbation de l’activité du NST par lésion de la structure, conduit à un comportement plus risqué.
Afin d’approfondir d’avantage cette étude, nous souhaiterions également étudier l’effet d’un traitement à la L‑Dopa sur cette tâche chez le rat. Ce traitement sera réalisé seul, ou en combinaison avec un antagoniste des récepteurs dopaminergiques, mimant la déplétion dopaminergique présente chez le patient parkinsonien.
Avec pour objectif de confirmer et approfondir nos recherches, nous souhaiterions vérifier la reproductibilité de ces résultats sur un nouveau groupe de rats, qui sont d’ores et déjà en cours d’apprentissage de la tâche permettant de mesurer la prise de décision.
La poursuite de ce projet nous permettrait une meilleure compréhension de l’implication du NST et des différents systèmes de neurotransmission dans les processus de prise de décision altérés chez certains patients parkinsoniens. Pouvoir anticiper et apporter une solution thérapeutique aux troubles cognitifs qui pourraient résulter du traitement chirurgical et dopaminergique chez le patient atteint de la maladie de Parkinson représente un enjeu majeur.
Lu par Jean Graveleau graveleau.jean2@orange.fr
Bilan des deux boursières soutenues par CECAP (1/2)
Publié le 27 décembre 2013 à 09:17Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Bilan de la thèse d’Elodie Mathieux : Le rejet suite à la greffe intracérébrale : étude de la réponse humorale et propriétés immunosuppressives des cellules souches.
La maladie de Parkinson est caractérisée par la dégénérescence progressive et sélective des neurones dopaminergiques de la voie nigrostriatale. La destruction des neurones dopaminergiques de la substance noire a pour conséquence une diminution de la sécrétion de dopamine au niveau du striatum.
Actuellement, il n’existe pas de traitement curatif de la maladie, mais différents traitements symptomatiques sont utilisés. L’administration par voie orale de L‑DOPA (lévodopa), précurseur de la dopamine capable de traverser la barrière hématoencéphalique, est l’un des traitements les plus couramment prescrits. Un inconvénient majeur de la prise de L‑DOPA est l’apparition, au bout de quelques années, de dyskinésies (mouvements anormaux). Une autre stratégie basée sur la stimulation électrique du noyau sous-thalamique montre une efficacité sur les troubles moteurs dans la plupart des cas, mais les risques chirurgicaux et les critères d’inclusion en font une opération accessible à un très faible nombre de patients. De plus, de nombreux symptômes ne sont pas corrigés par ces thérapies.
Aussi, il apparaît important de poursuivre les recherches sur les stratégies restauratrices, notamment la greffe intracérébrale de neuroblastes dopaminergiques fœtaux.
Des neuroblastes mésencéphaliques issus de fœtus humains (7 – 9 semaines) et transplantés dans le cerveau de patients parkinsoniens ont conduit à des améliorations cliniques basées, entre autres, sur la production de dopamine par les neurones greffés. Cependant, le recours à des cellules fœtales humaines est freiné par des considérations éthiques et logistiques qui limitent l’accès à ces greffes. Il est apparu alors nécessaire de se tourner vers d’autres sources cellulaires et notamment les cellules d’origine porcine.
En effet, le porc présente de nombreux avantages pour la xénotransplantation : un grand nombre d’embryons à chaque portée, une facilité d’élevage, la possibilité de contrôler la reproduction des animaux et de pouvoir pratiquer des manipulations génétiques. De plus, les neuroblastes issus de fœtus porcins émettent des neurites de longueurs similaires à celles observées chez l’Homme. Une survie des cellules greffées, une réinnervation du striatum ainsi qu’une récupération des fonctions motrices ont été observées lors d’essais cliniques menés chez certains patients parkinsoniens traités par des immunosuppresseurs (molécules permettant de limiter l’activité du système immunitaire). Mais le problème rencontré reste le rejet de ces greffes.
En effet, en l’absence d’immunosuppresseur comme la cyclosporine A, les greffes de neuroblastes porcins dans le striatum de rat sont systématiquement rejetées au bout de 7 – 8 semaines. Les traitements par des immunosuppresseurs prolongent la survie de la greffe, mais de manière transitoire. De plus, utilisés à fortes doses, ceux-ci entraînent des effets secondaires, notamment une toxicité rénale. Il est donc important de comprendre et d’étudier les mécanismes en cause dans le rejet pour envisager une survie à long terme de la greffe.
Diverses études ont mis en évidence un rôle important de la réponse immunitaire cellulaire dans le rejet. En effet, en l’absence d’immunosuppresseur, on observe vers 7 à 8 semaines une forte infiltration de la greffe par des lymphocytes T, des cellules dendritiques et des cellules microgliales activées.
Outre la réponse cellulaire, il a été observé un dépôt d’anticorps et de complément au niveau du greffon. Cette observation suggère une réponse humorale caractérisée par la production d’anticorps dirigés contre la greffe, qui, à ce jour, a été très peu étudiée.
Une partie de mon travail de thèse au sein de l’INSERM U1064 de Nantes a eu pour but de caractériser le rôle de la réponse humorale dans le rejet des xénogreffes intracérébrales.
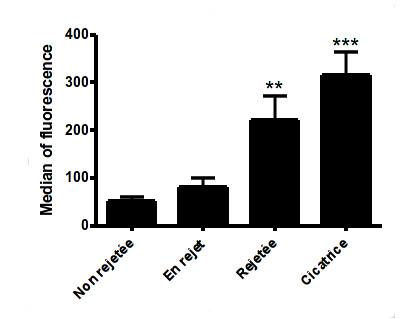
Evolution de la production d’anticorps au cours des différents stades du rejet.
Les anticorps produits suite à la greffe vont venir se fixer sur les cellules porcines du greffon et le détruire. Nous avons pu mettre en évidence que la production d’anticorps augmentait en fonction du délai post greffe et du statut de la greffe. En particulier, une forte concentration d’anticorps est observée dans le sérum de rats pour lesquels la greffe est rejetée. Les anticorps accompagnés d’une activation du complément seraient cependant, en premier lieu, attirés au sein de la greffe avant d’être détectés dans le sérum.
Evolution de la production d’anticorps au cours des différents stades du rejet.
Les anticorps vont préférentiellement venir se fixer sur les neurones et en moindre mesure sur les astrocytes. De plus, la survie des greffes de cellules mésencéphaliques porcines est augmentée chez des rats ne possédant plus d’anticorps. Ces résultats suggèrent un rôle important de la réponse humorale dans le rejet des xénogreffes intracérébrales.
Afin de limiter le rejet des greffes intracérébrales, une autre partie de mon travail a été d’étudier les propriétés immunosuppressives des cellules souches et en particulier des cellules souches neurales (CSN). Les CSN sont des cellules multipotentes capables d’auto-renouvellement et de prolifération. Elles peuvent générer les trois types cellulaires principaux du système nerveux central que sont les neurones, les astrocytes et les oligodendrocytes. Les CSN vont pouvoir être cultivées sous forme de neurosphères.
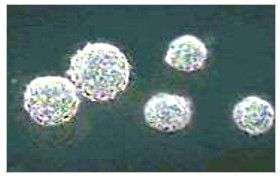
Cellules souches neurales de rat sous forme de neurosphères.
Nous avons pu démontrer que les CSN de rat inhibaient la prolifération des cellules T de rat de manière dose dépendante. Les CSN agissent alors par l’intermédiaire de facteurs solubles dont l’hème oxygénase.
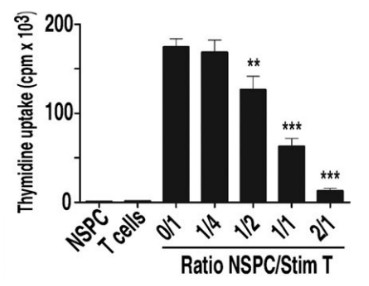
Inhibition de la prolifération des cellules T de rat par les cellules souches neurales de rat de manière dose dépendante.
Les CSN possèdent donc des propriétés immunosuppressives qui permettraient de limiter le rejet lors de greffes intracérébrales tout en diminuant l’utilisation d’immunosuppresseurs systémiques.
L’ensemble des résultats de ma thèse ouvre des nouvelles perspectives pour parvenir à contrôler le rejet de xénogreffes intracérébrales. En l’occurrence, on pourrait espérer qu’une immunosuppression locale, basée sur la transplantation de cellules souches associées à une administration systémique d’immunosuppresseurs ciblant les réponses humorales et cellulaires, soit suffisamment efficace pour assurer la survie à long terme de cellules neurales xénogéniques dans un cerveau.
Je tenais à remercier tous les membres de l’association CECAP pour leur soutien tout au long de ma thèse.
Rédigé par Elodie Mathieux
Cure de nicotine contre la maladie de Parkinson
Publié le 20 décembre 2013 à 07:42Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
Article paru dans Sud-ouest Dimanche du 10 novembre 2013
Isabelle Castillon part en croisade pour défendre la nicotinothérapie.
Isabelle Castillon vit à Bayonne. Atteinte depuis 1987, elle participe au protocole unique de nicotinothérapie en France. Et ça va mieux ! La maladie de Parkinson a eu tort de s’en prendre à Isabelle Castillon. Elle est tombée sur un os. Car cette enseignante, installée à Bayonne, n’est pas du genre à se laisser attraper sans broncher. À 64 ans, elle participe en tant que patiente à un protocole thérapeutique unique en France. Totalement alternatif, révolutionnaire, archicontroversé, puisqu’il fait appel à la nicotine. Un mot est né de cette initiative médicale : nicotinothérapie.
Retour en 1987. Isabelle se souvient : « Je me dédouble, je m’entends parler, avec un écho, parfois je me mets à trembler. Je ne dors plus. En consultation, je vois un neurologue, il me prescrit un anxiolytique. Mais en 1992, je plonge. Trois semaines sans pratiquement dormir. Je suis hospitalisée pour dépression pendant un mois et j’en sors toujours aussi mal. Mes problèmes physiques se multiplient. C’est un neurologue que je croise qui va me diagnostiquer : Parkinson. »
Panique et soulagement. Isabelle sait ce qu’elle a ; elle est désormais prise en charge et traitée à la L‑dopa. « Je découvre ce que signifie l’expression lune de miel. La L‑dopa dope… pendant dix ans en moyenne », poursuit-elle. Puis, Isabelle Castillon la battante, toujours prof, est rattrapée par les symptômes de Parkinson qui se bousculent. « Mon écriture se rétrécit, je marche de plus en plus lentement, des difficultés d’élocution, tremblements, dyskinésie (mouvements involontaires). J’ai peur de sortir, je me renferme. J’ai honte qu’on me juge, car on me juge. Je prends des renseignements partout, pour aller mieux. »
Quatre ans de patience :
Parkinson est une maladie neurodégénérative, Isabelle sait qu’il faudra accepter la dégringolade. Elle se rebelle. « Un jour, en 2000, je découvre un reportage sur CNN. Il est question de nicotine dans le traitement de Parkinson. Je note le nom du médecin : Gabriel Villafane, de l’hôpital Henri-Mondor à Créteil (94). Je vais batailler des mois pour obtenir un rendez-vous. La débrouille et le bouche-à-oreille. Je débarque à Mondor avec mon dossier médical, mais il faudra encore quatre ans de patience avant d’obtenir mes premiers patchs de nicotine pure. » DAT-Scan, un scanner qui date les courts-circuits du cerveau générés par la maladie, examens du cœur, tension, sang. Le corps et le cerveau d’Isabelle sont passés au crible. En 2009, elle obtient enfin la première série de patchs.
« Il faut le positionner en bas de la colonne, dans le dos. La nicotine diffuse alors jusqu’au cerveau », précise la patiente. Les effets positifs du traitement se font sentir au bout de quelques semaines. La maladie ne disparaît pas, mais les symptômes régressent. Isabelle demeure sous L‑dopa, bien entendu. « J’ai recommencé à marcher, je ne tremble plus, la dyskinésie a pratiquement disparu, je suis plus active, le moral revient. Je vois des gens, je sors et, surtout, je me moque éperdument du regard des autres. La joie de vivre à nouveau… Aujourd’hui, je m’occupe de mes petits-enfants, je chante. Sans la nicotine pure, je serais à ce jour en fauteuil roulant. J’ai diminué de moitié la dose de mes médicaments. Ce fut un parcours du combattant, et aujourd’hui encore, je me heurte à l’incrédulité de mes médecins, des neurologues, des pharmaciens. Je suis considérée comme une malade récalcitrante. »
Thérapie ostracisante :
Des médecins l’accusent de s’adonner à une thérapie « ostracisante » parce que les patchs ne sont pas remboursés par la Sécurité sociale. « Que font les autres, ceux qui ne peuvent pas payer ? » entend-elle. Les pharmaciens lui font la morale. Certains lui ont même asséné : « À ce prix, mieux vaut reprendre les cigarettes, c’est moins cher ! » En effet, deux boîtes de patchs par mois reviennent à 80 euros (1). Pas à la portée de toutes les bourses…
D’un autre côté, les réseaux sociaux bouillonnent, les malades de Parkinson cherchent des solutions pour aller mieux, ils veulent tout tenter, s’intéressent de près aux travaux de recherche. Alors, Isabelle Castillon est partie en croisade, elle mesure que tout le monde n’a pas son tempérament têtu. « Si je me fais connaître, c’est pour qu’un réseau défendant la nicotinothérapie se monte. Je sais que tous les patients ne peuvent pas être traités, parce que le traitement répond à des critères exigeants. Il n’est pas sans risque s’il est prescrit n’importe comment. Il faut savamment doser le taux de nicotine. » Les patients suivis à l’hôpital Mondor de Paris sont en train de se fédérer pour monter un collectif pro-nicotinothérapie. Et inciter le réveil des pouvoirs publics qui, enfin, cautionneront le médicament.
(1) À ce jour, les patchs de nicotine sont remboursés à hauteur de 50 euros par an.
Interview de Gabriel Villafane, neurologue à l’hôpital Henri-Mondor de Créteil
C’est lui qui a mis au jour ce traitement alternatif de la maladie de Parkinson. Neurologue au sein de l’hôpital Henri-Mondor à Créteil, Gabriel Villafane a, en 1999, avec son chef de service, le professeur Pierre Cesaro, déposé une demande de brevet sous cette appellation : « Utilisation de la nicotine à l’état pur comme médicament pour les maladies neurodégénératives, notamment la maladie de Parkinson… »
Sud-ouest Dimanche : Comment avez-vous pensé à utiliser la nicotine pure ?
Gabriel Villafane : J’ai observé des malades, notamment psychiatriques, placés sous neuroleptiques qui devenaient accros à la cigarette. Alors qu’ils étaient atones, lorsqu’ils fumaient, ils retrouvaient une énergie, le temps de la cigarette. J’ai fait le lien : la nicotine. Nous avons déposé un brevet en1999, au nom de l’Assistance publique. Il est protégé durant vingt ans. En 2009, la validité scientifique du brevet a été validée.
S‑O : Combien de patients avez-vous suivis avec ce traitement ?
G. V. : À ce jour, plus de 1 000 personnes. Le plus ancien est sous nicotine pure transdermale (NEP) depuis douze ans. Il va bien. Le premier protocole a permis à six patients de tenter cette aventure. En 2004, face à une arrivée massive de demandes de patients, nous avons été débordés. Il a fallu créer un second protocole, intitulé « protocole compassionnel ». Nous assurons le diagnostic, les examens, la prescription, mais les patients doivent payer la NEP, pas remboursée.
S‑O : Pourquoi cette thérapie alternative, alors qu’elle semble porter ses fruits, tarde-t-elle à trouver plus d’écho ?
G. V. : D’abord, elle n’est pas politiquement correcte. Le message autour de la nicotine est complexe. D’un côté, on connaît les dégâts du tabac, de l’autre, on veut faire entendre que la nicotine peut être un médicament… Il ne s’agit pas de fumer, la cigarette est un danger. La nicotine à l’état pur n’est pas dangereuse. Elle est un neuro-modulateur des neurones du système nerveux central. Un neurotransmetteur qui intervient au niveau de la synapse neuronale, des récepteurs de la dopamine dans le cas de Parkinson. Les observations cliniques et d’imagerie (DAT-Scan) montrent un ralentissement de la maladie. Alors, pourquoi ce blocage ?
Aujourd’hui, on soigne Parkinson avec des traitements chimiques et chirurgicaux. En dehors de la NEP, aucun traitement n’agit aussi bien sur l’évolution de la maladie. À ce jour, nous n’arrivons pas à obtenir une autorisation de mise sur le marché (AMM) des patchs nicotiniques, qui sont conçus pour un usage transitoire et seulement à vocation de sevrage tabagique. Du coup, les parkinsoniens que nous traitons sont quasi clandestins… Aux États-Unis, en Allemagne, les publications sur les vertus de la nicotine dans le traitement de Parkinson affluent. Ils vont nous doubler et déposer des brevets de patchs nicotiniques pour Parkinson avant nous.
Trop de lenteurs administratives, de peurs.
Recueilli par Isabelle Castera i.castera@sudouest.fr
Transmis par Dominique Bonne dominique.bonne@gmail.com
Éditorial
Publié le 19 décembre 2013 à 07:49Article paru dans LE PARKINSONIEN INDÉPENDANT n°55
La nicotinothérapie :
Nous nous sommes engagés dans une action pour faire reconnaître et diffuser la Nicotinothérapie. En effet, nous en avions parlé dans le précédent numéro, cette pratique thérapeutique est en œuvre depuis plus de dix ans (cf. le numéro 3 du P. I. de mars 2001) et elle apporte de réels progrès pour les « rares élus » qui en bénéficient. Malheureusement elle demeure très discrète, voire clandestine, et pratiquée dans un seul lieu sous la direction du docteur Villafane au CHU Henri Mondor à Créteil.
Pourquoi cette absence de diffusion ? C’est toute la question que nous nous posons : pourquoi une pratique thérapeutique, dont les résultats semblent permettre de réduire considérablement la consommation médicamenteuse, ne bénéficie-t-elle pas d’une AMM (Autorisation de Mise sur le Marché) pour les patchs de nicotine ?
A cela plusieurs réponses et pistes de réflexions : « Tout d’abord, elle n’est pas politiquement correcte. Le message autour de la nicotine est complexe. D’un côté, on connaît les dégâts du tabac, de l’autre, on veut faire entendre que la nicotine peut être un médicament… Il ne s’agit pas de fumer, la cigarette est un danger. La nicotine à l’état pur n’est pas dangereuse. Elle est un neuro-modulateur des neurones du système nerveux central. Un neurotransmetteur qui intervient au niveau de la synapse neuronale, des récepteurs de la dopamine », explique le docteur Villafane dans une interview au journal Sud-ouest.
Mais peut-être y a‑t-il une réponse plus prosaïque : les intérêts financiers en jeu tant des laboratoires pharmaceutiques que des équipes chirurgicales engagées dans la Neurostimulation Cérébrale Profonde (NCP) ? C’est en toute connaissance des conséquences de nos propos que nous évoquons cette interrogation : il y va d’économie substantielle pour les régimes d’assurance médicale !
Certes, tous les patients ne sont pas concernés par cette pratique mais, pour les malades susceptibles d’en bénéficier, il s’agit là d’une thérapie non agressive qui réduit les risques de dyskinésies bien connues liées à la L‑dopa.
Le bilan du fond de Recherche CECAP :
Nos deux boursières de cette année nous présentent leur bilan certes un peu ardu à la lecture mais ô combien optimiste pour l’avenir des recherches sur la maladie ! Vos dons permettent des avancées modestes certes mais importantes pour la connaissance de notre partenaire imposé&nbnsp;: Parkinson.
Témoignage :
Et puis, un témoignage bouleversant que nous avons voulu vous présenter pour dire à nos accompagnants, quand nous en avons ( !), combien leur rôle est important pour nous les patients et mérite d’être valorisé y compris par les Pouvoirs Publics car ils représentent une économie, là aussi, substantielle pour la collectivité !
Permettez-moi, enfin, de vous souhaiter tous mes vœux de bonheur et de santé pour cette nouvelle année 2014 !
Jean GRAVELEAU graveleau.jean2@orange.fr
56 — association de parkinsoniens du Morbihan
Publié le 26 novembre 2013 à 07:35Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Pour clôturer le deuxième trimestre :
10 Juin, la Conférence de Territoire n°3, nous invitait à débattre sur la méthodologie de mise en œuvre des actions du Plan Territorial de Santé (PTS) sur la thématique « Handicap ».
17 Juin, réunion avec le groupe de travail de l’ARS de Rennes, sur la « Bientraitance et la lutte contre la maltraitance » dans les services et établissements sociaux et médico-sociaux.
18 juin, réunion au Centre Socioculturel de Ménimur pour faire le point sur les échanges avec la direction et les Associations, et prévoir les activités pour l’année 2013/2014.
Début juillet, nous assistons à la présentation de la plate-forme d’information et de coordination du Territoire Gérontologique Vannetais au niveau départemental pour 2011/2015.
Le temps des vacances s’achève, il faut penser à reprendre nos activités. Déjà deux rencontres prévues fin Août, une avec la municipalité pour la mise en place du Forum des Associations qui aura lieu le 7 Septembre, l’autre avec le Centre Socioculturel de Ménimur pour la journée « porte ouverte » du 11 Septembre.
Plusieurs interventions prévues en septembre et octobre durant la Semaine Bleue.
Début octobre, nous assisterons aux Assemblées Générales AGP & CECAP dans la Manche.
Françoise Vignon,
secrétaire ADPM
35 — association de parkinsoniens d’Ille et Vilaine
Publié le 23 novembre 2013 à 09:46Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Tout d’abord, quelques nouvelles du périple de notre Président.
Après 62 jours de marche du 26 mars au 28 mai, après avoir parcouru 1 700 km à raison de 27 km en moyenne journalière, effectué 2 400 000 pas, Yves nous est revenu de Compostelle.
Son périple a été salué par plus de 8 000 internautes et son action aura rapporté près de 8 500 euros pour la Recherche, dont une partie pour CECAP Recherche et une partie pour l’INCR (Institut des Neurosciences Cliniques de Rennes) du Professeur Vérin et chercheurs associés.
Par cette action, Yves a surtout voulu démontrer que la marche était une excellente thérapie.
Il remercie celles et ceux qui lui ont apporté du soutien.
Sortie annuelle : Avant de vous donner des nouvelles de notre activité, il est agréable de conter notre sortie annuelle. Celle-ci a eu lieu à Saint Coulomb, commune voisine de Saint-Malo en Ille-et-Vilaine. Les mérites de cette organisation reviennent à François, Bernard, Arlette, Bernadette. Nous avions programmé la visite d’une Malouinière.
Il s’agit d’une maison de maître créée au XVIIIe siècle par un riche armateur de la Compagnie des Indes. Ces riches négociants ont bâti à l’époque de Louis XIV ces hôtels particuliers et résidences nommées Malouinières, une centaine dans la région de Saint-Malo.
L’histoire nous dit que ces armateurs étaient aussi riches que Louis XIV, car l’aventure maritime enrichissait les corsaires, les prises étant partagées entre le Roi Soleil, l’armateur et l’équipage.
Et quant on est aussi riche que le roi, on s’expose à des récriminations, ce qui adviendra pendant la Révolution où, si les biens immobiliers résistèrent, le mobilier fut disséminé.
La Malouinière fut restaurée au siècle dernier et les propriétaires mirent l’essentiel de leur fortune dans la rénovation de la maison de maître, son pigeonnier, sa chapelle, ses jardins, et surtout par l’acquisition de plusieurs centaines de pièces de vaisselle d’époque ainsi qu’un papier peint panoramique du XVIIIe siècle qui demanda trois années de travail de rénovation.
La journée se termina après un excellent repas pris en bord de mer.
Nos activités perdurent, chaque mois nous effectuons nos journées rencontres dans chaque territoire de notre département, nous présentons la MP dans les écoles de santé, et participons à des forums de santé.
Le dernier en date a eu lieu dans le pays de Brocéliande, à l’initiative de Bernard et de François et réuni plus de cinquante participants.
Bernard MARCHAND, vice-président.
29 — association de parkinsoniens du Finistère
Publié le 22 novembre 2013 à 08:07Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Repas à l’auberge-expo du Youdig à Brennilis
Nous étions 77 personnes à nous rassembler pour notre repas annuel de l’association à l’auberge du Youdig où nous attendait un copieux plat du terroir « un Kig-ha-farz ». Kir, soupe au pain, kig (cochon en breton) !! Puis fars aux pruneaux et gâteaux au beurre pour clore le repas, le tout bien sûr accompagné de cidre local. Après une démonstration de gavotte des montagnes noires, nous étions invités à visiter le musée du Youdig, commentée par la mythique patronne des lieux.
Ce musée abrite un village miniature en schiste un chef d’œuvre!!! Celui d’Annick Le Lann. Bâti ardoise par ardoise, il représente les scènes de la vie du XVIème siècle dans cette Bretagne de légendes, retraçant l’histoire du hameau du YOUDIG, ainsi qu’une collection de costumes et matériels d’époques.
Rappels :
Assemblée Général CECAP 2014 : Prévoyez les vacances fin septembre 2014 en Finistère dont les dates seront communiquées prochainement.
Prenez bien soin de vous !
Dominique Bonne ‑président de l’Association Parkinsoniens du Finistère
22 — association des Parkinsoniens des Côtes d’Armor
Publié le 14 novembre 2013 à 09:13Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
L’été se termine avec chez nous une aggravation de l’état de santé de bon nombre de nos adhérents, nous nous demandons si c’est le cas dans les autres départements ?
Avant l’été, le 27 Juin, nous avons organisé à Trégueux une réunion d’information sur la prise en charge de personnes atteintes de la maladie de parkinson par l’hôpital de jour des Châtelets dans la région de Saint-Brieuc. 6O personnes étaient présentes et le docteur Baronnat, responsable de ce service, a pu apporter toutes les précisions.
Le 27 Juillet, à l’initiative de notre secrétaire-adjointe Jeanine Filbing, nous avons pu bénéficier d’une deuxième séance de chant védique, les adhérents présents étaient très satisfaits de cette prestation.
A la rentrée, le 7 Septembre, nous serons présents au forum des associations sur 5 sites : Lanvollon, Lannion, Penvenan, Paimpol, Trégueux.
Les cours de gymnastique adaptée vont reprendre à Lannion, Paimpol et Trégueux, une fois par semaine, ainsi que les séances de piscine en eau de mer 2 fois par mois au Centre héliomarin de Trestel.
Une nouveauté à la rentrée, des séances de yoga du rire destinées plus particulièrement aux aidants, sont prévues à Guingamp ; 5 séances sont programmées avant la fin de l’année.
Les ateliers et groupes de paroles destinés aux personnes atteintes de la maladie de parkinson et aux aidants vont se poursuivre à Paimpol et démarrer à Trégueux. Ce programme qui s’achève en 2013 s’est déroulé sur 3 ans. Ensuite, il faudra rechercher des financements. Il s’avère en effet que le quotidien est très dur à vivre et que ces échanges en présence de professionnels de santé nous sont devenus complètement indispensables.
En ce qui concerne ce programme, nous organisons avec l’appui du Conseil Général, par l’intermédiaire du Clic, une réunion d’information le mercredi 11 Septembre à 15 H salle Ispaïa 4, Rue Camille Guérin à Ploufragan.
Nous avons toujours le projet d’expérimenter le Qi Gong sur 10 séances, le dossier est en cours.
Nous serons heureux de vous retrouver le mardi 1er octobre et mercredi 2 octobre lors de l’assemblée générale du CECAP à Hauteville sur Mer.
A très bientôt
Joëlle Guenanen : guenanen.joelle@orange.fr
Témoignage de B Dupont
Publié le 13 novembre 2013 à 14:17Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
L’éditorial de Jean Graveleau, dans le numéro 53 du « Parkinsonien Indépendant », m’a fait réagir « positivement » et voici le message que je lui avais adressé :
« Merci Jean pour la force de ton édito ; j’approuve entièrement car je constate sur moi-même les bienfaits de mes 20mn. de gym. Journalière (parkinsonien depuis 15 ans). Pour info, je peux également témoigner des bienfaits remarquables de la réflexologie du cerveau que me fait mon kiné ; j’en suis à ma 23ème séance (1 séance toutes les 3 semaines). Je vis « presque normalement » et participe encore à des activités communautaires ».
Jean : « Merci sincèrement de tes félicitations : ça fait beaucoup de bien ! Si tu veux présenter ton expérience, je pourrais trouver de la place dans un prochain numéro ».
Sa réponse a été généreuse, mais une expression devrait tous nous interpeller : « ça fait beaucoup de bien »… Ne devrions-nous pas communiquer davantage avec celui qui nous informe si régulièrement, si pertinemment et si bien ?
Sans vouloir attirer l’attention sur moi, je détaillerai cependant ce qui fait mon quotidien :
CHAQUE JOUR : 20 à 30mn de sport (vélo d’intérieur, tapis de marche ou marche scandinave, mouvements de coordination des bras, réveil de la voix).
CHAQUE SEMAINE : une séance d’orthophonie + une séance de kiné et 2 fois par semaine, yoga et atelier vocal adapté, au sein de notre association. A tout cela s’ajoute, évidemment, un suivi médical avec neurologue et médecin homéopathe.
J’insiste beaucoup sur la réflexologie du cerveau : pratiquée par mon kiné (qui a fait l’objet d’un article du Parkinsonien Indépendant n°49 pages 13 et 14).
Je ne peux pas affirmer que cette technique soit bénéfique à tous les parkinsoniens. Dans mon cas, ça marche !!! Après environ 5 séances (1 séance toutes les 3 semaines), j’ai perçu une amélioration indéfinissable…! Après 23 séances, je suis à nouveau participant de plain-pied (mais modérée), de mes activités antérieures.
Vous comprendrez pourquoi, je tiens à vous faire partager ce qui n’est qu’un chemin d’espoir mais, malgré tout, une réalité ; car la maladie est et sera toujours là : j’essaie d’être le plus fort…! Je suis soutenu et compris par mon épouse, mes enfants, petits enfants, nos amis et connaissances, et cela est, pour beaucoup, dans ma volonté de me « battre » ; mais, sans les séances de CERVIOREFLEXOLOGIE, je n’en serais pas là de ce bien-être retrouvé. Cela je l’affirme très fort !
Je terminerai en empruntant la conclusion de Jean Graveleau : « Luttons, bougeons-nous pour être des Parkinsoniens indépendants ». Se prendre en « main » dès le début de la maladie, augmente les chances de dominer la maladie.
Bon courage à tous
Bernard Dupont bernard.dupont56530@orange.fr
« Un sourire de marbre »
Publié le 08 novembre 2013 à 08:26Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Lu dans le Parkinson Suisse n°108 – décembre 2012
C’était une journée d’automne comme tout le monde les aime : au bord du lac, un soleil doux révélait de luxuriantes couleurs dans les châtaigniers et réchauffait jusqu’aux tréfonds de l’âme. Mon épouse et moi-même étions en croisière sur le lac de Zurich. A côté de nous, une famille admirait également les ondes bleues et profitait de la traversée jusqu’à Rapperswil. Dans une poussette, leur plus jeune enfant, surveillé par sa sœur à peine plus âgée. Je remarquai qu’elle me dévisageait et se moquait de moi.
Elle finit par demander à son père, à mi-voix : « Papa, c’est un méchant monsieur ? »
La brise me souffla sa question.
Elle n’était pas du goût du père, qui répondit : « Ah non, absolument pas ! » Il s’agissait probablement de la réaction à un avertissement contre les méchants et les monstres. Pourquoi cette petite m’avait-elle classé dans cette catégorie ? Je le compris rapidement ! Les enfants sont de très fins observateurs. Pour moi, il était grand temps de prendre mon médicament antiparkinsonien. Sacrebleu ! Mon visage était de nouveau impassible et figé. Il ne m’autorisait aucune mimique, je ne pouvais plus articuler ni même siffler. Dans ces conditions, comment provoquer le sourire d’un enfant ?
La fillette tâcha d’user de son charme à plusieurs reprises, mais mon sourire restait masqué, comme le coucher de soleil derrière un orage. Pourtant, elle ne s’avoua pas vaincu. Au bout d’un moment, elle saisit l’appareil numérique de son père, se planta devant moi et me prit en ligne de mire, sans appuyer sur le déclencheur. Le père s’excusa pour son geste. « Tu n’as pas le droit de prendre des inconnus en photos sans leur demander la permission ! » La situation était vraiment très étrange. Les commissures de mes lèvres se soulevèrent quelque peu. Satisfaite, la petite reposa l’appareil sur la table, se consacra à nouveau à ses parents et à son petit frère, en m’envoyant de temps à autres un sourire avenant.
Lu par Jean Graveleau
graveleau.jean2@orange.fr
De nouvelles preuves au lourd dossier des pesticides — Le Roundup® : un herbicide qui nous empoisonne
Publié le 04 novembre 2013 à 13:11Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
De nouvelles preuves au lourd dossier des pesticides
Les résultats de la vaste étude publiée en juin par l’INSERM, pulvérisent les arguments encore fréquemment employés par les industriels pour nier l’implication des pesticides dans l’augmentation du nombre de cas de maladies graves. Un SOS lancé aux politiques.
L’INSERM, le 13 juin, a publié le résultat sans appel de ses recherches sur le lien entre pathologies et exposition aux pesticides. Cette étude appelle à des nouveaux travaux notamment sur les « effets cocktails » des molécules aujourd’hui utilisées massivement par l’agriculture conventionnelle. Elle conclut, en rassemblant des données issues de nombreux pays, à la responsabilité des pesticides dans une augmentation « significative » des cancers, maladies du sang, troubles neurologiques et malformations.
Sans surprise, le risque de ces maladies est accru chez les agriculteurs et personnes résidant à proximité des zones agricoles, c’est-à-dire 15% de la population française. Un seul exemple tiré de cette étude, que l’on espère voir suivie d’une réaction des plus verts (sinon des plus courageux) de nos politiques : en Gironde, une région viticole très touchée par les pesticides, l’incidence des tumeurs du système nerveux est trois fois plus importante que sur l’ensemble du territoire. Et cette incidence a augmenté de 17% entre 2000 et 2007… De quoi au moins clore le bec aux industriels qui nient ces implications depuis des décennies.
Le Roundup® : un herbicide qui nous empoisonne
Trois Français sur dix présenteraient dans leurs urines des traces de « glyphosate® » herbicide le plus utilisé dans le monde. Tests menés dans 17 autres pays européens qui montrent que 44% des échantillons d’urine analysés contiennent des traces de glyphosate®. C’est la première fois qu’un tel test est mené en Europe pour détecter la présence dans le corps humain de ce désherbant, commercialisé principalement par Monsanto. Ce produit est utilisé par les agriculteurs, les collectivités locales et les jardiniers. Sa présence dans les denrées alimentaires ou dans l’eau est rarement contrôlée par les autorités gouvernementales. Alarmant au regard des résultats de l’étude réalisée l’an dernier par le professeur Séralini.
Articles relevés dans le magasine Bio Info de juillet
Par Soize Vignon
soize.vignon@orange.fr
Comment ne pas craquer quand on est aidant ?
Publié le 02 novembre 2013 à 10:36Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Voulant tout assumer seuls, les aidants se retrouvent au fil du temps épuisés, prêts à craquer. Pour éviter cette situation, il est capital de connaître ses propres limites et d’accepter de se faire aider…
La situation des aidants n’est pas simple. Si tout semble possible au début, les choses se compliquent ensuite. Entre amour, culpabilité et souffrance, on se fatigue nerveusement, puis physiquement et l’on ressent fréquemment un sentiment d’impuissance : « Je n’arrive pas à faire tout ce que je voudrais pour aider mon mari, ma femme ». Il faut réagir dès les premiers signaux d’alerte : quand on commence à mal dormir, à devenir irritable, à se sentir en échec ou isolé(e). Il faut savoir prendre du recul et envisager des solutions pour lâcher prise. Il devient capital de se ménager des temps de répit.
En s’appuyant sur des aides extérieures (malheureusement trop peu nombreuses par rapport aux demandes), l’aidant devient plus disponible pour la personne aidée, parce que moins fatigué, épaulé et souvent tranquillisé par cette présence, ou cette prise en charge par un organisme.
Françoise Vignon
soize.vignon@orange.fr
La Levodopa Equivalent Dose (LED), ou comment déterminer la L‑dopa reçue par le malade
Publié le 29 octobre 2013 à 07:26Article paru dans LE PARKINSONIEN INDÉPENDANT n°54ü
Par Claire Smith
Les traitements médicamenteux de la MPI ont pour but de compenser le déficit dopaminergique au niveau du striatum, en administrant :
- soit un précurseur de la dopamine,
- soit un agoniste dopaminergique
- ou bien en inhibant les métabolismes de la dopamine MAO‑B et COMT.
Dans un article paru dans Le Parkinsonien Indépendant n°53 de Juillet 2013, des conseils d’utilisation des différents médicaments antiparkinsoniens sont donnés aux patients. (Dossier réalisé par l’Agence Nationale de Sécurité du Médicament et des Produits de Santé).
Pour établir la prescription, le neurologue va choisir parmi une panoplie d’une quinzaine de médicaments ceux qui correspondent le mieux au traitement des troubles du patient. Puis, il lui faudra doser chaque médicament, et déterminer l’efficacité globale du traitement. Au final, l’ordonnance journalière se présente comme une liste de plusieurs médicaments (de 3 à 5) très souvent à libération immédiate, mais parfois à libération prolongée (LP) avec des dosages de plus en plus variés. Il devient alors peu évident de comparer l’efficacité de deux traitements ou de prévoir la substitution d’un médicament par un autre. C’est ici qu’intervient la notion de LED (Levodopa Equivalent Dose). C’est le sujet de l’article qui suit, rédigé à partir de comptes-rendus de travaux réalisés à l’Université de Birmingham (UK) et publiés par Claire Smith.
Définition de la LED :
La LED d’un médicament est définie comme la quantité de ce médicament qui a le même effet antiparkinsonien que 100 mg de Lévodopa à libération immédiate.
Quelques exemples :
- Led d’un comprimé de Sinemet 100 mg : 100 mg
- Led d’un comprimé de Sinemet LP 100 mg : 133 mg. La version LP est moins efficace de 25% que la version à libération immédiate.
- Led d’un comprimé de Requip 5 mg : 100 mg
- Led d’un comprimé de Requip 8mg : 160 mg
Sur le premier exemple, on voit que, à dose égale, la version LP est moins efficace que la version LI (-25%).
Sur le deuxième exemple, à libération identique, l’effet est proportionnel à la dose.
Les travaux de l’Université de Birmingham :
Il s’agit de travaux de collecte et de traitement de données sur l’ensemble des médicaments antiparkinsoniens sur le marché, jusqu’en 2009.
La démarche suivie consiste tout d’abord, à collecter, à partir de mots clés « levodopa » et « equivalency », toute information de 1980 à 2009 sur l’efficacité des antiparkinsoniens, et cela pour tous les types d’études publiées en anglais. Les données ont fait ensuite l’objet de traitements statistiques (mean et mode), pour aboutir à l’obtention de Led pour tous les antiparkinsoniens.
L’étude a fourni les résultats suivants en Led, exprimés en mg, pour une quinzaine de médicaments antiparkinsoniens. Alors que les auteurs désignent chaque médicament, par le nom de sa molécule (Pramipexole, Ropinirole etc..), nous avons volontairement conservé les dénominations commerciales (Sifrol®, Requip® etc..) plus familières à nos lecteurs :
Médicaments à base de Levodopa :
- Sinemet 100 à libération immédiate 100 mg
- Sinemet 100 à libération prolongée LP 133 mg
- Modopar 125 à libération immédiate 100 mg
- Duodopa 90 mg
Agonistes dopaminergiques :
- Sifrol 1mg
- Requip 5mg
- Neupro 3,3mg
- Trivastal 100mg
- Parlodel 10mg
- Célance 1mg
- Dopergine 1mg
Inhibiteurs :
- Deprenyl 10mg
- Otracel 1,25mg
- Azilect 1mg
Utilisation de la Led :
Désormais, on connait la Led de chacun des médicaments composant une ordonnance journalière. On peut alors calculer la dose globale journalière. Soit une ordonnance comprenant :
- 3 comprimés de Sinemet à 100 mg, soit : 100/100 X 300 = 300 mg
- 1 comprimé de Sinemet LP à 100 mg, soit : 100/133 X 100 = 75mg
- 1 comprimé de Azilect 1 mgsoit : 1/1 X 100 = 100 mg
- 1 comprimé de Requip à 8 mg, soit : 8/5 X 100 = 160 mg
Soit un total d’équivalent Levodopa par jour de : 635 mg
Il s’agit d’une dose journalière plutôt moyenne. Cette dose peut excéder 1 000, voire 1 500.
Les valeurs fournies par Claire Smith sont commentées et parfois contestées dans la revue NeuroTalk, sans que soit remis en cause le principe de la LED.
Bibliographie :
— Levodopa Dose Equivalency par Claire Smith du Clinical Trials Unit de l’Université de Birmingham (UK).
— Levodopa Dose Equivalency dans la revue NeuroTalk
Traduit et transmis par Jean Pierre Lagadec
jpmo5@orange.fr
Changement de formule pour le Sinemet®
Publié le 23 octobre 2013 à 08:49Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Les comprimés à libération immédiate de SINEMET 100mg/10mg et de SINEMET 250mg/25mg, sont désormais ronds, bleu clair tacheté et non sécables.
Les codes CIP ne sont pas modifiés.
Sécabilité impossible
La perte de la barre de sécabilité rend impossible l’utilisation de demi-doses, c’est-à-dire des doses à 50mg/5mg ou 125mg/12,5mg de lévodopa/carbidopa.
Dans le cas où ces posologies sont recommandées, le laboratoire oriente les professionnels de santé vers une formulation commercialisée de lévodopa/carbidopa 250mg/25mg ou 100mg/10mg en comprimés sécables.
Info de David Paitraud journaliste médical de VIDAL new Officine du 16 Mai 2013
Traitement à base de patch de nicotine : où en est-on ?
Publié le 12 octobre 2013 à 14:58Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Une fois n’est pas coutume, il me semble important de donner une publicité à un traitement qui semble très prometteur. Et pourtant, il demeure confidentiel sauf sur notre site de référence GP29, pour ne pas le citer, où un véritable « buzz » explose et dénonce une réticence réelle à mettre en œuvre les moyens d’une reconnaissance officielle des bienfaits (ou des limites !) de cette thérapie.
Depuis la parution d’un article du Nouvel Observateur du 22/28 janvier 2009, de la réponse du professeur Pierre Cesaro et des réserves du professeur Ludin (lu dans le Parkinson Suisse N°58 de juin 2000) – cf. le Parkinsonien Indépendant N°36 mars 2009 – de nombreux témoignages s’expriment sur notre site. Ils réclament une prise en compte des résultats indubitables, à leur dire, et sur le « mieux-être » qu’ils ressentent ainsi que la réduction des quantités de médicaments ingurgités.
Je m’étais, à l’époque, permis d’exprimer les réserves d’usage en la matière : « Attendons donc les résultats contrôlés des recherches en cours et menées par des équipes qui, nous l’espérons, ne sont pas subventionnées par les fabricants de tabac, avant de nous dire que cette voie est véritablement porteuse d’espoir. Soyons patients et ne nous laissons pas emporter par notre envie, normale, de trouver la solution miracle ! »
Mais aujourd’hui, plus de quatre années se sont écoulées et nous ne pouvons pas rester indifférents à l’absence de volonté officielle de répondre à l’attente de tous ces malades et de leur famille qui attendent une réponse claire… !
Je ne voudrais pas paraître ni mauvaise langue ni saugrenu : mais n’y aurait-il pas quelques pressions, même indirectes, des « lobbys de la L‑dopa et du traitement par la Stimulation Cérébrale Profonde » ?
Nous aurions pourtant là un moyen de réduire les dépenses de l’Assurance Maladie et de repousser un peu plus loin la fin de vie désastreuse qui nous attend inéluctablement si nous prolongeons trop loin et trop fort le traitement actuel (dyskinésie, blocages, etc…).
Nos associations pourraient peut-être se mobiliser et interpeller les Pouvoirs Publics. Elles ont bien su le faire pour le Livre Blanc en le portant à bout de bras et même en pétitionnant pour sa reconnaissance !
Il me semble judicieux de se lancer dans la bagarre pour faire reconnaître une thérapie douce pour le patient, améliorant le poids des médicaments et, aussi, économe des fonds publics… Nous pourrions écrire à Madame le Ministre comme le suggère un commentaire du site.
Quelques témoignages :
Je viens de relire les commentaires, suite à l’article de Mars 2009 sur la Nicotinothérapie, paru sur GP29. J’ai trouvé 56 commentaires, depuis la parution de l’article, et depuis quelque temps il y en a de plus en plus. La Nicotinothérapie est de loin le sujet qui semble actuellement intéresser le plus les lecteurs de GP29 ! Il y a beaucoup de demandes d’information, et aussi beaucoup de commentaires positifs, aussi bien sur la thérapie que sur le docteur Villafane. Je n’ai pas trouvé d’avis négatif. Dommage que cette thérapie ne soit pas agréée !
Commentaire by Jean Pierre Lagadec — 27 juin 2011
Bonsoir,
De retour de Paris où j’ai vu le Docteur Villafane pour mon suivi, je veux témoigner une nouvelle fois des bienfaits que m’a apportés la nicotine. Parkinsonienne « officielle » depuis le 11 décembre 2008, je n’ai toujours pas eu besoin de recourir à la L‑dopa et pourtant.
Pourtant, l’année 2012 a été une année très éprouvante puisque du 23 janvier 2012 au 30 avril, j’ai eu à soutenir mon époux hospitalisé d’abord 6 semaines en réanimation, puis …etc… Sans les patchs de nicotine, je n’aurais jamais eu l’énergie nécessaire à un tel parcours.
Avant de commencer ce traitement en septembre 2011 grâce au docteur Villafane, j’avais besoin de 2 à 3 heures de sieste chaque jour ou presque. Là, je reviens d’un A/R Toulouse-Paris effectué seule avec des conditions climatiques rudes, et j’ai tenu le choc malgré un trajet aller en TGV rallongé à cause de la neige, malgré un arrêt à Marne la Vallée suivi d’un trajet en RER incertain jusqu’à Paris…
Toute cette résistance retrouvée, je la dois, sans doute aucun à la nicotine et au docteur Villafane qui m’accompagne dans sa prescription. J’oubliais de dire qu’avant d’entreprendre cet A/R, j’avais déménagé et de ce fait, loin de me reposer, j’avais fait puis défait quelques cartons… ! Alors, je souhaite à ceux qui hésitent encore de se décider à franchir le pas.
Je ne suis pas sûre que ce traitement me guérisse : je suis certaine par contre qu’il m’a redonné un confort de vie inestimable et c’est déjà fabuleux ! Et cela, sans avoir à recourir à une intervention du cerveau pour le moins complexe, malgré toutes les louanges prodiguées par certaine association.
Merci docteur Villafane ! Merci pour ces mois de vie retrouvée, et plus peut-être, sans risque aucun. Tenez bon malgré toutes les difficultés semées sur votre route : nous avons plus que jamais besoin de vous ! En souhaitant très vivement que vous soyez reconnu officiellement le plus tôt possible afin que cette thérapie puisse être mise en œuvre ailleurs qu’à Paris.
Commentaire by Marie-Paule Subarroque — 22 janvier 2013
Bonjour
Pour l’amélioration des symptômes, je ne peux parler que de mon cas. Si vous êtes ancien fumeur, les récepteurs nicotiniques s’ouvrent plus vite. J’ai commencé la nicotinothérapie depuis 3 ans avec des doses de nicotine allant de 2,5 mg jusqu’à 65 mg pendant une courte période. Je suis resté à 42 mg/jour pendant deux ans, puis 16 a17 mg de nicotine/jour me suffisent actuellement, et je continue de m’améliorer. Je suis passé de 600 mg de dopa à 500 voire 450 mg par jour (Sinemet®, Stalevo®) en 3 ans. Pour moi au bout de 6 à 8 mois j’ai senti une amélioration.
Le plus spectaculaire çà a été au début, un visage moins crispé, plus du tout les yeux hagards au lever. J’ai ressenti moins de fatigue, moins de crispation. Ma famille autour de moi dit que j’ai fait de gros progrès. Actuellement je calcule mes doses de nicotine au milligramme prés, car un surplus de nicotine crispe.
Quand l’équilibre est atteint, on revit. Je peux affirmer ici, après 3 ans de recul, que la nicotine ça marche et depuis mon état, mes crispations se sont améliorées. Avant que je prenne de la nicotine j’étais passé de 300mg de dopa a 600mg, mon état se dégradait.
Commentaire by Yves Auberdiac — 7 juillet 2013
L’article en question
Les commentaires
Sources :
Le site de nos amis du Finistère : http://gp29.org
Le site de référence sur la nicotine : http://www.google.com/patents/EP1212060A1?cl=fr
Rédigé par jean Graveleau
graveleau.jean2@orange.fr
Quand les parkinsoniens maigrissent sans le vouloir
Publié le 10 octobre 2013 à 09:00Article paru dans LE PARKINSONIEN INDÉPENDANT n°54
Lu dans le Parkinson Suisse N° 109 – mars 2013
Contrairement aux « jeunes » séniors qui prennent trop de poids, les parkinsoniens risquent de maigrir involontairement, voire ne plus avoir que la peau sur les os. L’alimentation n’est pas toujours responsable.
De nombreuses raisons peuvent expliquer la dénutrition des individus avec l’âge. L’odorat et le goût faiblissent, l’appétit disparaît – parfois en raison du vieillissement, parfois à cause d’un effet secondaire médicamenteux. La capacité gastrique réduite avec l’âge, l’activité accrue des hormones de satiété et les éventuels problèmes de déglutition et de mastication jouent également un rôle.
Les raisons de la cachexie en cas de Parkinson
Chez les parkinsoniens, d’autres facteurs s’ajoutent à ces problèmes « normaux » avec l’âge. En conséquence, un patient sur cinq répond à la définition de la cachexie (perte involontaire de plus de 5% du poids corporel en six mois). Souvent, l’odorat et le goût sont altérés avant l’apparition des premiers symptômes moteurs. Les tremblements demandent beaucoup d’énergie et certains antiparkinsoniens peuvent (la plupart du temps, temporairement) provoquer de fortes nausées allant jusqu’aux vomissements. Au détriment de l’observance thérapeutique et du poids.
Certains patients doivent en outre séparer les repas riches en protéines de la prise de médicament car la résorption de la L‑dopa administrée par voix orale entre en concurrence avec celle des protéines alimentaires dans l’intestin. Chaque jour, les patients prennent jusqu’à cinq fois leurs médicaments et n’ont plus le temps de manger.
Si des complications thérapeutiques (phases off, dyskinésies) et des symptômes non moteurs tels que les troubles de la vidange gastrique, la constipation et les lourdeurs d’estomac, les troubles de la déglutition ou l’hypersiallorrhée accompagnent la progression de la maladie, une rapide perte de poids peut en résulter.
Actions possibles
Tout d’abord, l’alimentation doit bien sûr être adaptée aux besoins du patient : collations plus fréquentes, en-cas énergétiques, apport suffisant en liquide et présentation appétissante, sans oublier le calme en mangeant, sont essentiels. Si des symptômes moteurs gênent considérablement la prise de nourriture, des aides (couverts, bord d’assiette rehaussé) peuvent s’avérer utiles.
En cas de troubles de la déglutition, un logopédiste doit absolument être consulté et le cas échéant, la consistance des aliments doit être adaptée. Bien sûr, les éventuelles prothèses dentaires doivent être correctement et solidement fixées. Dans les cas très grave, une alimentation artificielle peut également s’avérer inévitable.
Source : Medical tribune, 12 2012
Lu par Jean Graveleau
graveleau.jean2@orange.fr
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.
