réunion d’information sur la NEPT, organisée par les Asso ADPM (56) et A2N
Publié le 03 septembre 2016 à 12:20
pétition pour une Prise en Charge de la Nicotinothérapie
Publié le 29 août 2016 à 15:27Atteint depuis 4 ans de la maladie de Parkinson (61 ans aujourd’hui), voici une pétition pour une Prise en Charge de la Nicotinothérapie dans la Maladie de Parkinson et bien d’autres pathologies …
pour signer la pétition, cliquez ici…
[vu sur le net] — Parkinson : un test de vision pour dépister la maladie ?
Publié le 23 août 2016 à 11:50Article trouvé sur le site de Metronews
Des chercheurs ont mis au point un examen permettant d’identifier, dans les yeux, des signes précurseurs de la maladie de Parkinson.
Certains changements peuvent être observés dans la rétine.
pour lire cet article dans son intégralité, suivez ce lien…
Communication de l’Unité Parkinson d’Ydes (UPY)
Publié le 22 août 2016 à 08:42Nous avons reçu une communication de l’Unité Parkinson d’Ydes (UPY), à laquelle nous avions consacré cet article
C’est avec grand plaisir, que je vous invite à la troisième Journée Portes Ouvertes de l’Unité Parkinson d’Ydes dans le Cantal.
Fort de notre expérimentation, l’Unité Parkinson accueille depuis Avril 2012 des patients, de toute la France, atteints de la Maladie de Parkinson et syndromes apparentés en Hébergement Temporaire ou Permanent dans une prise en charge adaptée et spécifique.
Le mois de Septembre est un mois charnière puisque nous sommes dans l’attente de l’autorisation d’activité par la nouvelle ARS Auvergne Rhône Alpes.
C’est en tout cas ce que nous souhaitons dans l’espoir de continuer notre démarche auprès des malades et de leurs familles et de voir un jour cette initiative se multiplier ailleurs en France.
Venez nombreux soutenir et découvrir l’Unité Parkinson lors de notre 3ème Journée Portes Ouvertes, le Mercredi 14 Septembre 2016 à 14h00 à l’Unité Parkinson d’Ydes.
l’Unité Parkinson d’Ydes (UPY)est présentée sur le site de l’hôpital dont elle dépend
Communication de l’association A2N (association Neurothérapie et Nicotine)
Publié le 22 août 2016 à 08:33Suite à notre article du 29 juillet 2016 nous avons reçu cette ce message de A2N (association Neurothérapie et Nicotine)
Bonjour,
Beaucoup occupé par la situation actuelle de la NEPT (traitement par la Nicotine à l’Etat Pur par voie Transdermique) Je n’ai pas remarqué qu’une erreur sur mon N° de téléphone avait été reproduite. Les auteurs de l’article n’en sont pas responsables. Imprimé sur un millier de cartes de visite la correction n’a pu être complète !
Pour me joindre faites les N° suivants : 06 83 71 30 12 ou 02 99 62 38 17.Pour répondre aux demandes des uns et des autres quant à la réaction à avoir face à ces tentatives de suppression, sachez que nous travaillons ferme au sein de l’association A2N sur plusieurs fronts : courriers envoyés aux principaux décideurs (Martin HIRSCH, directeur général de l’AP-HP, Martine ORIO, directrice du CHU Henri Mondor, Pr A‑C BACHOUD-LEVY, chef du seervice neurologie, Pr Pilippe REMY, responsable du Centre Expert, Marisol TOURAINE, ministre de la santé…) D’autres types d’actions sont en cours de mise au point en direction des élus, de la presse… auxquels l’ensemble des personnes concernées pourront s’associer (patients, proches et toutes personnes n’acceptant pas les diktats de l’administration et des personnels médicaux qui combattent les découvertes du Dr Villafane sans prendre en compte les résultats obtenus sur le terrain.
Si vous avez des propositions d’interventions n’hésitez pas à les faire connaître.
DÉTERMINÉS et SOLIDAIRES.Auguste Pousset au nom d’A2N
La Plateforme de Répit et d’accompagnement vous propose un nouveau service
Publié le 19 août 2016 à 09:15Vous êtes domicilié (e) au sein ou à proximité des cantons de Pont-Croix et de Douarnenez ? Vous avez besoin de temps pour vous, pour rencontrer des membres de votre famille, réaliser une activité de loisir, culturelle ou de détente, faire des démarches administratives ou vous rendre à un RDV médical ?
La Plateforme de Répit et d’accompagnement vous propose un nouveau service qui permet de s’absenter en toute confiance pour avoir du temps pour vous. En partenariat avec un service d’aide à la personne, une auxiliaire de vie peut venir chez vous afin de prendre soin de votre proche et vous permettre ainsi de bénéficier de temps libéré.

[vu sur le net] — La maladie de Parkinson
Publié le 12 août 2016 à 10:58article trouvé sur le site du ministère des affaires sociales et de la santé
La maladie de Parkinson est une affection chronique neurodégénérative : c’est-à-dire qu’elle se caractérise par la disparition progressive de certains neurones dans le cerveau.
La conséquence principale de cette disparition neuronale est la diminution de la production de dopamine (une molécule qui permet aux neurones de communiquer entre eux), dans une région essentielle au contrôle des mouvements. De ce fait, la maladie de Parkinson est avant tout une maladie qui touche les fonctions motrices.
pour lire cet article dans son intégralité, suivez ce lien…
[vu sur le net] Ouverte depuis plus de deux ans, la structure assure une prise en charge de la maladie de Parkinson
Publié le 11 août 2016 à 10:08article trouvé sur le site de La Montagne
Ouverte depuis avril 2012, l’Unité Parkinson d’Ydes (UPY) a été la première structure d’hébergement et de soins pour personnes atteintes de la maladie de Parkinson, en France. Elle reste, aujourd’hui, très originale et innovante.
pour lire cet article dans son intégralité, suivez ce lien…
Menace sur la Nicotinothérapie
Publié le 22 juillet 2016 à 11:13Peut être étiez-vous à Plestin les Grèves au mois d’octobre dernier pour entendre le Dr. Villafane nous présenter ses travaux sur les traitements de la Maladie de Parkinson à partir de la Nicotine ? … Une des rares piste de recherche qui nourrit l’espoir, sinon de faire reculer la maladie, tout au moins d’en freiner l’évolution. Alors que déjà quelques 1300 patients ont opté pour cette thérapie, des décisions sont actuellement en cours à l’hôpital Henri Mondor, qui visent à l’abandon de ces travaux (voir courrier joint adressé à la direction de l’hôpital).
Si nous n’avons pas compétence pour en juger la pertinence, la manière dont elles sont prises est inacceptable. C’est pourquoi pour envisager des actions de soutien à venir, nous appelons les patients directement concernés par la nicotinothérapie à se faire connaître près de l’Association A2N dont voici les coordonnées :
- Jeanne (75) 01 45 33 29 73
- Michel (30) 04 66 33 06 42 / 02 31 92 24 37
- Auguste (35) 06 83 71 30 12 ou 02 99 62 38 17
e_mail : a2n@neuronicotine.eu
adresse postale :
A2N — neurothérapie et Nicotine
1, La Porte
35220 SAINT JEAN SUR VILAINE
Le Pr Benabid, as du Parkinson : le cerveau du cerveau !
Publié le 04 juillet 2016 à 11:27Article paru dans LE PARKINSONIEN INDÉPENDANT n°65
Prix Lasker en septembre 2014, « 2015 Breakthrough Prize » quelques semaines plus tard : couronné pour ses travaux portant sur la stimulation cérébrale profonde dans la maladie de Parkinson, le Grenoblois Alim-Louis Benabid franchit une nouvelle étape : l’illumination proche de l’infrarouge est testée dans la neuroprotection des neurones dopaminergiques.
Les travaux de l’équipe d’Alim-Louis Benabid sont maintenant bien connus : la stimulation cérébrale profonde permet d’obtenir une réduction considérable des symptômes moteurs (tremblements, akinésie, rigidité) de la maladie de Parkinson.
L’intervention se déroule chez le patient éveillé : introduction transcrânienne de fines électrodes jusque dans la zone cérébrale cible (noyau sous-thalamique). Dans ces électrodes, on fait passer un courant électrique de fréquence variable. Quand ces courants sont suffisamment élevés (aux alentours de 100 MHz), cela bloque l’activité de la cellule qu’on stimule et diminue considérablement les symptômes.
La recherche d’une neuroprotection
Il faut savoir que, lorsque les premiers signes de la maladie de Parkinson apparaissent, 70% des neurones dopaminergiques sont déjà détruits. Est-il possible d’obtenir une neuroprotection des 30% restants ? En collaboration avec l’équipe de l’Australien John Mitrofanis, le Pr Benabid (Clinatec, Grenoble) teste l’illumination proche de l’infrarouge (NIR).
Pourquoi ? Parce que la « photobiomodulation » par NIR possède des propriétés neuroprotectrices (amélioration de la fonction mitochondriale, augmentation de la synthèse d’ATP, activation de photo-accepteurs). Première phase : chez le rongeur. Les chercheurs ont montré, chez des souris MPTP, que le NIR protège les cellules dopaminergiques de la substance noire compacta, avec une amélioration de l’activité locomotrice.
Deuxième étape : chez le primate MPTP, la fibre étant introduite dans le fond du 3e ventricule et reliée à une fibre laser. On observe un effet positif comportemental qui semble corrélé au niveau histologique. L’essai chez l’homme (Clinatec, Grenoble) a pour but de voir si, en début de maladie, l’illumination NIR permet d’obtenir une neuroprotection des 30% de neurones encore vivants.
Dr Emmanuel de Viel
Pour en savoir plus :
http://www.clinatec.fr/le-professeur-benabid-lacademie-des-sciences/
Le Quotidien du Pharmacien 17.03.2016
Lu par Renée Dufant
L’Apomorphine (Apokinon®)
Publié le 02 juillet 2016 à 12:57Article paru dans LE PARKINSONIEN INDÉPENDANT n°65
Per Os ou Voie sous-cutanée :
La plupart des médicaments antiparkinsoniens sont présentés sous forme de comprimés que le patient prend par la bouche (per os), qu’il s’agisse de L‑Dopa, d’agonistes dopaminergiques, ou d’inhibiteurs. Un médicament per os a l’avantage de ne pas être invasif. Il est facile à conserver et à employer même en voyage.
Mais, avant d’arriver à son point d’action, le médicament doit transiter par le tube digestif (l’œsophage, l’estomac, le duodénum et l’intestin), où il est en concurrence avec les protéines de l’alimentation.
Les conséquences en sont (par exemple pour la L‑Dopa) une perte importante d’efficacité et des temps élevés de réponse (2 à 3 h pour la L Dopa). C’est pourquoi la médecine s’est ingéniée à rechercher des médicaments plus efficaces. Finalement le choix s’est porté sur l’Apomorphine, un puissant agoniste dont la dénomination commerciale est Apokinon®. Il sera utilisé après injection sous-cutanée.
Un revenant
Il s’agit d’un médicament très ancien découvert en 1870. Il a été utilisé pour ses qualités émétiques, puis en per os dans le traitement de la MPI jusqu’en 1967. C’est alors que furent redécouvertes et exploitées ses propriétés dopaminergiques. Utilisée par voie sous- cutanée, l’Apomorphine présente une structure moléculaire voisine de celle de la Dopamine et, tout comme elle stimule les récepteurs D1 et D2.
Ses caractéristiques pharmacocinétiques sont tout à fait étonnantes. Par exemple : la disponibilité par voie sous- cutanée est de 100% contre 2% per os avec une absorption complète et une concentration maximale atteinte en 8 minutes. La durée moyenne de vie est de 34 minutes.
De telles performances font que l’Apomorphine est devenue le médicament le plus efficace pour le traitement des cas difficiles, comme celui des phases off.
Pour injecter l’apomorphine au patient on dispose d’une pompe à Apomorphine, ou d’un stylo à Apomorphine Il n’y a pas d’accoutumance au produit, la dose restant fixe dans le temps. Pour éviter les vomissements, le patient est traité au Domperidone 2 à 3 jours avant l’injection. Enfin, rappelons que l’Apomorphine ne doit pas être confondue en raison d’une regrettable homonymie, avec la morphine.
La pompe à Apomorphine
Ses indications sont les suivantes : fluctuations importantes, troubles de la déglutition, attente de chirurgie. Le liquide à injecter (apomorphine diluée dans du sérum physiologique) est contenu dans une seringue de 20 ml. Cette seringue est actionnée par une mini-pompe portable et programmable.
La mise en service de la pompe est faite en milieu hospitalier (séjour de 10 jours environ). Pendant ce séjour, la pompe sera programmée selon les heures de la journée et de la nuit et selon les prescriptions du neurologue. L’injection peut se faire sur le tronc ou sur les membres. Il est conseillé de changer tous les 2 à 3 jours de point d’injection, afin d’éviter la formation de nécroses.
Le patient se familiarise avec la pompe, qu’il pourra utiliser seul, à sa sortie de l’hôpital. Si nnécessaire, il pourra faire appel à une infirmière ou à des sociétés de services qui livrent le matériel et les accessoires.
Le Stylo à Apomorphine.
Le patient pourra aussi disposer pour l’injection d’un appareil plus léger que la pompe. Avant utilisation, le patient aura appris à bien reconnaître les phases On et Off. Dès le début d’une phase Off, le patient ou son aide arme le ressort, pique en sous-cutanée (abdomen plutôt que cuisse) et appuie sur le bouton doseur. La dose choisie est alors injectée. Un même stylo permet de réaliser plusieurs injections (les aiguilles sont changées après chaque injection). Lorsque la cartouche est vide, le stylo est jeté. Pour la posologie, on commence par une dose de 1 mg dont on évalue l’efficacité au bout de 30 minutes. En l’absence d’effet, on monte par palier de 1mg jusqu’à l’obtention d’un déblocage. Beaucoup de détails sont fournis dans les ouvrages (voir les références), que les lecteurs pourront consulter.
Références :
La maladie de Parkinson de Luc Defebvre et Marc Vérin
La Maladie de Parkinson de Fabien Zagnoli et François Rouhart
Rédigé par Jean Pierre Lagadec
In Wikipédia : Elle a été découverte tardivement à l’état naturel dans le lotus bleu (nénuphar), alors désignée sous le nom de nuciférine (dont elle s’avéra en fait n’être qu’apparentée et présente conjointement), après son isolation plus ancienne dans les alcaloïdes dérivés de la morphine. Son action émétique était connue et elle se forme notamment à partir de la morphine en cas de carbonisation accidentelle de l’opium au cours de sa fabrication. Elle ne possède cependant pas le squelette morphinique et n’est donc pas un morphinique ni n’en présente les propriétés narcotiques et analgésiques, et ne provoque pas de syndrome de sevrage.
Sa fabrication est simple et peu onéreuse, mais la recherche et le développement autour de ses applications dans la maladie de Parkinson auraient un coût très important qui en expliqueraient les prix, tout autant que par sa mise en faible concurrence sur le marché des troubles de l’érection et de la libido (plus de 10 euros le comprimé sublingual de 3 mg).
Lu par Jean Graveleau
Des nanoparticules* contre Parkinson !
Publié le 29 juin 2016 à 10:48Article paru dans LE PARKINSONIEN INDÉPENDANT n°65
Imaginez une grève générale des éboueurs, l’état de la ville se dégraderait vite ! Pour certains chercheurs, c’est un peu ce qui se produit dans la maladie de Parkinson, où les lysosomes, des organites** qui dégradent les déchets de la cellule, ne fonctionneraient plus correctement, entraînant la mort des neurones.
Un pH trop élevé au sein de ces organites serait en cause, d’où l’idée de l’abaisser, avec des nanoparticules acidifiantes. C’est ce qui a été tenté avec succès dans un projet dirigé par Benjamin Dehay de l’Inserm. Les chercheurs ont d’abord montré que ces nanoparticules « réparent » des lysosomes dysfonctionnels dans des cultures cellulaires, puis les ont injectées dans le cerveau de souris touchées par un modèle murin de la maladie de Parkinson. Ce traitement a ralenti la dégénérescence neuronale.
*nanoparticule : élément ayant une taille nanométrique entre 1 et 100 nanomètres (un nanomètre est 1°000 millions de fois plus petit qu’un mètre)
** organite : tout élément cellulaire différencié, assurant une fonction déterminée (ex. le noyau)
Article paru dans la revue « Cerveau & Psycho » d’Avril 2016
Lu par Françoise Vignon
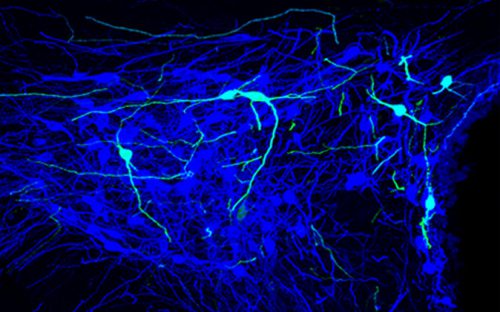
Découverte de 30 petits neurones qui endorment la douleur
Publié le 28 juin 2016 à 08:15Article paru dans LE PARKINSONIEN INDÉPENDANT n°65
Chez le rat, une trentaine de neurones (en vert) parmi les milliers qui secrètent une hormone atténuant la douleur, l’ocytocine, (en bleu) contrôlent la réponse à une douleur inflammatoire par 2 voies différentes.
« L’ocytocine est un acteur essentiel dans la modulation de la perception de la douleur », a expliqué à l’AFP, Alexandre Charlet, chercheur à l’Institut des neurosciences cellulaires et intégratives du CNRS de Strasbourg qui a coordonné l’étude menée par près de 30 scientifiques internationaux (France, Allemagne, Chine, Suisse, Italie, Etats-Unis). Outre son rôle antalgique, l’ocytocine est impliquée notamment dans le processus de l’accouchement et la sociabilité, ce qui lui a valu le surnom d’hormone « de l’amour et de l’empathie ».
Jusqu’à présent, le processus de libération de cette ocytocine (qui est notamment synthétisé par l’hypothalamus dans le cerveau), était mal connu. Les chercheurs sont parvenus à identifier un « centre de contrôle de la douleur » constitué d’une trentaine de neurones qui coordonnent la libération d’ocytocine dans le sang et la moelle épinière. Lors de douleurs aiguës ou d’une sensibilisation inflammatoire (brûlure, pincement, coupure, etc.) l’information est acheminée par les nerfs périphériques jusqu’aux neurones de la moelle épinière » explique le CNRS à l’AFP
« L’information est alors adressée à d’autres neurones, parmi lesquels une petite population de 30 cellules de petite taille de l’hypothalamus, identifiés par l’équipe d’Alexandre Chalet. En retour, ils activent une famille de gros neurones (magnocellulaires), dans une autre région de l’hypothalamus, qui libèrent l’ocytocine dans la circulation sanguine.
L’ocytocine vient alors ‘endormir’ les neurones périphériques (situés près de la zone douloureuse) qui envoient au cerveau le message responsable de la douleur. Parallèlement, le prolongement de ces trente neurones (appelés axones et mesurant jusqu’à un mètre) atteint la plus profonde des dix couches de la moelle épinière. C’est précisément à cet endroit, où le message sensoriel est codé en intensité, qu’ils libèrent l’ocytocine.
Ils diminuent donc, par deux voies simultanées, la reconduction du message douloureux au cerveau » selon le CNRS. Les chercheurs espèrent à présent, « trouver des marqueurs génétiques capables d’activer ou d’inhiber de manière spécifique ces trente neurones », afin de mieux atténuer les symptômes de patients souffrant de douleurs pathologiques, « tout en limitant les effets secondaires », a commenté Alexandre Charlet.
Article de la rédaction d’Allodocteurs du 04/03/2016
Lu par Françoise Vignon
Pesticides et santé : un dossier accablant
Publié le 26 juin 2016 à 08:49Articles parus dans LE PARKINSONIEN INDÉPENDANT n°65
Faut-il craindre les pesticides ? Indéniablement oui, en particulier si l’on est enceinte, enfant ou agriculteur. Agriculteur, parce que cette profession est exposée à des doses massives et régulières.
La preuve par la maladie de Parkinson :
Si les causes de la Maladie de Parkinson sont multiples et incluent un versant génétique, on sait aujourd’hui que les facteurs environnementaux jouent un rôle majeur. Parmi ceux-ci, l’exposition aux pesticides. La maladie est liée à la perte des neurones producteurs de dopamine, un neurotransmetteur impliqué dans le contrôle de la motricité.
En 2009, une équipe de recherche américaine a montré que le fait de vivre à moins de 500 mètres de zones agricoles traitées par des pesticides, augmente de 75% le risque de développer cette maladie. Les chercheurs ont mis en évidence ce risque accru lié à une double exposition au fongicide Manèbe® et à l’herbicide Paraquat®, à partir de l’historique d’utilisation des pesticides agricoles et du plan d’occupation des sols.
Les présomptions de lien entre les pesticides et la maladie de Parkinson remontent aux années 1980. Une vague de syndromes parkinsoniens précoces était apparue chez des toxicomanes californiens ayant consommé du MPTP, une neurotoxine produite par erreur lors de la synthèse d’un opioïde proche de l’héroïne. Or, le MPTP présente une structure chimique analogue à celle de l’herbicide Paraquat®. Très largement utilisé depuis 1961, ce composé a été interdit d’utilisation en Europe en 2007, mais persiste dans l’environnement. Il est toujours utilisé dans les pays en voie de développement.
Evaluer le facteur de risque pour le déclenchement de la maladie de Parkinson est particulièrement difficile : les agriculteurs sont en contact au cours de leur carrière avec de nombreuses substances actives, parfois simultanément. La tâche est encore complexifiée par le caractère évolutif de la maladie, indétectable durant une quinzaine d’années, jusqu’à l’apparition des premiers symptômes. Toutefois un grand nombre d’études établissent un faisceau de preuves. Le rapport publié en 2013 par l’Inserm, à la demande de la direction générale de la Santé, indique d’ailleurs que « d’après la méta-analyse la plus récente, un excès de risque significatif est rapporté chez les personnes exposées aux pesticides » Depuis le 4 mai 2012, la maladie de Parkinson provoquée par les pesticides a été inscrite au tableau des maladies agricoles professionnelles prises en charge par la Sécurité Sociale. Du fait de la diversité des pesticides, il n’est pas possible de parler de toxicité générale : la classification des plus utilisés fait déjà appel à cinquante familles chimiques. De nombreuses recherches ont été menées sur certains composés, mettant au jour une grande complexité des effets induits. Deux mécanismes d’action principaux émergent de ces travaux : un stress oxydant entraînant la mort cellulaire et le dysfonctionnement du système énergétique cellulaire, la mitochondrie. La plupart des pesticides combinent ces mécanismes avec d’autres effets. C’est le cas de la Roténone®, insecticide d’origine naturelle utilisé en agriculture biologique avant d’être interdit par la Communauté européenne en 2008.
L’étude publiée en 2008 par Ranjita Betarbet et ses collègues de l’université américaine d’Emory n’y est peut-être pas pour rien. En traitant des rats avec différentes concentrations de Roténone®, ces chercheurs ont reproduit les caractéristiques anatomiques, comportementales et neuropathologiques de la maladie de Parkinson. Ils ont pu constater que l’insecticide provoquait une réduction significative de la concentration en dopamine dans le cerveau, avec perte sélective des neurones dopaminergiques, ainsi que l’apparition d’agrégats d’alphasynucléine, protéine responsable de la dégénérescence des neurones.
Le constat épidémiologique et neurotoxicologique des liens entre exposition aux pesticides et maladie de Parkinson est sombre, mais les recherches en cours améliorent chaque jour la compréhension des mécanismes à l’œuvre, permettant d’envisager des pistes de lutte. Entre autres, Laurence Payrastre, chercheuse à l’Inra de Toulouse, s’interroge sur le possible bénéfice des micronutriments (tanin, polyphénols et pigments) présents dans la matrice végétale des aliments. Selon elle, « ces composés peuvent interagir avec les pesticides, soit directement, soit par compétition sur des cibles cellulaires communes ». Un espoir pour bloquer l’action délétère des produits phytosanitaires.
Article d’Aline Aurias, Oriane Dioux et Mathias Germain paru dans la revue « La Recherche » de Mars 2016
Lu par Françoise Vignon
Présents dans les insecticides et répulsifs en spray comme dans les champoings anti-poux, et les anti-moustiques, les pyréthrinoïdes sont nocifs pour le cerveau des enfants. Ils sont utilisés en agriculture pour combattre les nuisibles, par les vétérinaires pour éliminer les parasites, mais surtout à la maison pour se prémunir contre les moustiques et les poux. Les Pyréthrinoïdes, une classe d’insecticides très répandus, affecterait les performances cognitives des enfants, selon une étude menée en Bretagne.
Extrait d’un article paru dans « Science & Vie » du 11/08/15
Lu par Françoise Vignon
[vu sur le net] Parkinson : le nombre de cas a explosé en 30 ans
Publié le 24 juin 2016 à 07:23article trouvé sur le site pourquoi docteur ?
La maladie de Parkinson a progressé de manière alarmante en 30 ans. Le nombre de cas diagnostiqués par an est passé de 40 à 56 pour 100 000 personnes suivies.
pour lire cet article dans son intégralité, suivez ce lien…
[vu sur le net] PARKINSON : NAC, la protéine qui booste la dopamine
Publié le 21 juin 2016 à 07:57article trouvé sur le site Santé log
La NAC ou n‑acétylcystéine, un dérivé naturel de l’acide aminé cystéine, largement reconnu et utilisé pour ses effets antioxydants, montre, avec cette étude de l’Université Thomas Jefferson, un bénéfice très significatif chez les patients atteints de la maladie de Parkinson. 3 mois de supplémentation avec NAC suffisent ici à améliorer les niveaux de dopamine ‑en cause dans la maladie- et les capacités mentales des patients. Des conclusions présentées dans la revue PLoS ONE qui apportent un espoir dans la gestion des symptômes cognitifs de la maladie.
pour lire cet article dans son intégralité, suivez ce lien…
[vu sur le net] Maladies neurodégénératives : vers une meilleure prise en charge de la douleur ?
Publié le 24 mai 2016 à 10:35article trouvé sur le site de France TV info
C’est l’une des mesures du Plan maladies neurodégénératives : mieux prendre en charge les douleurs présentes dans les maladies d’Alzheimer et de Parkinson et la sclérose en plaques. Un colloque*, organisé le 12 mai 2016, a rassemblé les différents acteurs pour mieux comprendre ces souffrances invalidantes, leurs mécanismes, leur traitements et les voies de recherche. Compte-rendu d’une journée très riche.
pour lire cet article dans son intégralité, suivez ce lien…
[vu sur le net] PARKINSON : Médicaments et troubles compulsifs, quelles options
Publié le 13 mai 2016 à 09:10article trouvé sur le site Santé Log
Addiction alimentaire, au jeu, au shopping ou au sexe, retour avec cette étude de l’University Health System Loyola sur ces effets secondaires de risque de troubles compulsifs, avec certains médicaments indiqués dans le traitement de la maladie de Parkinson. Une revue de neurologues américains experts, des options disponibles, pour gérer au mieux, pour chaque patient, le traitement et ses effets collatéraux.
pour lire cet article dans son intégralité, suivez ce lien…
Vivre et accompagner le parkinsonien au quotidien, point de vue du neurologue
Publié le 06 mai 2016 à 21:45Texte de la conférence donnée par Dr Amélie Leblanc le 1er avril 2016, devant 200 personnes, à l’invitation par le GP29 à Landivisiau.
Pour mieux vivre sa maladie ou accompagner au mieux un patient parkinsonien en tant qu’aidant, il paraît indispensable de connaître la physiopathologie de la maladie de Parkinson, ses signes cliniques, les traitements et leurs effets secondaires ainsi que les structures d’aides médico-sociales. C’était le but de la conférence du 1er avril dernier à Landivisiau.
La maladie de Parkinson représente la deuxième maladie neuro-dégénérative en France après la maladie d’Alzheimer. Elle touche ainsi 150 000 personnes chaque année en France. Elle débute en moyenne vers 60 ans, plus rarement avant 40 ans et touche autant les hommes que les femmes. Elle est désormais intégrée au plan des maladies neuro-dégénératives (PMND) 2014 – 2019 visant à améliorer sa prise en charge.
La maladie de Parkinson est secondaire à un dysfonctionnement des noyaux gris centraux, siège de la motricité automatique. Du point de vue anatomopathologique, on peut observer une dépigmentation de la substance noire siégeant dans le mésencéphale liée à la dégénérescence des neurones dopaminergiques. A un niveau plus microscopique on observe des corps de Lewy dans les neurones. De nombreuses structures non dopaminergiques sont également touchées par le processus neurodégénératif. Les causes de cette perte neuronale sont la plupart du temps inconnues même si la responsabilité des pesticides est maintenant établie et si des formes familiales sont décrites.
Signes cliniques
Il est désormais acquis qu’il existe une phase pré-motrice précédant sûrement de plusieurs années l’apparition des symptômes moteurs. Cette phase comporte des signes cliniques variés tels que les troubles olfactifs, la constipation ou les troubles du comportement en sommeil paradoxal. Une des hypothèses physiopathologique serait l’existence d’une progression ascendante des lésions depuis le système nerveux digestif jusqu’au bulbe olfactif et au tronc cérébral.
Les signes moteurs apparaissent quant à eux lorsque les neurones dopaminergiques ont diminué de 70%. Ils comportent le tremblement de repos, l’akinésie et l’hypertonie extra-pyramidale (rigidité) qui composent la triade parkinsonienne.
Les patients parkinsoniens peuvent aussi se plaindre de symptômes non moteurs divers qui pourraient être représentés comme la partie immergée d’un iceberg. Ces symptômes souvent moins bien connus que les signes moteurs peuvent parfois être déroutants pour le patient et son entourage.
La mobilité peut être limitée par un freezing et des chutes secondaires à des troubles de l’équilibre, de la posture ou à une hypotension orthostatique.
Les capacités de communication sont parfois diminuées par une dysarthrie avec hypophonie ou par une hypersalivation.
Le sommeil est souvent agité avec un trouble du comportement en sommeil paradoxal ou un syndrome des jambes sans repos.
Outre un syndrome anxio-dépressif fréquent, pouvant précéder le diagnostic, la maladie de Parkinson peut comporter d’autres signes psychiatriques au premier rang desquels les hallucinations visuelles, le trouble du contrôle des émotions ou l’apathie peuvent surprendre l’entourage.
A un stade évolué, des troubles cognitifs peuvent survenir avec notamment des troubles de l’attention, un ralentissement cognitif qui entraînent une altération de l’autonomie cognitive et comportementale à des niveaux variables.
Beaucoup d’autres signes sont en fait liés à l’atteinte du système nerveux autonome : hypersudation, troubles vésico-sphinctériens, troubles sexuels, troubles de l’accommodation visuelle.
Les patients peuvent aussi présenter des signes plus généraux tels que des douleurs ostéo-articulaires ou neuropathiques, une dermite séborrhéique, des troubles de la vision des contrastes, un syndrome respiratoire restrictif…
Traitements
Sur le plan thérapeutique, trois grandes voies sont employées. Le traitement médical est utilisé en première intention alors que le traitement chirurgical est réservé aux formes compliquées. Quant à la rééducation et la réadaptation, elles sont utiles à tous les stades de la maladie.
Le traitement médical repose sur le principe de la compensation du déficit dopaminergique avec une multitude de médicaments disponibles que l’on peut classer dans 3 grandes voies thérapeutiques : apport d’un précurseur exogène de la dopamine (Levodopa), stimulation directe des récepteurs de la dopamine (agonistes dopaminergiques), réduction du catabolisme de la dopamine (IMAO, ICOMT). Dans la mesure du possible, les neurologues tendent à apporter une stimulation dopaminergique la plus continue possible et s’appuient de plus en plus fréquemment sur des techniques de perfusion sous-cutanée (pompe à Apomorphine) ou intra-duodénale (pompe à Duodopa).
La stimulation cérébrale profonde destinée aux patients parkinsoniens peut avoir plusieurs cibles : noyau ventral intermédiaire médian du thalamus pour le tremblement, noyau sub-thalamique en cas de forme akinéto-hypertonique et globus pallidus interne si des dyskinésies invalidantes viennent compliquer le traitement oral. Dans tous les cas son principe est d’inhiber les neurones cibles en appliquant une stimulation électrique à haute fréquence par le biais d’électrodes intra-crâniennes reliées à un stimulateur sous-cutané. Du fait de la lourdeur de la procédure chirurgicale, cette technique nécessite une sélection rigoureuse des patients éligibles pour éviter de possibles complications post-opératoires et des effets secondaires de ce traitement.
La prise en charge rééducative repose essentiellement sur la kinésithérapie et l’orthophonie. Le kinésithérapeute s’attachera à pratiquer des étirements globaux ainsi qu’un travail à haute intensité contre résistance et de dissociation axiale. La technique d’orthophonie la plus efficace dans la maladie de Parkinson est la Lee Silverman Voice Treatment (LSVT) pour la dysarthrie mais les séances sont également utiles pour la micrographie ou les éventuels troubles de la déglutition. L’intervention d’un ergothérapeute peut être nécessaire pour aménager le domicile dans les stades avancés.
Afin d’améliorer de nombreux paramètres moteurs et non moteurs, il est maintenant recommandé aux patients une activité physique quotidienne à type de marche nordique, Taï Chi, Qi Kong, tango… Cette prise en charge non médicamenteuse nécessite un investissement personnel de la part du patient et parfois de l’aidant mais apporte des bénéfices parfois insoupçonnés.
Il est important de savoir que les traitements médicamenteux peuvent provoquer des effets secondaires moteurs et non moteurs afin de pouvoir les dépister et les prendre en charge précocement. Au niveau moteur, on voit apparaître des fluctuations d’efficacité motrice et des dyskinésies liées à une diminution d’efficacité après plusieurs années de traitement. Des effets secondaires non moteurs peuvent aussi survenir : signes digestifs (nausées, vomissements, sécheresse buccale), hypotension orthostatique, troubles psychiatriques (trouble du contrôle des impulsions avec développement d’addictions alimentaires, au jeu, sexuelles … , hallucinations visuelles, troubles du comportement), somnolence.
Pour mieux connaître la maladie.
Selon l’OMS, l’éducation thérapeutique du patient. (ETP) vise à aider les patients à acquérir ou maintenir les compétences dont ils ont besoin pour gérer au mieux leur vie avec une maladie chronique. C’est une avancée dans la conception de la prise en charge des maladies chroniques dont fait partie la maladie de Parkinson, c’est pourquoi l’ETP prend sa place dans les actions à développer dans le PMND. Un projet est d’ailleurs en cours de rédaction par le service de neurologie du CHRU de Brest, en association avec l’association des parkinsoniens du Finistère et sera déposé à l’Agence Régionale de Santé (ARS) de Bretagne courant juin.
Les patients et leur entourage font souvent des démarches personnelles pour obtenir des informations complémentaires sur la maladie. Divers documents édités par des organismes d’Etat (Agence nationale de sécurité du médicament, Haute autorité de santé) ou des sites internet tels que le site du réseau Oniric http://www.neurobretagne-oniric.com sont à même d’apporter des informations fiables sur la maladie et les traitements.
Comment se faire aider ?
Si un problème médical ou social survient au cours de la prise en charge, le réseau de soins, médical, paramédical, et social qui s’est tissé autour du patient et de l’aidant doit être sollicité. Les associations de malades peuvent parfois apporter une aide complémentaire. Pour répondre aux questions plus sociales (aides financières, mise en place d’aides à domicile, aménagement du domicile) les structures sanitaires et sociales (CLIC = Centre Local d’Information et de Coordination, CCAS ou CDAS= Centre Communal ou Départemental d’Action Sociale, service APA = Allocation Personnalisée d’Autonomie, MAIA = Maisons pour l’Autonomie et l’Intégration des malades d’Alzheimer, Services d’aide à domicile, SSIAD = Services de Soins Infirmiers A Domicile) peuvent être sollicitées. Par ailleurs, des structures de répit existent afin d’éviter l’épuisement de l’aidant.
Pour conclure, il est important que le parkinsonien devienne l’acteur principal de sa prise en charge. Pour cela, l’ETP est d’un intérêt fondamental car elle a pour but d’induire une meilleure connaissance de la maladie et des traitements pour une meilleure gestion de la vie quotidienne. Le patient peut aussi s’impliquer dans sa prise en charge en pratiquant une activité physique quotidienne.
La place des aidants est maintenant reconnue et développée dans le PMND. L’accompagnement d’un patient au quotidien nécessite pour lui aussi une meilleure compréhension des symptômes de la maladie afin d’entretenir la plus grande autonomie possible.
Il est indispensable de mettre en place un réseau local centré sur le couple « patient-aidant » mais dans les situations difficiles, le recours aux structures d’aides et de répit peut être nécessaire.
Dr. Amélie Leblanc
Spécialiste des hôpitaux des armées
Service de neurologie et unité neuro-vasculaire
CHRU Cavale-Blanche, Brest
[vu sur le net] L’unité Parkinson d’Ydes (15), une structure spécialisée unique en France
Publié le 28 avril 2016 à 12:14article trouvé sur le site de France 3 Auvergne
L’unité d’hébergement et de soins pour personnes atteintes de la maladie de Parkinson d’Ydes (Cantal) a ouvert en avril 2012. Classée unité de soins de longue durée expérimentale, cette structure est unique en France.
pour lire cet article dans son intégralité, suivez ce lien…
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.