Témoignage : La stimulation consciente
Publié le 29 mars 2009 à 15:56Paru dans LE PARKINSONIEN INDÉPENDANT N°36 – mars 2009
Par Jocelyne Gouge
Bonjour et merci de vous intéresser à mes travaux.
Vous comprendrez que le programme que j’applique est de mon cru, inspiré par des techniques et approches existantes. Qu’il en est toujours au stade expérimental et que je tiens à ce que mes résultats soient validés par mon neurologue avant de les rendre publics. Je tiens à ce que le maximum de personnes en bénéficie. Cela va me demander beaucoup de travail car je dois commencer par expliquer les bases, la « mécanique » et les mises en garde : la stimulation consciente amène avec le temps une réduction de la médication, le suivi médical est donc primordial.
Moi aussi j’ai la maladie de Parkinson et je dois prendre des médicaments. Il faut bien comprendre qu’une maladie qui nous détruit depuis cinq, dix, quinze ans ou plus ne disparaîtra pas en six mois. J’ai mis dix mois à réapprendre à marcher et deux mois supplémentaires pour pouvoir le faire sans la canne que j’utilisais depuis sept ans. Pour l’écriture, à peu près le même temps. Il ne s’agit pas d’exercices que l’on fait comme un robot et, pour l’instant, rien ne me permet de croire que les résultats puissent être permanents sans la pratique régulière. Lorsque je relâche, comme je l’ai fait pendant la période des Fêtes, les symptômes se réinstallent. C’est donc un travail de tous les jours qui demande de s’impliquer dans l’amélioration de sa condition. C’est un mode de vie, une occupation à temps plein, mais qui en vaut la peine. J’ai réduit de moitié ma médication sur une période de dix-huit mois.
Je me lance donc. Je vais tenter de vous expliquer brièvement sur quoi se base la stimulation consciente.
La neuroplasticité : Quand une zone du cerveau présente un trouble particulier, le cerveau a la capacité de rééduquer la fonction touchée en utilisant une autre zone cérébrale. De nouvelles connections neuronales sont créées. Le corps a tout pour se guérir, mais il demande notre collaboration. Chaque jour, plusieurs milliards de cellules sont remplacées en commençant par les cellules malades.
La mémoire du corps : Notre corps nous fait souffrir mais il est prêt à guérir si on lui dit comment faire. Il a une mémoire infaillible ; il suffit de lui rappeler comment s’y prendre pour récupérer des fonctions perdues.
Le plaisir : Le plaisir change la chimie du cerveau.
La posture et la respiration : Il faut d’abord corriger la posture, cela facilite la respiration et augmente l’oxygénation de l’organisme.
Donc la première étape consiste à rétablir progressivement sa posture en prenant conscience des changements que cela amène dans tout notre corps. Le mauvais alignement du corps se fait sentir à cette étape. L’aide professionnelle (physio, kiné, chiro) peut aider. Personnellement j’ai eu recours aux services d’une physiothérapeute sur une période de dix mois.
Tout en corrigeant sa posture, on intègre des exercices respiratoires et de relaxation, toujours en prenant conscience de ce qui se passe dans son corps.
Ensuite on se fait un « plan de match ». Il s’agit ici faire la liste de ses objectifs. On construit l’escalier qui nous mènera à l’objectif ultime, une marche à la fois, en intégrant des paliers qui serviront de points de repère. Les petits objectifs sont plus faciles à atteindre et l’atteinte d’un objectif, renforce la motivation. Le simple fait d’être capable de se tenir droit est une grande victoire pour plusieurs personnes. Et cette étape est une étape-clé.
Lorsque l’on demande au corps de reproduire un mouvement, on demande au cerveau d’établir les connections nécessaires à la reproduction de ce mouvement. Il est important de faire ces connections à plusieurs reprises au cours de la journée. C’est comme un pianiste de concert. Il a beau être excellent et maîtriser son art, s’il veut demeurer au sommet il doit pratiquer chaque jour. Donc, lorsque vous aurez récupéré une fonction, vous devrez l’utiliser régulièrement ensuite. Si vous réapprenez à marcher et que vous passez ensuite vos journées dans un fauteuil devant la télé ou l’ordinateur, vous reperdrez vite vos aptitudes à marcher.
J’espère avoir répondu un peu à vos questions. Parallèlement à l’écriture de mon livre, je vais essayer dans les semaines à venir de faire un document modulaire traitant les divers aspects du programme : physique, cognitif, social, etc. Je pourrai par la suite placer des exercices spécifiques dans chacun des modules. Je vais aussi essayer de décrire ma progression, mais il va falloir que je retrouve mes notes.
Je n’ai aucune prétention, j’y vais avec l’intuition et les connaissances acquises au fil des années. Pour l’instant, les résultats sont positifs, je sens que la maladie est toujours présente, surtout lorsque je néglige mes exercices, mais elle est moins envahissante. Les résultats dépendent évidemment du stade d’évolution de la maladie, mais aussi de la détermination et de l’énergie que l’on met à regagner la santé.
Jocelyne, Québec, 51/8.5
passemots@iquebec.com
Lu par Jean GRAVELEAU graveleau.jean2@orange.fr
Parkinson : stimuler le cerveau réduit les symptômes
Publié le 28 mars 2009 à 09:38Paru dans LE PARKINSONIEN INDÉPENDANT N°36 – mars 2009
7 janv. 2009
WASHINGTON (AFP) — Des stimulations électriques en profondeur dans le cerveau réduisent les symptômes des personnes atteintes de la maladie de Parkinson mais cette procédure accroît les risques d’effets secondaires potentiellement graves, selon une étude clinique publiée mardi.
Les patients souffrant de Parkinson à un stade avancé à qui on a implanté chirurgicalement des électrodes en profondeur dans le cerveau ont connu, après six mois, une amélioration dans la coordination de leurs mouvements et la qualité de leur vie nettement plus grande que ceux ayant bénéficié d’autres thérapies, expliquent les auteurs de cette recherche parue dans le Journal of the American Medical Association (JAMA) daté du 7 janvier.
Ainsi, 71% des malades de l’étude dont le cerveau a été stimulé par des électrodes ont connu après six mois une amélioration clinique très nette de leurs fonctions motrices avec moins de tremblements et de mouvements incontrôlés contre seulement 32% dans le groupe témoin traité avec des thérapies conventionnelles.
« Toutefois, de récentes informations mettant en lumière des effets secondaires inattendus de la stimulation cérébrale en profondeur indiquent que ce traitement qui améliore les fonctions motrices peut aussi avoir des conséquences indésirables », relève la Dr Frances Weaver, du Hines VA Hospital à Hines dans l’Illinois (nord), principal auteur de cette étude.
Le risque de subir des effets secondaires tels que des infections, des troubles du système nerveux ou des troubles cardiaques ou psychiatriques était 3,8 fois plus élevé dans le groupe ayant des électrodes cérébrales que chez les patients traités avec d’autres thérapies.
C’est ainsi que 45 sujets avec des électrodes implantées dans le cerveau, (soit 40% du total) ont subi 82 effets secondaires graves. Dans le groupe témoin, 15 sujets (11%) ont subi 19 effets secondaires de même gravité.
La prudence devrait être observée pour éviter d’exagérer ou de minimiser les risques de la stimulation du cerveau en profondeur avec des électrodes implantées chez les malades atteints de la maladie de Parkinson, estiment les auteurs de l’étude.
Les médecins doivent continuer à évaluer les risques potentiels à court et long terme de cette procédure par rapport aux effets bénéfiques pour chaque malade, concluent-ils.
Au total, 255 patients souffrant de la maladie de Parkinson à un stade avancé ont participé à cette étude clinique, dont 25% avaient plus de 70 ans.
Les électrodes ont été implantées dans différentes zones du cerveau, variables selon les patients.
Dans un éditorial également publié dans le JAMA, le Dr Günther Deuschl, de l’Universitätsklinikum Schleswig-Holstein à Kiel en Allemagne, juge que « les résultats de cette importante étude ont confirmé de façon convaincante l’efficacité après six mois de la stimulation cérébrale profonde pour les cas de Parkinson avancé dans le plus grand groupe de patients ayant à ce jour participé à un essai clinique ».
Il note toutefois que « cette étude combinée à des recherches antérieures sur cette thérapie, montre que de tels progrès dans le traitement ne peuvent se faire sans un prix en termes d’effets secondaires ».
On estime qu’au moins 500.000 personnes sont atteintes de Parkinson aux Etats-Unis et que 50.000 nouveaux cas sont diagnostiqués chaque année, selon les statistiques des Instituts nationaux américains de la santé (NIH).
Ces chiffres devraient augmenter avec l’accroissement de l’âge moyen de la population.
Les hommes paraissent être légèrement plus touchés que les femmes.
L’âge moyen d’apparition de la maladie, dont les causes restent obscures, est d’environ 60 ans.
Texte trouvé sur Internet Google
Transmis par Henri MINARET et lu par Jean GRAVELEAU graveleau.jean2@orange.fr
Le mouvement du cormoran
Publié le 27 mars 2009 à 07:13Paru dans LE PARKINSONIEN INDÉPENDANT N°36 – mars 2009
Un exposé de Mr. Hubert Colombel, psychomotricien et orthophoniste
Résumé par Jean Pierre Lagadec
Le 25 Janvier 2009, l’Association des Parkinsoniens des Côtes d’Armor, à l’initiative de son président Sylvain Bielle, organisait une réunion d’information pour ses adhérents à Paimpol (22).
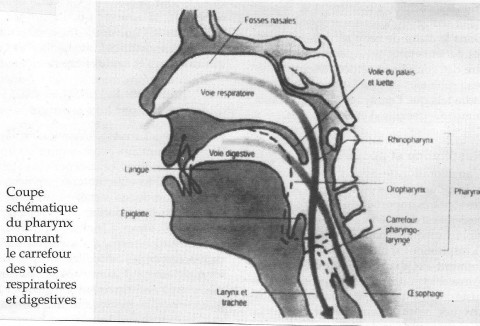
Lors de cette réunion, Mr Hubert Colombel, psychomotricien et orthophoniste à Lannion (22), a fait un exposé sur le fonctionnement, les troubles et la rééducation de la déglutition, dans la maladie de Parkinson. Cet exposé est résumé dans le texte qui suit.
1. Fonctionnement de la déglutition
Après une première démarche (parfois laborieuse pour le Parkinsonien) consistant à porter l’aliment vers la bouche, la déglutition va se dérouler en 3 temps :
- le temps buccal (mouvements volontaires)
- le temps pharyngé (mouvements réflexes)
- le temps œsophagien (mouvements réflexes)
la figure ci-après donne une représentation des voies respiratoires et digestives.le temps buccal :
Il est géré par le système pyramidal (les mouvements sont volontaires). Ce temps buccal va se dérouler en plusieurs phases successives :- Tout d’abord, une phase bilabiale, pour saisir l’aliment par les lèvres et le porter au niveau des dents, ce qui suppose une bonne mobilité et tonicité des muscles des lèvres.
- Puis, une phase apicale (pointe de la langue ou apex). La langue fonctionne comme une « louche » pour venir récupérer l’aliment derrière les dents et amorcer le début de la formation du bolus, en cherchant à condenser l’aliment au niveau du palais. Cette action de louchage demande une bonne mobilité de la langue.
- Ensuite, une phase de mastication. En fonction de l’aliment, les mandibules sont mises en action pour écraser l’aliment, lui associer de la salive et préparer le bolus.
- Enfin, une phase de constitution du bolus. Grâce à l’élévation de la langue au palais, et à la compression en amont du bolus, une dépression s’exerce à l’arrière ce qui prépare le temps pharyngé qui va suivre. Cette phase demande du tonus pour exercer cette pression et déclencher le temps pharyngé.
Le temps pharyngé (réflexe) :
Le déplacement du bolus vers l’arrière de la bouche provoque une élévation du voile du palais, ce qui évite le reflux nasopharyngé en fermant l’accès aux voies nasales. Le temps pharyngé réflexe se déclenche lorsque le bolus arrive à la base de la langue. Le bolus est propulsé vers l’arrière par un coup de piston de la langue. Au même moment, se produit un mouvement d’ascension du larynx et un abaissement de l’épiglotte pour empêcher la fausse route de l’aliment vers la trachée. Simultanément, les sphincters de l’œsophage se relâchent pour permettre au bolus de glisser jusqu’à l’estomac.Le temps œsophagien (réflexe) :
Les muscles de l’œsophage se relâchent pour permettre la descente du bolus vers l’estomac.2. Les troubles de la déglutition (Dysphagie)
La déglutition fait appel à un ensemble de mouvements fins et complexes de la bouche, du pharynx et de l’œsophage. Une bonne déglutition implique une parfaite synchronisation entre le mouvement volontaire et les mouvements réflexes.
Chez le Parkinsonien, les troubles apparaissent dès l’atteinte de la sphère bucco-faciale (lèvres, bouche, pharynx…), dont les muscles perdent souplesse et tonicité.
Le Parkinsonien dysphagique peut être sujet :- aux fausses routes,
- à des reflux,
- à l’hypersiallorrhée
Les fausses routes
Dans ce cas, généralement en raison d’un mauvais réflexe pharyngé, l’aliment, au lieu d’emprunter la voie digestive vers l’œsophage, se dirige vers la voie respiratoire de la trachée. Il est alors le plus souvent refoulé avec ou sans toux. Mais, dans le cas de patients gravement atteints, les fausses routes peuvent provoquer des problèmes pulmonaires de plus en plus graves, voire le décès par asphyxie.Les reflux
Il s’agit, soit de remontée du bol alimentaire de l’estomac ou de l’œsophage, soit de reflux de débris alimentaires à partir de cavités latérales du pharynx. Ces reflux désagréables peuvent provoquer une perte de poids, voire une déshydratation.L’hypersiallorrhée
Elle est rarement due à un excès de salive par les glandes salivaires, mais le plus souvent à un trouble de déglutition. Normalement, la salive produite régulièrement est absorbée automatiquement, à raison de 2000 fois par jour. En cas de non absorption, la salive s’accumule dans la bouche et comme le patient a les lèvres entrouvertes et la tête baissée, finit par déborder et couler à la commissure des lèvres. C’est le « bavage ».Les troubles de la déglutition concernent environ 50% de Parkinsoniens. Environ 90% de ces dysphagiques ont une phase buccale perturbée. Plus de 90% n’arrivent pas à bien former le bolus et 30% ont tendance à avoir des fuites de liquide au niveau des lèvres. 80% ont tendance au bavage.
3. Rééducation de la déglutition
Compte tenu des risques dus aux troubles de la déglutition, la rééducation chez un orthophoniste est nécessaire et cela le plus tôt possible. Or actuellement, 5% des dysphagiques seulement bénéficieraient d’une rééducation.Le rôle de l’orthophoniste consiste :
- à établir pour le patient un bilan de la déglutition
- à proposer une démarche thérapeutique
- à proposer des exercices de rééducation
Bilan de la déglutition
Pour établir le bilan, l’orthophoniste utilisera tout d’abord les informations fournies par le patient sur ses difficultés (problèmes gestuels, fausses routes, la manière d’organiser ses repas, etc …).
Ensuite, il procédera à un examen clinique pour savoir comment le patient déglutit les liquides, les semi liquides et les solides, en notant la posture, la coordination des différentes phases de la déglutition.
Enfin il pourra prendre en compte des informations médicales, comme celles fournies par un examen par fibroscopie. Cet examen est indispensable pour détecter certaines fausses routes souvent silencieuses et peut fournir des informations précieuses sur le déroulement des différentes phases de la déglutition.
La cinéradiographie et la manométrie permettront aussi, si nécessaire, de préciser le bilan.Démarche thérapeutique
L’orthophoniste pourra alors engager une démarche thérapeutique avec le patient. Il pourra :- mettre le doigt sur le dysfonctionnement,
- expliquer le processus de déglutition verbalement et à l’aide de représentations visuelles (dessins, photos, vidéos)
- lui donner des conseils pour l’organisation des repas, le comportement à table, ainsi que pour le choix des aliments.
- travailler la perception et la réalisation des schèmes moteurs de la déglutition à partir d’exercices personnalisés. Par exemple, on pourra solliciter une réaction réflexe des phases pharyngée et œsophagienne.
- préparer des exercices à réaliser fréquemment à domicile.
Exemple d’exercice (le mouvement du cormoran)
Voici un exercice proposé en consultation par Mr Colombel à ses patients dysphagiques et qu’il leur conseille de faire à domicile. Mr Colombel a présenté une vidéo pour expliquer les mouvements qu’il a ensuite mimés devant l’assistance.
L’exercice a pour but, une fois le bolus correctement constitué, de favoriser le déclenchement du réflexe pharyngé. Les différents gestes sont les suivants :- inspiration
- blocage respiratoire (pour stimuler la fermeture des voies respiratoires)
- mouvement assez rapide et léger d’extension de la tête, pour aider notamment les liquides à glisser vers l’arrière (la zone pharyngo-laryngée),
- pression spontanée et forte du milieu de la langue sur le milieu du palais, menton légèrement fléchi, nuque étirée, épaules basses, tronc vertical, pieds à plat.
- secousse éventuelle de la tête au moment où la phase pharyngée s’installe en relevant le menton et en le rabaissant ensuite pour dynamiser l’action réflexe. C’est le « mouvement du cormoran », qui s’apparente à celui de l’oiseau marin, lorsqu’il ingurgite un gros poisson.
- toux accompagnant l’expiration pour dynamiser le mouvement. Le patient pourra orienter la tête en fonction de sensation de présence de résidus alimentaires et tousser deux à trois fois avant le bolus suivant.
Cet exercice répété au domicile, aussi bien pendant que hors des repas doit améliorer le déclenchement du réflexe pharyngé et doit être pratiqué en cas de risque de fausse route.
Enfin, à partir de son expérience de psychomotricien, Mr ColombeI recommande le mouvement du cormoran aux dysphagiques sujets au « bavage », la répétition de l’exercice pouvant permettre de retrouver le réflexe (mémoire procédurale).Rédigé par Jean Pierre Lagadec jpmo5@wanadoo.fr
Rester alerte grâce à un entraînement quotidien — Parkinson suisse N°92
Publié le 26 mars 2009 à 06:37Paru dans LE PARKINSONIEN INDÉPENDANT N°36 – mars 2009
Par Jörg ROTHWEILER
La physiothérapie et la gymnastique quotidienne aident les parkinsoniens à entretenir et préserver leur mobilité le plus longtemps possible. Un bon entrainement leur permet de rester alertes et leur garantit une plus grande sécurité au quotidien.
Si l’on ne bouge pas régulièrement on « rouille ». Les muscles fondent, le ventre grossit, les tendons raccourcissent, les articulations se raidissent et l’esprit devient de plus en plus rigide.
C’est pourquoi hommes et femmes, jeunes et vieux, personnes saines et malades doivent garder en tête cette vérité fondamentale : bouger prévient les problèmes. S’étirer, se plier et faire régulièrement des efforts permet de rester alerte et fort, et de bien coordonner ses mouvements au quotidien.
La science a prouvé depuis longtemps qu’une physiothérapie régulière et des exercices de gymnastique quotidienne amélioraient considérablement la qualité de vie des personnes souffrant de la maladie de parkinson. Grâce à une physiothérapie ciblée, il est possible de ralentir l’évolution des troubles moteurs des parkinsoniens et de réduire leurs problèmes de posture. En outre, une stimulation quotidienne des capacités de coordination permet aux malades d’accomplir seuls et en toute sécurité les mouvements de tous les jours, pendant longtemps.
Pas d’exercice sans l’avis d’un spécialiste.
La condition essentielle pour que la physiothérapie produise des effets optimaux est d’ne respecter les indications. Car s’il effectue les exercices de manière erronée, le malade obtient souvent des résultats inverses à ceux souhaités et, dans les cas les plus graves, peut se blesser. C’est pourquoi les personnes concernées doivent effectuer uniquement les exercices qu’un spécialiste leur a minutieusement expliqués et appris. Par ailleurs, les muscles, l’état neurologique général et bien sûr le système cardio-vasculaire doivent être surveillés et contrôlés régulièrement. Grâce aux informations ainsi acquises, la pertinence du programme et, le cas échéant, les exercices sont adaptés.
Le programme en cinq points pour rester alerte
Les objectifs fondamentaux d’un programme d’entraînement sont :
- Prévenir le raccourcissement des muscles et des tendons.
- Parvenir à une flexibilité maximum.
- Améliorer la posture de base.
- Développer ou entretenir les muscles.
- Améliorer ou préserver la motricité fine.
- Renforcer la respiration et l’inspiration.
- Améliorer l’équilibre et la stabilité lors des déplacements.
- Améliorer le sentiment général de bien-être corporel.
Afin d’atteindre ces objectifs, le programme d’entraînement doit en principe couvrir les cinq points suivants :
1 – Le mouvement : les personnes souffrant de la maladie de parkinson doivent effectuer quotidiennement des exercices destinés à développer leurs muscles et à améliorer leur endurance. C’est pourquoi ces exercices doivent pouvoir être réalisés à la maison et sans l’aide d’accessoires particuliers. Idéalement, il faut combiner des exercices actifs (développement musculaire, endurance) à des exercices passifs.
2 – Détente : les exercices de relaxation et de détente sont aussi importants que les exercices de mouvement, car ils contribuent à décontracter les muscles efficacement et durablement, à se délasser spirituellement et, ainsi, à apaiser dans une certaine mesure les douleurs dues aux tremblements. En outre, ils aident à gérer les situations de stress au quotidien.
3 – Mobilité quotidienne : ce module d’entrainement vise à permettre aux patients d’accomplir avec plus d’assurance et de facilités les mouvements quotidiens, tels que s’asseoir sur une chaise ou s’en lever, monter en voiture ou en descendre, tourner son corps en position allongée, monter des escaliers. Par ailleurs, elle permet de maintenir à un bon niveau les capacités motrices fines : écrire, trier ses cachets, s’habiller et se déshabiller seul, manipuler des accessoires, etc. Dans le cadre de cette série d’exercices, les patients peuvent également apprendre des conseils et astuces afin de gérer les problèmes caractéristiques de la maladie tels que l’enrayage cinétique de la marche (« freezing ») et les blocages.
4 – Respiration et posture : l’amélioration de la capacité pulmonaire et la réduction des problèmes respiratoires sont très importantes. La clé pour bien respirer est de se tenir aussi droit que possible. Lorsque le haut du corps est droit, la respiration est plus profonde et le mouvement du diaphragme plus ample. Ainsi, l’appareil digestif, qui se trouve juste en dessous, est plus mobile et mieux irrigués, ce qui a pour effet de faciliter la digestion et donc de mieux alimenter le corps en énergie. Le fait de respirer plus profondément augmente la saturation du sang en oxygène, la condition physique du patient s’en trouvant globalement améliorée : il retrouve agilité et vivacité d’esprit. Il est également utile d’effectuer, si les symptômes l’exigent, des exercices de prononciations et de déglutition (orthophonie).
5 – Marche et équilibre : l’objectif de ces exercices est de permettre au patient de marcher avec plus d’assurance et de se tenir debout de la manière la plus stable possible (prévention des chutes), et ce pas uniquement au calme chez lui, mais également dans la nature, sur des chemins inégaux et dans des environnements animés comme le centre commercial ou la gare.
Méthodes complémentaires de physiothérapie
Préalablement à l’entraînement quotidien – et, au besoin, pendant – il est naturellement nécessaire d’apaiser ou d’éliminer les problèmes tels que douleurs, contractures, crampes, etc. par des traitements ciblés tels que massages et applications de chaleur.
Impliquer les proches ou participer aux groupes
Naturellement, il est souhaitable d’expliquer l’entraînement aux proches qui s’occupent des malades. Ainsi, ceux-ci peuvent vérifier que la patient effectue correctement ses exercices lors de son entraînement quotidien à la maison, lui apporter leur aide et, en cas de démotivation, l’inciter à poursuivre l’entraînement même s’il lui arrive parfois de rencontrer des difficultés. La meilleure solution consiste encore à effectuer l’entraînement en groupe. Les participants se motiveront mutuellement et l’effet de groupe les aidera à s’entraîner régulièrement.
Lu par Jean GRAVELEAU graveleau.jean2@orange.fr
Garder une bouche saine
Publié le 13 janvier 2009 à 16:28Article paru dans LE PARKINSONIEN INDÉPENDANT N°35 – décembre 2008
Indispensable à tout âge, une bonne hygiène bucco-dentaire s’avère d’autant plus importante quand l’âge fragilise notre bouche.
Se servir d’une brosse à dents demande a la fois de la dextérité, de la force et de la coordination… Si une personne ne peut plus effectuer ce geste, il va falloir l’aider car, aux problèmes bucco-dentaires que nous connaissons tous, l’âge ajoute des facteurs aggravants.
La rétraction de la gencive, par exemple, qui favorise l’apparition de caries au niveau des racines ; la diminution de la production de salive, qui s’accélère encore avec la prise de médicaments. Non seulement la sensation de bouche sèche est désagréable mais, surtout, la salive ne joue plus son rôle protecteur et autonettoyant ; le port d’une prothèse, totale ou partielle, qui augmente le risque d’irritation ou d’inflammation.
Le Pr Marysette FOLLIGUET, chef du Service d’odontologie de l’hôpital Louis Mourier à Colombes (92), estime indispensable de veiller à la toilette buccale des personnes âgées, autant pour leur santé (inflammation mais aussi risque de dénutrition) que pour leur vie familiale et sociale (troubles de la parole et repliement sur soi)…
Suivons ses conseils : après chaque repas, se rincer la bouche avec un verre d’eau, ou si cela est plus facile, simplement boire un verre d’eau ; brosser les dents, mais aussi la langue, le palais, les gencives avec une brosse souple et douce ; utiliser une brosse électrique si nécessaire ; enlever les prothèses et les nettoyer soigneusement ; enfin, si une personne supporte mal l’usage de la brosse, utiliser une compresse humide sur les faces des dents et des muqueuses, et boire suffisamment.
Ces mesures simples sont parfois difficiles à appliquer, reconnaît le Dr FOLLIGUET : Brosser les dents de quelqu’un est un geste malaisé à effectuer, non seulement techniquement, mais aussi psychologiquement. Certaines personnes âgées ne supportent pas « cette intrusion ». Le chirurgien-dentiste peut donner des conseils, montrer la façon d’enlever une prothèse sans blesser ou comment éviter les réflexes nauséeux.
Le soin des dents et de la bouche ne doit pas constituer une épreuve triquotidienne. Mieux vaut un seul brossage, le soir, bien accepté et bien effectué, que trois tentatives stressantes.
« L’important aujourd’hui est de sensibiliser les personnes et leur entourage à la nécessité d’une hygiène quotidienne et d’un suivi dentaire ».
Extrait d’un article de « Notre Temps », Octobre 2008
Lu par Françoise VIGNON
Exposé d’une orthophoniste — rédigé par Jean Pierre Lagadec
Publié le 13 janvier 2009 à 01:47Article paru dans LE PARKINSONIEN INDÉPENDANT N°35 – décembre 2008
Lors de l’assemblée générale du CECAP, à Loctudy, une orthophoniste a fait un exposé sur les troubles et la rééducation de la parole, de la déglutition et de l’écriture dans la maladie de Parkinson.
Cet exposé est résumé dans le texte qui suit.
1. Troubles de la parole (Dysarthrie)
Ces troubles sont très fréquents chez les sujets parkinsoniens
Ils se caractérisent par une réduction de l’intensité vocale, une voix rauque et monotone et une articulation imprécise.
Les troubles de la parole apparaissent souvent au début de la maladie, mais peuvent rester assez longtemps, ignorés ou incompris du patient. Lors de la première consultation orthophonique, on peut entendre ce genre de phrases : « on ne m’écoute pas ! », « on me coupe la parole », « je ne peux pas prendre la parole en réunion », « ma femme est sourde » etc…
Les troubles de la parole sont pourtant pénalisants et handicapent le patient dans la vie sociale et professionnelle. Ils doivent donc être traités le plus précocement possible.
Que proposer comme traitement ?
- les traitements médicamenteux antiparkinsoniens classiques (L Dopa, agonistes dopaminergiques..) efficaces pour l’amélioration de la motricité des membres, sont très peu ou pas du tout efficaces dans le traitement de la dysarthrie. Il en est de même des traitements neurochirurgicaux.
- les traitements orthophoniques traditionnels, souvent fastidieux pour le sujet, n’ont pas non plus démontré leur efficacité dans le traitement de la dysarthrie parkinsonienne. Pour rééduquer la parole, il faut parler et non se limiter à des exercices devant une glace.
C’est pourquoi, cette orthophoniste préconise une méthode, qu’elle applique avec succès depuis plusieurs années, la LSVT (Lee Silverman Voice Treatment) ou méthode de Lee Silverman.
Cette méthode est spécifique au traitement de la dysarthrie parkinsonienne. Pour être pleinement efficace, il faut respecter les conditions suivantes :
- la rééducation doit être précoce et intensive
- chaque session de rééducation comprend 16 séances de 1 heure, à raison de 4 séances hebdomadaires sur 4 semaines consécutives.
- les sessions sont à renouveler dans le temps (voire tous les ans)
- la rééducation demande de l’énergie et la participation active du patient
- après chaque séance journalière, le patient fait des exercices à domicile avant la séance suivante.
Au cours des séances, le travail de rééducation (simple et précis) est porté particulièrement sur l’augmentation de la production phonatoire.
Cette méthode LSVT d’origine américaine est pratiquée en France par des orthophonistes agréés.
2. Troubles de la déglutition (Dysphagie)
Les troubles de la déglutition touchent presque tous les patients parkinsoniens à des degrés divers, et apparaissent souvent dès le début de la maladie.
Les symptômes des troubles de déglutition sont en particulier une mobilité réduite de la langue, une formation difficile du bol alimentaire, une perte du réflexe pharyngé et une contraction pharyngée insuffisante.
La dysphagie a pour conséquences une perte d’appétit du patient entraînant souvent une perte de poids, des difficultés à avaler ses médicaments, Dans les derniers stades de la maladie, elle peut provoquer des « fausses routes », à l’origine de pneumopathies d’aspiration pouvant entraîner le décès du patient.
Enfin, la dysphagie empêche que la salive produite régulièrement par les glandes salivaires soit absorbée automatiquement (de l’ordre de 2000 fois par jour normalement). La salive non absorbée s’accumule alors dans la bouche, et comme le patient a généralement la tête baissée finit par déborder et couler à la commissure des lèvres (bavage).
Le traitement de la dysphagie par l’orthophoniste consiste d’abord à travailler sur un redressement de la posture du patient et une modification de son régime alimentaire.
Ensuite des exercices spécifiques de motricité orale peuvent être proposés au patient pour améliorer la tonicité musculaire. Et associés à la LSVT pour améliorer la fonction de déglutition.
3. Troubles de l’écriture (Micrographie)
Le traitement des troubles de l’écriture fait aussi partie de la compétence de l’orthophoniste.
La micrographie est un trouble de l’écriture souvent présent dès le début de la maladie de Parkinson. Elle se caractérise par une écriture qui devient de plus en plus petite à mesure que la main progresse vers la fin d’un mot ou d’une ligne.
L’écriture peut n’être que légèrement ralentie ou micrographique et rester lisible. Mais elle peut être perturbée au point que la phrase entière soit illisible. Ce trouble a des conséquences négatives sur la vie sociale et professionnelle
En rééducation, l’accent est mis sur l’exagération de l’amplitude du mouvement et la grosseur des lettres à tracer. On peut par exemple, en bougeant le bras et l’épaule, mimer le tracé d’énormes ”0” ou de “8”. Par ailleurs l’orthophoniste dispose d’autres techniques pour ralentir la progression du trouble.
Une session de rééducation peut être faite en 15 séances.
Enfin le patient peut par l’utilisation de certaines recettes (choix de papier quadrillé de crayons et de stylos adaptés ; écriture en lettres détachées de préférence à l’écriture cursive) pallier les inconvénients de la micrographie
Le patient devra s’entrainer à écrire régulièrement, en pensant à ce qu’il fait. Et écrire le plus souvent possible, par exemple il faut qu’il continue à communiquer par écrit avec ses proches.
La narcolepsie vue par le professeur LUDIN du comité consultatif Parkinson suisse
Publié le 13 janvier 2009 à 01:36Article paru dans LE PARKINSONIEN INDÉPENDANT N°35 – décembre 2008
Question d’une lectrice : mon mari souffre du Parkinson depuis quelques années. Il s’en accommode très bien, et moi-même je m’adapte bien à lui et à sa maladie. Cependant, quelque chose me stresse : la narcolepsie. Cela lui arrive le plus souvent au restaurant ou lorsque l’on nous rend visite. Tout le monde panique, veut nous aider ou appeler une ambulance. Je sais que ce n’est pas dangereux, mais je suis tout de même peu rassurée. Devons-nous vivre avec ce handicap ?
Réponse du professeur : Il serait important de m’en dire davantage sur les médicaments pris par le patient et sur sa qualité de sommeil pendant la nuit. Les médicaments contre le Parkinson, en particulier les agonistes de la dopamine, peuvent aggraver la somnolence diurne et également provoquer ce que l’on appelle des crises de sommeil, susceptibles d’avoir des conséquences catastrophiques en particulier au volant d’un véhicule motorisé. Si le patient est traité par agonistes de la dopamine, il conviendrait d’envisager une réduction de la posologie lors de la consultation avec le médecin traitant. Si les médicaments sont responsables de la somnolence décrite, en général l’amélioration ne tarde pas à se manifester. Une mauvaise qualité du sommeil pendant la nuit peut également être à l’origine d’une plus grande somnolence diurne. Malheureusement, les troubles du sommeil sont fréquents chez les Parkinsoniens. Ils peuvent avoir différentes origines. Une analyse approfondie permet souvent de cibler la cause et d’obtenir une amélioration.
Le fait que l’endormissement ait lieu en particulier au restaurant ou lors des visites permet de soupçonner une autre cause possible : chez de nombreux Parkinsoniens, les processus cognitifs sont ralentis. Ils ont ainsi plus de mal à suivre une discussion animée et leurs propres contributions sont souvent trop tardives. Cela peut les inciter à décrocher de la conversation et à s’assoupir. Dans le cas précis, il serait essentiel que tous les participants tiennent compte du ralentissement du patient et le fassent participer activement à la conversation.
Lu dans « PARKINSON Suisse » n°88 par Jean GRAVELEAU
Une découverte fondamentale : Une nouvelle source de neurones dans le cerveau adulte
Publié le 09 janvier 2009 à 06:59Article paru dans LE PARKINSONIEN INDÉPENDANT N°35 – décembre 2008
Lu sur Google, lundi 27 octobre 08
 Des chercheurs de l’Institut Pasteur et du CNRS viennent d’identifier une nouvelle source de production de neurones dans le cerveau adulte. Leurs travaux, publiés dans le Journal of Neuroscience, apportent la preuve des capacités intrinsèques du cerveau à s’auto-réparer. Ils ouvrent ainsi des perspectives inattendues pour le développement de thérapies, notamment pour le traitement des pathologies neurodégénératives, comme la maladie de Parkinson ou la Chorée de Huntington.
Des chercheurs de l’Institut Pasteur et du CNRS viennent d’identifier une nouvelle source de production de neurones dans le cerveau adulte. Leurs travaux, publiés dans le Journal of Neuroscience, apportent la preuve des capacités intrinsèques du cerveau à s’auto-réparer. Ils ouvrent ainsi des perspectives inattendues pour le développement de thérapies, notamment pour le traitement des pathologies neurodégénératives, comme la maladie de Parkinson ou la Chorée de Huntington.
En 2003, alors que les neurobiologistes considéraient depuis toujours que le cerveau et la moelle épinière ne pouvaient se réparer, en cas de lésion ou de maladie, la découverte de cellules souches au cœur du cerveau adulte par Pierre-Marie Lledo et son équipe, à l’Institut Pasteur (unité Perception et mémoire, CNRS URA 2182), avait bouleversé le dogme central en neurobiologie. Les chercheurs avaient en effet montré que certaines cellules non-neuronales, appelées cellules gliales, pouvaient se transformer en neurones, eux-mêmes capables d’intégrer des réseaux cellulaires existants. L’année suivante, la même unité avait identifié une molécule chargée d’attirer ces néo-neurones depuis leur zone de formation jusque dans le bulbe olfactif, une autre région du cerveau.
Aujourd’hui, Pierre-Marie Lledo et son équipe apportent de nouveaux espoirs pour les stratégies thérapeutiques qui visent à réparer le cerveau. En collaboration avec l’unité de Virologie moléculaire et vectorologie, dirigée à l’Institut Pasteur par Pierre Charneau, les chercheurs prouvent en effet que ces cellules souches de type glial, capables de se transformer en neurones, sont localisées non seulement dans la zone de formation qu’ils ont identifiée en 2003, mais également tout le long d’un tunnel dans lequel migrent les nouveaux neurones, ainsi que dans le bulbe olfactif.
Les chercheurs ont pu observer et prouver directement ce phénomène grâce à la mise au point d’un vecteur viral capable de cibler spécifiquement les cellules gliales et de les rendre fluorescentes. Après avoir injecté ce vecteur dans la zone neurogénique déjà connue, puis dans de nouveaux territoires, ils ont constaté que de nombreuses régions du cerveau devenaient fluorescentes, et possédaient donc la capacité unique à produire des neurones.
L’équipe a en outre observé que l’absence de stimulation olfactive, à la suite d’une lésion de l’organe sensoriel, intensifiait la transformation des cellules gliales en neurones. Cette formation des néo-neurones ainsi exacerbée prouve donc que le cerveau possède des propriétés intrinsèques d’autoréparation.
« Ces travaux donnent un nouvel éclairage sur les fonctions réparatrices du système nerveux central, souligne Pierre-Marie Lledo. En détournant des neurones nouvellement formés depuis leur zone germinative vers les régions lésées, on pourrait en effet espérer contribuer à élaborer de nouvelles stratégies thérapeutiques, pour le traitement des pathologies neurodégénératives comme la Chorée de Huntington ou la maladie de Parkinson ».
Source : CNRS (Ct Nal RecherchesScientifiques)
Maladie de Parkinson et souffrance psychologique
Publié le 09 janvier 2009 à 06:43Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
Samedi 11 février, devant une assemblée d’environ 80 personnes, le Dr Laurence AUTRET, psychiatre, nous a dressé un tableau de la souffrance psychologique dans la Maladie de Parkinson, avec des mots simples, en partant du vécu. Le but de la démarche peut se résumer ainsi : « mieux se connaître, pour mieux agir ».
Après une description des troubles psychiques possibles dans la Maladie de Parkinson, de leur fréquence, le cas de la dépression a été abordé avec ses symptômes et la difficulté du diagnostic chez le malade parkinsonien. S’en est suivi un chapitre sur les conséquences de ces troubles neuropsychiatriques, leurs origines, et la question : « que faire quand la souffrance est là ? ». Le Dr Laurence AUTRET a proposé des conseils au quotidien et abordé les situations de crise.
Dans la symptomatologie psychiatrique de la M.P, on reconnaît, les troubles de l’humeur comme la dépression, les troubles anxieux, les troubles du sommeil, les hallucinations, les états délirants (jalousie, peur du complot…), les troubles de conduite (impulsivité, agressivité, dépendance à la L‑Dopa…), les troubles compulsifs (jeux, hyper sexualité…).
60% des malades parkinsoniens sont confrontés un jour ou l’autre, à une de ces formes.
Dans 25% des cas, on rencontre des troubles cognitifs. Cela peut se traduire par : la perte de la notion d’espace, des troubles de la concentration, de la mémoire, la difficulté à gérer deux choses à la fois, à suivre un raisonnement complexe, une lenteur dans les réactions, une moindre initiative, une hyperémotivité…, mais une grande variabilité selon les moments.
Les troubles dépressifs touchent 40% des parkinsoniens contre 6% à 12% pour l’ensemble de la population. 70% des parkinsoniens contre 30% de la population connaîtront la dépression. Dans certains cas la dépression précède les premiers signes de la maladie.
Quelques questions qui orientent vers la présence d’une dépression :
Pour le malade :
- Vous sentez-vous globalement insatisfait de votre vie ?
- Ressentez-vous un vide à l’intérieur de vous ?
- Diriez-vous que vous êtes plutôt malheureux, plutôt inquiet ?
- Avez-vous laissé de côté des activités ?
- Pleurez-vous pour un rien ?
- Avez-vous tout le temps l’impression que les autres y arrivent mieux ?
Et pour l’entourage :
- Avez-vous l’impression que le malade en demande parfois trop ? De vous mettre en colère ou d’être gêné par le comportement du malade ?
- Avez-vous l’impression de n’avoir plus de temps à vous ? Que vos relations se détériorent ? Que vous perdez la santé ?
- Avez-vous peur de l’avenir ?
- Avez-vous l’impression de ne pas être à la hauteur, qu’il faudrait faire mieux ou plus ?
Dans la dépression, c’est toute la personne qui est atteinte. Cela se traduit par des signes psychiques et physiques, des changements de comportement intenses et durables (douleur morale, hypersensibilité, honte, culpabilité, angoisse, confusion, ralentissement psychophysique, perte de l’appétit, perte du goût des choses, irritabilité, impossibilité à se relaxer…).
Quand on suspecte une dépression, il faut en parler au médecin, mais il y a toujours une grande difficulté pour la personne à reconnaître qu’elle souffre d’une dépression. Il s’agira donc de poser la question indirectement : « Tu n’es plus comme avant », y revenir progressivement et amener la personne à faire une démarche, sans jamais prendre un rendez-vous à sa place, ni la mettre devant le fait accompli.
Les conséquences des troubles neuropsychiatriques :
- altération de la qualité de vie
- altération de la relation à l’autre (vie commune, vie de couple)
- retrait social, isolement
- conséquences morales et judiciaires (jeux, sexualité)
- risque suicidaire dont le diagnostic est difficile car les intentions ne sont pas exprimées. Il n’y a pas de surreprésentation statistique chez les parkinsoniens en général, cependant il est constaté un taux anormalement élevé chez les neurostimulés. Depuis peu, une équipe de chercheurs se penche sur cette problématique.
Le diagnostic de la dépression est rendu plus difficile chez les parkinsoniens car on retrouve des symptômes communs avec la M.P.
A retenir, les troubles psychiques font partie de la M.P., et il faut en parler, ne pas avoir honte, les médecins connaissent les troubles et peuvent les évaluer.
L’origine des troubles neuropsychiatriques :
- origine neurologique : les dysrégulations dopaminergiques et des modifications structurales des noyaux de la base
- origine iatrogène, due aux médicaments qui peuvent entraîner des effets de dépression, des hallucinations
origine dégénérative, due au vieillissement, avec des lésions anatomiques cérébrales. - origine psychique, les difficultés liées au vécu de la maladie et du handicap ont des incidences sur le psychisme et engendre un sentiment de perte : perte de contrôle sur ce qui arrive, incapacité à travailler d’où blessure identitaire, perte de l’estime de soi (« on ne vaut pas grand-chose »), perte de la libido, perte d’autonomie…
Alors que faire ?
- Se soigner, consulter, car on ne peut pas s’en sortir seul quand on est dépressif. Dans un premier temps, soigner la M.P., traiter les symptômes, trouver le meilleur traitement, surveiller les effets secondaires. Puis, traiter la dépression avec des médicaments psychotropes et anxiolytiques. Attention, il n’y a pas d’effet immédiat, il faut surveiller les précautions d’emploi, respecter les prises et les durées et persévérer dans le traitement.
- Chercher un soutien psychologique, dans l’entourage, à travers le réseau de soin (médecin traitant, neurologue, pharmacien, orthophoniste…), les groupes d’entraide (associations)., Mais aussi rencontrer un « psy », interlocuteur neutre et bienveillant qui peut entendre des confidences que l’on ne peut pas toujours faire à l’entourage. Exprimer sa souffrance, c’est s’autoriser à reconnaître ses émotions, à envisager des solutions, à relativiser, à se déculpabiliser. Seulement 5% des personnes acceptent de se faire aider
Conseils au quotidien :
- S’informer sur la maladie, mais pas trop, et ne chercher que ce qui nous intéresse. Connaître donne le sentiment de contrôler. La fiabilité des informations doit être validée par le médecin. Ne pas hésiter à demander des explications simples au neurologue.
- Respecter ses limites et celles de l’autre. La maladie entraîne une perte de l’énergie vitale d’où une moindre disponibilité. Réduire les autres « pertes » d’énergie, chercher activement ce qui nous intéresse. N’entreprendre qu’une chose à la fois. Fractionner les tâches. Faire des pauses souvent. Rechercher, privilégier une ou des activités en dehors de chez soi – l’extérieur est une stimulation – Savoir s’arrêter quand on est fatigué (pas évident !).
- Revoir ses priorités. Où est mon essentiel ? Se « débarrasser » du sens du devoir, d’un système de valeur arbitraire qui repose sur l’image que l’on veut donner. Rechercher la paix avec soi-même.
- Reconnaître sa valeur humaine. Se connaître, être bienveillant avec soi-même. Savoir exploiter ses potentialités différentes. Ne pas se comparer aux autres. Admettre le changement. En parler pour cesser de se dévaloriser. Malade oui, mais adulte responsable.
- Accepter le négatif. Les émotions négatives c’est une plainte intérieure, une souffrance, le signe que quelque chose ne va pas. Dépasser la culpabilité. La vie continue son cours, on n’a pas à être ménagé. Il y aura forcément des moments difficiles. Savoir passer à autre chose. Surtout, ne pas s’isoler.
- Se préserver l’environnement. Faire des aménagements concrets pour se faciliter la vie. La constance des repères procure un sentiment de sécurité. Veiller à la régularité des prises des médicaments surtout des psychotropes.
- Se préserver le temps. Chaque jour, on a 24 h pour « caser » ses besoins. Le temps libre se décide, se planifie. Privilégier les sorties. Rechercher le plaisir dans les activités. Gérer l’emploi du temps, lister les taches fixes (toilette, courses) réviser la fréquence, revoir les « us et coutumes », prévoir des marges. Renoncer n’est pas démissionner, c’est mieux de s’investir dans l’essentiel, laisser le superflu et éviter de se mettre la pression. Rechercher la qualité plus que la quantité.
- Demander de l’aide. C’est une démarche difficile, cela suppose de reconnaître ses faiblesses, c’est prendre le risque du refus de l’autre. Demander de l’aide, n’est pas capituler, mais une démarche active pour durer. Déléguer n’est pas se décharger de ses responsabilités, c’est se décharger du superflu. Redistribuer les rôles, n’est pas perdre de l’importance, c’est renforcer la solidarité. Personne n’ose contester l’omniprésence de l’aidant, mais il faut savoir la remettre en cause ; tous les couples ont besoin de « respirer » l’un sans l’autre. Accepter l’imperfection et toujours chercher des solutions.
- Savoir profiter de la vie. Avoir toujours un projet d’avance, et le désir d’aller de l’avant. Chercher la compagnie des vivants. Trouver des alternatives pour diminuer les frustrations. Les stimulations extérieures sont généralement bénéfiques sur les symptômes de la M.P.
- Enrichir sa vie de couple. Avoir un but commun, le bien-être de chacun, ensemble. Devenir aidant n’a rien de naturel, éviter de n’être que le garde malade, on est avant tout un aimant et un aimé. La dépendance a des aspects multiples, on a besoin l’un de l’autre mais sur des plans différents. Nécessité de se ménager l’un et l’autre. Ne pas tomber dans la surenchère : malaise/culpabilité. Encore une fois, rechercher la qualité et préserver l’atmosphère de la relation. L’ambiance dans laquelle sont faites les choses compte plus que le résultat.
Les situations de crises :
- l’impossible acceptation, la maladie est une injustice,
- le renoncement à une certaine idée de la vie,
- Les problèmes de sommeil mettent le couple à l’épreuve, jours et nuits sont envahis.
- la modification de la libido déstabilise l’intimité du couple
- la peur de perdre l’autre,
- la « surveillance » justifiée par « c’est pour ton bien »,
- les phases OFF, périodes d’aggravation,
- les situations à risque.
Continuer quand même.
Pour chaque chose, chercher une solution, revoir les objectifs, renoncer, trouver une suppléance, changer tout ce qui peut être changé et surtout demander de l’aide.
Conclusion
La Maladie de Parkinson induit des troubles psychiques, et il faut en tenir compte dans la vie quotidienne et pour mieux communiquer. Il n’y a pas de honte, et cela fait partie de la maladie. Il est important d’en parler avec son médecin, avec des personnes de confiance.
Vivre avec la maladie de Parkinson, c’est un défi au quotidien. La personne est « tombée malade », l’entourage est « tombé aidant » et le mot d’ordre c’est le bien-être de chacun ensemble et pour longtemps. Chacun est seul maître à bord de son navire, jusqu’au bout. L’être humain est, avant tout, un être sensible au sentiment de dignité.
Rédigé par Guy SEGUIN
Lutter contre les périodes sombres
Publié le 09 janvier 2009 à 06:06Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
Par Johannes KORNACHER, Lu dans le « PARKINSON Suisse » N°88
Chez les Parkinsoniens, le risque de dépression est élevé. Elle a des origines chimiques et psychiques. S’il est aidé par le malade et son entourage, le médecin a les moyens de l’endiguer.
Une fois de plus, Heinz F. a l’impression de tout faire de travers. Aujourd’hui, au volant de sa voiture automatique, il est entré en marche avant dans la porte de son garage, persuadé que la marche arrière était encore enclenchée après un moment d’inattention. « C’est tout moi. Depuis que je souffre du Parkinson, la guigne me colle aux basques », pense-t-il. Heinz F. a le sentiment d’être responsable de tous ses malheurs. Il considère sa maladie comme une punition.
Tout le monde le contredit. Toutefois Heinz F. ne souffre pas seulement du Parkinson. Il est également dépressif. On ne peut rien lui dire ; actuellement, il vit dans ce que l’on appelle une spirale de pensées négatives. Le principe est le suivant : le Parkinsonien pense par exemple : « Je ne peux plus rien faire correctement », puis : « Je préfère ne pas essayer » et enfin conclut en constatant son échec : « Rien ne va plus ». Ces derniers mois, Heinz F. s’est empêtré de plus en plus dans une spirale de pensées négatives. Chez le médecin, il se ressaisit, mais la remarque suivante lui échappe cependant : « Je fais tout de travers ».
Souvent, comme c’est le cas pour Heinz F., les dépressions accompagnant la maladie de parkinson sont d’origine psychoréactive. Il s’agit de réaction à la maladie. Par exemple, alors que les handicaps physiques altèrent la qualité de vie : « on veut continuer à tout faire comme avant », indique Joachim Kohler, ancien neurologue. « En réalité, on n’accepte pas la maladie ». La dépression remplace la colère, la rage ou la tristesse. Souvent on minimise le Parkinson dès la phase de démarrage. On met en doute la gravité de la nouvelle situation et on refuse toute aide. Les spécialistes rapportent qu’au cours de cette phase, cinq pour cent tout au plus des Parkinsoniens acceptent une aide psychologique. Cependant, ils doivent assimiler un point capital : la perte de leur ancien mode de vie.
Près de la moitié des Parkinsoniens développent une dépression. Il ne s’agit d’une réaction émotionnelle à la maladie que pour une partie d’entre eux. Souvent, les symptômes dépressifs accompagnant le Parkinson se manifestent par un déséquilibre de différents messagers chimiques et par la dégénérescence des liaisons nerveuses dans le cerveau. Les dépressions préexistent fréquemment à l’apparition des premiers symptômes visibles du Parkinson. Les médecins le savent depuis longtemps.
Cependant, ces derniers temps, on prête davantage attention aux dépressions. « Auparavant, les problèmes moteurs figuraient au premier plan », déclare le neurologue Stephan Hägele, médecin à l’hôpital cantonal de Saint-Gall. L’objectif thérapeutique principal consistait à éviter les fluctuations des performances motrices et les dyskinésies. « Aujourd’hui, nous savons que les symptômes non moteurs tels que la dépression jouent un rôle encore plus important pour la qualité de la vie ». Entre-temps, les dépressions accompagnant la maladie de Parkinson ont fait l’objet de recherches et l’on dispose désormais de davantage de conclusions certaines, qui sont intégrées au traitement. Le thème de la dépression était-il négligé ? « Souvent, on ne l’a pas discernée car de nombreux symptômes visibles du Parkinson sont identiques à ceux de la dépression, comme par exemple l’expression du visage et le ralentissement », explique le docteur Hägele. Par ailleurs, les patients informent rarement leur médecin de leur état émotionnel. Si celui-ci ne pose pas de questions ciblées, la dépression peut passer inaperçue.
Le dialogue avec le médecin est décisif pour le diagnostic et le traitement. Il en va de même pour le partenaire et pour les proches. Ils peuvent faire part au médecin de leurs observations et de leurs expériences, notamment d’un récent changement de l’expression du visage ou de certaines déclarations du patient, ou lui indiquer au cours de quelle phase les états dépressifs se manifestent, par exemple en phase off. « La contribution des proches peut s’avérer précieuse lors de l’anamnèse », déclare le docteur Hägele. Cependant, le patient peut également s’observer et donner des indications à son médecin. Ce dernier doit alors l’interroger : « Ressentez-vous une sensation de vide ? Vous est-il impossible de vous réjouir véritablement ? Avez-vous déjà vécu des périodes dépressives ? ».
Les dépressions des Parkinsoniens représentent un grand facteur de stress pour leurs partenaires également. Ils doivent trouver le juste milieu, encourager et inciter leur partenaire à s’activer sans toutefois le soumettre à un effort excessif. Parallèlement, ils ne doivent pas se mettre complètement en retrait, mais affirmer leurs besoins et leurs sentiments. Sous la pression, ils peuvent également finir par entrer en dépression. S’entretenir avec des personnes de confiance et des spécialistes peut aider à mieux s’en tirer.
L’aide du partenaire est d’une importance capitale, en particulier pour la stratégie non médicale du traitement ou de la prévention de la dépression. L’activité, la physiothérapie, la distraction, les contacts sociaux, les jeux, la culture : en cas de dépression, tout cela n’a plus grande efficacité. La motivation du partenaire peut activer beaucoup de choses. Le neurologue Stephan Hägele le sait, « Le rafraîchissement mental fait également partie du traitement ». « Une personne qui pratique régulièrement un sport, par exemple, se sent assurément mieux ». Dans le sport, le patient contrôle beaucoup de choses et peut faire ce qui lui plaît. Le bien-être psychique s’en trouve favorisé, car l’autonomie, limitée par la maladie, est renforcée. Malgré le petit nombre d’études à ce sujet, on présume que la physiothérapie aide à lutter contre les dépressions et peut contribuer à briser le cercle vicieux.
Naturellement, le traitement de la dépression peut être médicamenteux. « Il s’agit avant tout d’optimiser l’ajustement dopaminergique », retient M. Hägele. Pour ce faire, on peut avoir recours aux antidépresseurs. Un Parkinsonien dépressif doit cependant faire preuve de patience et se préparer à l’apparition d’éventuels effets secondaires avant l’action antidépressive. « C’est pénible », déclare M. Hägele. L’effet dure au moins trois semaines, parfois plus longtemps. Il recommande vivement de ne pas interrompre trop tôt, mais d’adapter la dose progressivement.
Les dépressions constituent un symptôme typique du Parkinson, déclare M. Hägele : « Nous n’en savons pas encore suffisamment », concède – t‑il. « Cependant nos progrès sont remarquables depuis que nous accordons une plus grande importance à la dépression en cas de Parkinson, qui fait l’objet de davantage de recherches ». Lorsque le patient collabore et parle de ses problèmes avec son médecin, les chances de vaincre la dépression sont grandes. Heinz F. a appris à vivre avec sa maladie au cours d’une psychothérapie par entretien de plusieurs semaines. Depuis il va beaucoup mieux. Malgré ses handicaps, il prend de nouveau plaisir à vivre : « Je suis heureux que la période sombre soit passée ».
Lu par Jean GRAVELEAU
L’excès de fer origine du Parkinson ?
Publié le 08 janvier 2009 à 07:31Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
« Limiter l’excès de fer dans les neurones dopaminergiques pourrait protéger contre la maladie de Parkinson ». Voilà comment commence le communiqué de l’Inserm en référence à l’étude menée par Etienne HIRSH, directeur de recherche au CNRS, et par son équipe de l’unité mixte 67. L’étude appelée « Neurologies et Thérapeutique Expérimentale » signée Inserm-UPMC (université Pierre et Marie Curie) a été publiée dans la revue scientifique PNAS (Proceeding of the National Academy of Sciences) le 27 Octobre dernier.
Il en ressort après des tests effectués sur des souris que l’excès de fer serait à l’origine de la mort de neurones. Les chercheurs sont partis du constat que les personnes décédées des suites de la maladie de Parkinson, comportent dans leur cerveau des neurones contenant un excès de fer.
Ils ont donc utilisé des souris pour mieux comprendre le phénomène et tenter de trouver l’origine de ce problème. Les recherches se sont orientées vers le DMT1 chargé de transporter le fer vers le cerveau. Pour la première phase de leurs travaux ils ont introduit chimiquement la maladie de Parkinson sur des souris et ont constaté que les DMT doublaient et donc augmentaient l’arrivée de fer dans les cellules du cerveau, un à deux jours après l’injection. Il s’en suit « un stress oxydatif » entraînant la mort neuronale seulement cinq jours après.
Ensuite, les chercheurs ont inhibés ces DMT1. En introduisant une toxine provoquant la maladie de Parkinson, le constat est très explicite : « Les souris malades chez qui ce transporteur est inhibé résistent beaucoup mieux à la maladie. Ces résultats sont très concluants. Nous avons montré qu’en inhibant l’activité du transporteur DMT1, nous protégions les rongeurs contre la maladie » indique Etienne HIRSH.
Cela est donc une avancée qui semble importante dans le domaine de la recherche contre la maladie de Parkinson.
L’INSERM rappelle que « la Maladie de Parkinson représente la seconde affection neurodégénérative après la maladie d’Alzheimer ».
Lu dans INFOS.com du 31 octobre 2008
Par Françoise VIGNON
La Rasagiline : un nouvel espoir pour limiter la progression de la maladie ?
Publié le 08 janvier 2009 à 07:25Article paru dans LE PARKINSONIEN INDEPENDANT N°35 – décembre 2008
Un récent essai clinique suggère que la Rasagiline (Azilect) pourrait limiter la progression de la maladie de Parkinson.
Un essai clinique de phase III qui a été conçu pour évaluer si la Rasagiline (commercialisé sous le nom d’Azilect) pouvait ralentir la progression de la maladie de Parkinson a montré un grand succès. Les premiers résultats de l’étude ont indiqué des avantages de la Rasagiline si le traitement est pris à un stade précoce de la maladie. Les résultats sont plus mitigés si le médicament est pris dans les phases plus avancées de la maladie. Cela est le premier essai clinique de cette envergure, en double aveugle qui montre l’efficacité d’un médicament qui peut freiner la progression de la maladie.
La Rasagiline est un puissant inhibiteur irréversible de la monoamine oxydase de type B (MAO‑B). La Rasagiline et ses analogues font aussi l’objet d’une étude pour le traitement de la maladie d’Alzheimer. Selon des chercheurs, la Rasagiline améliorerait aussi la mémoire et les capacités d’apprentissage. La Rasagiline pourrait aussi améliorer l’humeur, la motivation et le déclin de la mémoire durant le vieillissement.
Les signes déclarés de la maladie de Parkinson sont associés à une perte de 80% ou plus de neurones dopaminergiques de la substance noire du mésencéphale. Certains chercheurs pensent que tout le monde est amené à développer des symptômes parkinsoniens si nous vivons assez longtemps. Cette hypothèse peut s’expliquer par la perte disproportionnée de cellules dopaminergiques à chaque décennie de notre vie d’adulte. L’augmentation du catabolisme de la dopamine est aussi associée au stress oxydatif et à la mort neuronale.
Les inhibiteurs de la MAO‑B retardent ce processus, mais les mécanismes moléculaires de neuroprotection de la Rasagiline semblent être indépendants de l’inhibition de la MAO‑B. En effet, l’isomère de la Rasagiline, TVP1022, a des effets neuroprotecteurs similaires mais n’est pas un inhibiteur de la MAO‑B, ce qui suggère que l’effet neuroprotecteur de la Rasagiline n’est pas lié à la fonction inhibitrice de la MAO‑B.
Les facteurs responsables de l’effet du médicament restent encore à élucider. Selon des études, la Rasagiline augmenterait la quantité de la protéine de survie cellulaire BCL2 et dans le même temps réduirait la quantité de molécules destructrices comme BAX, BAD et BIM. La Rasagiline limiterait aussi la perméabilité des mitochondries, un signe précoce de la maladie. De plus, des études préliminaires suggèrent que la Rasagiline augmenterait aussi les taux de facteurs neurotrophiques BDNF et GDNF lesquels favorisent la neurorégénération.
En inhibant la MAO‑B, la Rasagiline limite le désamination des deux monoamines que sont la dopamine et la phénethylamine, en augmentant ainsi leur concentration dans la synapse et en réduisant la production des espèces oxygénées réactives. En effet, de fortes concentrations de peroxyde d’hydrogène sont associées à l’augmentation du stress oxydatif. Ainsi, la Rasagiline augmente à la fois le niveau de dopamine dans le striatum (en synergie avec la levodopa) mais aussi améliore la survie des neurones dopaminergiques eux-mêmes. Cet effet salvateur permet de restituer une locomotion normale et une coordination des mouvements chez le patient parkinsonien.
Les avantages de la Rasagiline, tant en monothérapie qu’en co-traitement avec la levodopa, s’étendent au-delà de la restitution de l’activité motrice. La Rasagiline améliorait aussi modestement la performance cognitive et suggère un rôle dans l’amélioration de la fonction de cholinergique mais dont le mécanisme d’action reste encore obscur.
La Rasagiline a été d’abord synthétisée et développée par le professeur Moussa YOUDIM un chercheur israélien d’origine iranienne, professeur de pharmacologie à la Faculté de Médecine Technion-Rappaport d’Haïfa. Le médicament est produit par la compagnie pharmaceutique Teva Neurosciences sous le nom de marque Azilect. Le 16 mai 2006, une Autorisation de mise sur le marché (AMM) a été accordée aux Etats-Unis à Azilect. La FDA (American Food & Drug Administration) a approuvé Azilect tant en monothérapie dans les phases précoces de la maladie qu’en thérapie conjointe à la levodopa dans le traitement des formes plus avancées.
En Europe, Azilect est co-produit par le géant du médicament danois Lundbeck. La Rasagiline est devenu disponible au Royaume-Uni en juin 2005. D’autres pays de la communauté européenne ont rapidement suivi.
A ce jour en France, l’Azilect a reçu une autorisation de mise sur le marché mais n’est pas encore disponible, « faute d’accord sur le prix de vente », souligne le Panorama du Médecin.
Le professeur YOUDIM croit que dans quelques années nous pourrons mélanger une cuillerée de ce médicament dans nos céréales quotidiennes pour protéger le cerveau des maladies neurodégénératives. « Peut-être à l’avenir prendrons-nous un cocktail de comprimés neuroprotecteurs pour retarder le processus de vieillissement lui-même ». Le professeur YOUDIM s’avère sans doute très optimiste ; mais ni la sénescence ni les maladies liées à l’âge ne sont inévitables.
En savoir plus : http://www.tevapharm.com/pr/2008/pr_782.asp
Dr Benoît Melchior,
La Jolla Bioengineering Institute,
La Jolla (CA) USA.
Vivre plus longtemps chez soi
Publié le 09 octobre 2008 à 15:43Paru dans LE PARKINSONIEN INDÉPENDANT N°34-septembre 2008
Source : l’Information Service Malakoff Méridic Septembre 2008
Aujourd’hui, nous comptons1,3 million de Français de plus de 85 ans , ils devraient être 2 millions en 2015 ; la question de perte d’autonomie est désormais cruciale.
Vivre le plus longtemps possible chez soi pour le bien-être mais aussi pour la pérennité du système de protection sociale, tel est l’enjeu… Des solutions existent, à mettre en place dès que nécessaire.
Quelques conseils pour vivre plus longtemps chez soi :
- se faire aider : penser aux livraisons des courses proposées par les supermarchés ou les associations de quartiers. La livraison ou la préparation de repas à domicile est généralement un grand soulagement pour les personnes fatiguées.
- Utiliser les chèques emploi service universels (Cesu) pour certains gestes quotidiens qui sont devenus pénibles : ménage – petits travaux de bricolage ou de jardinage. L’utilisation de ces chèques permet une simplification des démarches déclaratives mais aussi de bénéficier des avantages fiscaux liés à l’emploi d’une aide à domicile (50% des dépenses engagées dans la limite d’un plafond annuel). Le Centre Communal d’Action Sociale (CCAS) de votre ville pourra vous fournir de plus amples renseignements.
- Prendre soin de soi : faire une (ou des) marche chaque jour – Manger varié et équilibré – boire beaucoup d’eau et je dirais ne pas abandonner la coquetterie … (Jacqueline).
- Garder le contact : entretenir une vie sociale. La vie associative représente un tissu dans lequel vous pouvez vous impliquer et éviter l’isolement qui touche certains inactifs.
- Des outils pour se rassurer : lorsque les risques de chutes s’accentuent, il peut être rassurant d’investir dans un dispositif de téléassistance. Celle-ci eut être active ou passive, allant du simple bouton sur lequel on appuie en cas de problème, au détecteur électronique de chute (bracelet actimétrique1 qui prévient un service médical en cas d’absence suspecte de déplacements de la personne). Par ailleurs les distributeurs électroniques de médicaments permettent d’éviter les oublis de prises médicamenteuses.
Les alternatives à l’hospitalisation : la maladie amène souvent à un suivi médical ou à âtre assisté en permanence dans les tâches quotidiennes. Mais cette prise en charge ne signifie pas un passsage brutal du domicile à la maison de retraite.. Des solutions intermédiaires existent : l’hôpital de jour par exemple. Quant à l’hospitalisation à domicile, elle permet d’âtre suivi médicalement chez soi, après accord du médecin traitant et de la famille et si le logement est jugé adapté. Pour en savoir plus adressez-vous à votre médecin ou à l’Agence Régionale de l’Hospitalisation (ARH). - La maison de retraite à temps partiel — Possible dans certaines maisons de retraite : Accueil de jour – Accueil lorsque la famille part en vacances ou lorsqu’un événement survient et oblige à un accueil temporaire de quelques semaines ou quelques mois. Une partie de ces frais peut être prise en charge par l’APA.
Dans tous les cas, entre les premiers signes de la dépendance et le besoin constant de soins, il existe de nombreux paliers. Le mieux est de se renseigner le plus tôt possible auprès de la Direction Départementale de l’Action Sanitaire et Sociale (DDASS) ou du Centre Loal d’Information et de Coordination (CLIC) de votre département.
Lu par Jacqueline GEFARD-LE BIDEAU
1L’actimétrie est la mesure et l’enregistrement des mouvements corporels pendant plusieurs jours, et, par extension, l’analyse de l’activité d’une personne
Quelles Aides pour le maintien à domicile ?
Publié le 08 octobre 2008 à 14:01Paru dans LE PARKINSONIEN INDÉPENDANT N°34-septembre 2008
Source : l’Information Service Malakoff Méridic Septembre 2008
Depuis que le gouvernement a lancé le plan Solidarité Grand Age en 2006, les aides publiques en faveur du maintien à domicile sont de plus en plus axées sur l’offre de services à la personne et le soutien aux familles aidantes.
L’an dernier, selon une étude de la DREES (Direction de la Recherche des Etudes de l’Evaluation et des Statistiques), 60% des bénéficiaires de l’Aide Personnalisée à l’Autonomie (APA) vivaient à domicile, contre 40% en Etablissements d’Hébergement pour Personnes Agées (EHPA)
Attribuée par le Conseil Général, cette aide s’adresse aux 60 ans et plus, ayant besoin d’un soutien pour les tâches quotidiennes. Elle n’est pas soumise à conditions de ressources, mais son calcul tient compte des revenus des bénéficiaires ainsi que de leur degré de dépendance, évalué lors d’un entretien. Elle peut être accordée aux personnes vivant chez elles, mais aussi aux proches qui les assistent. En effet, pas moins de 26% des personnes les plus dépendantes sont prises en charge par leurs familles.
En faire la demande auprès du Centre Communal d’Action Sociale (CCAS) de votre ville.
DES ALTERNATIVES à L’APA
Si l’APA vous est refusée vous pouvez en revanche recevoir l’Aide Sociale aux Personnes Agées, pour de nombreux services : aide aux repas, ménage, bricolage, aide aux déplacements…Vous en bénéficiez si vos ressources annuelles sont inférieures à 7.719,52 € pour une personne seule et à 13.521,27 € pour un ménage (allocation logement et retraite du combattant non comprises). S’adresser au CCAS.
Si vos ressources sont supérieures à ces montants, vous pouvez en bénéficier par l’intermédiaire de votre caisse de retraite.
Par ailleurs, un dense réseau de bénévoles est disponible pour vous soulager : l’Aide à domicile en milieu rural (ADMR), un maillon d’associations au service de la personne qui représente plus de 100.000 bénévoles en France.
Voir ADMR – 184 A rue du Faubourg Saint-Denis – 75010 PARIS – Tél 01 44 65 55 55
Internet : www.admr.org
Pour en savoir plus sur les aides à domicile :
Agence Nationale des Services à la Personne – 3 square Desaix – 75015 PARIS –
tél 01 45 78 26 90
Internet : www.servicesalapersonne.gouv.fr
Lu par Jacqueline GEFARD-LE BIDEAU
Informations sociales : Dispositif de soutien au départ en vacances des aidants familiaux
Publié le 07 octobre 2008 à 08:42Paru dans LE PARKINSONIEN INDÉPENDANT N°34 – septembre 2008
Source « Vacances Ouvertes » Région Poitou Charentes
CONTEXTE
En 2006, la Région Poitou-Charentes a souhaité confier à Vacances Ouvertes une étude sur l’accompagnement au départ en vacances des personnes qui sont en situation dite « d’aidant », c’est-à-dire les personnes de la famille ou de l’entourage proche qui interviennent quotidiennement dans l’aide ou le soutien à une personne âgée. Il apparaît que ce public est susceptible d’un soutien spécifique au départ en vacances pour deux raisons :
- il est essentiellement constitué de personnes retraitées ayant des revenus limités
- ces personnes sont très souvent exclues des vacances.
Pour 2008, Vacances Ouvertes propose donc les jalons d’un dispositif expérimental d’aide au départ pour les aidants familiaux de la région Poitou-Charentes.
INTÉRETS DU SOUTIEN AUX AIDANTS FAMILIAUX
Le soutien aux aidants familiaux est, pour de nombreuses raisons, indispensable aujourd’hui.
D’abord soutenir les aidants permettrait de limiter les coûts des politiques vieillesse. Le maintien à domicile des personnes âgées est très directement lié à l’accompagnement quotidien assuré par leurs proches.
Ensuite, l’aide apportée par les proches est différente et complémentaire de celle apportée par les professionnels. Elle ne se réduit pas à l’accomplissement de gestes techniques mais est un signe de la vivacité du lien intergénérationnel, constitutif de la construction identitaire des individus, et donc, des sociétés qu’ils forment. Le soutien aux aidants familiaux participe donc à la construction sociale.
Enfin, il s’agit de soutenir les aidants car ils constituent un public fragilisé à risque. La prise en charge d’une personne âgée a un impact sur la santé physique et psychologique de l’aidant. Il existe une véritable pathologie de l’aidant : asthénie croissante, surmenage, insomnies, stress, dépression, risque plus élevé de pathologies cardio-vasculaires et cancéreuses.
Au plan social, les aidants familiaux souffrent d’isolement et de solitude, ont des activités de loisirs réduites et des risques plus importants de difficultés financières. Or, il est nécessaire de préserver la santé physique et psychique des aidants pour permettre qu’ils restent aidant.
Le soutien aux aidants familiaux est non seulement le garant de solidarités intergénérationnelles ou de liens sociaux mais implique aussi des solutions d’allégement en termes de politique vieillesse et de prise en charge financière de nos personnes âgées.
LÉGITIMITÉ D’UN PROJET VACANCES
S’il est indispensable d’encourager la reconnaissance des aidants familiaux, il est primordial de prendre en compte leur besoin de répit.
Les aidants ne s’autorisent pas à penser aux vacances car ils n’envisagent pas de solution de remplacement satisfaisante auprès de la personne âgée qu’ils soutiennent. Par ailleurs, ils ne savent pas toujours où s’adresser.
Quatre réponses peuvent être apportées à la question : « Pourquoi des vacances pour les aidant familiaux ? »
Les interrogations, les craintes et résistances visées dans les actions d’aide aux aidants peuvent apparaître en périphérie d’un projet destiné à l’aidant. Il paraît plus facile d’accompagner l’aidant sur ces questions par le biais d’un projet dynamique qui le concerne.
La mise en œuvre d’un projet vacances, dans l’objectif de soulager les aidants, repose sur un levier puissant : celui du plaisir.
La loi du 29 juillet 1998 relative à la lutte contre les exclusions stipule que « l’égal accès de tous, tout au long de leur vie (…) aux vacances et aux loisirs constitue un objectif national ». Pour cette seule raison, l’aide au départ en vacances des aidants familiaux, public manifestement exclu des vacances, est légitime.
Enfin, ce soutien permet de donner un contenu à la notion de « droit au répit ». Les aidants se sentent souvent coupables de revendiquer du temps pour eux. Bien plus que du répit, les aidants familiaux ont besoin de temps pour eux.
ACTIONS PROPOSÉES PAR VACANCES OUVERTES
Les aidants intéressés doivent contacter Vacances Ouvertes qui pourra leur proposer plusieurs types d’accompagnement selon leurs besoins :
Une aide logistique dans la recherche d’une éventuelle solution de remplacement pour la personne aidée (principalement mise en relation avec le CLIC — Centre Local d’Information et de Coordination) et dans la recherche d’un lieu de vacances. Une aide financière, versée sous conditions de ressources.
Les aidants construisent ensuite leur projet de vacances (liberté quant au type de séjour, à la destination, …).
Vacances Ouvertes peut également soutenir des structures qui prévoient des séjours collectifs avec des aidants (ou des aidants et les personnes aidées) ou qui envisagent simplement d’accompagner des aidants dans la construction d’un projet vacances.
CONCLUSION
La nécessité de soutenir les aidants est désormais admise par tous.
Ces soutiens se heurtent encore trop souvent, malheureusement, à un écueil majeur : celui de convaincre les aidants de bénéficier de l’action.
Vacances Ouvertes cherche donc à mettre en place un dispositif simple d’accès, adapté et concret dont l’objectif principal est de permettre aux aidants un temps de répit, de prendre du temps pour soi.
Proposer un projet vacances comme outil a une action d’aide aux aidants ne va pas de soi. il s’agit d’une approche radicalement nouvelle de l’aide aux aidants. A ce titre,
MONTER UN PROJET DE VACANCES POUR LES AIDANTS FAMILIAUX RELÈVE D’UNE VÉRITABLE INNOVATION SOCIALE.
Transmis par Raoul Griffault
Une approche intéressante de la maladie
Publié le 06 octobre 2008 à 08:59Paru dans LE PARKINSONIEN INDÉPENDANT N°34 – septembre 2008
Nous avons en son temps fait part de notre lecture de l’ouvrage de Thierry Janssen intitulé « La solution intérieure » paru chez Fayard (Le Parkinsonien Indépendant n°30 de septembre 2007)
Son approche de la maladie est suffisamment originale pour nous donner quelques clés et nous aider à trouver nos propres solutions à toutes formes de maladie.
Dans une interview orale sur Internet, il exprime clairement son point de vue, qui peut nous donner espoir dans une réduction de nos difficultés si nous essayons de suivre ses conseils.
Si vous êtes intéressés, vous pouvez visiter le site suivant :
http://www.lanutrition.fr/Thierry-Janssen-La-Force-des-emotions-a-1918.html
Jean GRAVELEAU
graveleau.jean2@wanadoo.fr
La personne de confiance
Publié le 04 octobre 2008 à 12:11Paru dans LE PARKINSONIEN INDÉPENDANT N°34 – septembre 2008
Le mercredi 4 juin, l’Espaces des Usagers du CHU de Nantes proposait une conférence-débat sur la personne de confiance avec pour intervenant Dr Annie Rochedreux du service de soins palliatifs et soins de support et Isabelle Marcoux de l’unité de recherche en sciences humaines et sociales appliquées en cancérologie.
Dans le cadre du droit des patients, depuis mars 2002, il est fait obligation au personnel de l’hôpital que le patient puisse désigner une personne de confiance qui va intervenir en quelque sorte comme porte-parole. Dans certains établissements privés, la demande de désigner une personne de confiance se fait lorsque l’on remplit le questionnaire d’entrée, à l’hôpital, cette démarche est menée par les infirmières qui vont prendre le temps de dialoguer avec le patient car désigner une personne de confiance demande réflexion.
La personne de confiance jouera le rôle d’intermédiaire entre le patient et l’équipe médicale et va intervenir comme un nouvel acteur tout au long des soins. Sa présence est d’autant plus importante que le patient souffre d’une maladie grave ou incurable et n’est pas toujours dans la capacité de recevoir les informations du corps médical ou d’assumer toutes les démarches dans l’établissement.
André apporte son témoignage. Il a accompagné un ami qui souffrait d’une maladie orpheline et était atteint d’une perte d’autonomie qui le rendait « légume » alors qu’il conservait une vivacité intellectuelle. Au fil des mois André a intégré l’équipe de soins palliatifs et a contribué à offrir à son ami une fin de vie apaisée et à défendre sa dignité. De cette expérience qui exige une grande implication et une grande disponibilité, on n’en sort pas indemne nous dit-il. Par sa présence, il a joué ce rôle d’intermédiaire, il a aidé le personnel à mieux comprendre le malade pour mieux prendre les décisions et a participé à créer de l’harmonie autour du patient.
Anne, infirmière, intervient pour apporter le point de vue du service du Centre Gauducheau et nous fait part de ses interrogations : quelle place pour ce nouveau partenaire dans la prise en charge ?
- dans un premier temps, l’infirmière propose au patient de désigner une personne de confiance : réponse favorable 9 fois sur 10 et souvent le conjoint. Ensuite, elle informe la personne de confiance à quoi elle s’engage (démarche chronophage : compréhension de l’enjeu, préparation de l’usager, temps de la réflexion)
- difficultés après désignation :- identification de la personne de confiance, faire sa connaissance, ajuster les rôles, équilibre à trouver, « activation » de la personne de confiance : elle est sollicitée par l’équipe, mais souvent difficultés à être impliquée.
- Reste la question de l’information de l’état du malade tout en conservant le secret médical ?
- Les avantages : facilité de prise de décision, surtout en phase terminale, accompagnement de qualité, reconnaissance des proches, meilleur respect du patient.
En conclusion : encore des efforts à faire pour former les soignants et informer les usagers.
Annie Rochedreux nous précise la mission et les droits de la personne de confiance. Toute personne majeure hospitalisée (à l’exclusion des mineurs et des personnes sous tutelle) choisit librement soit un membre de sa famille, soit un proche, soit le médecin traitant comme personne de confiance. La désignation se fait par écrit, sur fiche spéciale, elle est valable pour la durée du traitement.
L’objectif est d’être soutenu moralement tout au long de sa prise en charge. La personne de confiance aide à prendre les décisions concernant sa santé et est garante du droit.
Sa mission : accompagner dans les démarches dans l’établissement et participer aux décisions thérapeutiques. Elle peut assister aux entretiens médicaux (sauf si le patient ne le souhaite pas). Le médecin ne peut refuser sa présence et ne peut opposer le secret médical.
La personne de confiance est consultative dans les situations où le patient est hors d’état d’exprimer sa volonté et l’équipe médicale n’est pas tenue à suivre ses indications.
Le droit à l’information est octroyé à la personne de confiance en cas de diagnostic ou pronostic graves (sauf si le patient s’oppose à cette information).
L’information donnée à la personne de confiance ne dispense pas d’informer la famille et les proches.
L’avis de la personne de confiance prévaut sur celui de la famille.
Lors d’un échange, on est venu à parler des limites du rôle de la personne de confiance qui n’a qu’un rôle consultatif auprès de l’équipe médicale pour traduire les volontés du patient lorsque celui-ci n’est plus à même de s’exprimer. Ce qui est très frustrant. D’où la nécessité, pour ceux qui le désirent, de rédiger sur papier libre les « directives anticipées ». Toute personne majeure peut rédiger des directives anticipées pour le cas où elle serait un jour hors d’état d’exprimer sa volonté. Ces directives anticipées indiquent le souhait de la personne relatif à sa fin de vie concernant les conditions de la limitation ou l’arrêt du traitement, datées et signées elles sont valables trois ans. Elles sont révocables à tout moment.
Pour finir, Isabelle Marcoux nous dresse un tableau comparatif sur la personne de confiance dans le cadre des décisions médicales de fin de vie entre la France, le Canada et les Pays-Bas, sur les mesures existantes pour faire valoir les volontés de soins en fin de vie et les prises de décisions de limitation de traitement. Il en ressort qu’en France il y a moins d’information d’une manière générale et que la loi est plus restrictive.
A la question, la personne de confiance est-elle un bon représentant de la volonté de la personne malade ?
Un premier constat, les proches font de meilleurs représentants que le médecin traitant (disponibilité).
On remarque aussi que, généralement, plus on est malade et plus on est en demande de soins et les directives anticipées, souvent rédigées hors contexte médical, peuvent être remises en cause. Il existe une réaction STP (stress post traumatique) chez les personnes qui ont participé aux décisions. La présence de directives anticipées diminue l’impact du stress, les discussions préalables et une meilleure connaissance des préférences allègent le fardeau de la décision.
On constate qu’un proche sur deux ne veut pas participer au processus de décision.
Quant au droit à l’information, la réponse est que l’on peut tout dire mais pas n’importe comment.
En conclusion, être la personne de confiance est un engagement qui ne se prend pas à la légère. Accompagner une personne malade exige de s’adapter au travail d’une équipe médicale, d’être le porte-parole auprès de la famille et peut demander une grande disponibilité
Proposé par Guy SEGUIN
guymaick@wannadoo.fr
La musicothérapie
Publié le 03 octobre 2008 à 10:39Article par dans LE PARKINSONIEN INDÉPENDANT N°34 – septembre 2008
Laurence Marie, pionnière en musique thérapeutique
Par Emmanuelle Chapados de L’Étoile, le 7 juin 2008
Laurence MARIE allège la souffrance et illumine des vies avec sa harpe. Elle pratique la harpe thérapeutique et la harpe thérapeutique vibroacoustique au Conservatoire de musique Rivière Chocolat et à l’École Camille Vautour de Saint-Antoine. Elle se rend aussi parfois chez des gens qui ne peuvent pas se déplacer et accueille des clients chez elle dans son petit bureau à Shédiac.
« La musique thérapeutique est un art basé sur la science des sons. C’est de la musique acoustique jouée ou chantée sur mesure pour les besoins immédiats du client. Pour moi, c’est d’arriver par les quatre principes : l’utilisation d’éléments intrinsèques de la musique live afin de créer un environnement qui favorise la guérison, les vibrations, la résonance et l’entraînement, à quelque guérison, que ce soit au niveau physique, mental, émotionnel, psychologique, spirituel », explique Mme MARIE.
Avec les enfants, elle trouve que la harpe thérapeutique est ce qu’il y a de mieux, car elle peut utiliser une méthode interactive avec eux alors qu’avec la thérapie vibroacoustique, le patient doit rester immobile sur un matelas spécial. Durant la thérapie vibroacoustique, la harpe de Laurence est amplifiée jusque dans les quatre hauts parleurs situés au niveau du bassin, de la poitrine et des deux côtés de la tête dans le matelas. Cela fait en sorte que la personne entend la musique et la ressent. Laurence témoigne des bienfaits de ces thérapies au niveau de la douleur, du stress, du contrôle des tremblements dus à la maladie de Parkinson et de la tension artérielle, entre autres. Elle dit aussi réussir parfois à sortir des enfants de leur autisme.
« Ce qui marche dans ce genre de thérapie (vibroacoustique), c’est les vibrations de la harpe. La harpe est l’instrument qui vibre le plus et quand tu es sur le matelas, tu ressens les vibrations, physiquement, mais aussi aux autres niveaux. », Ajoute-t-elle.
Laurence MARIE travaille dans le domaine de la santé depuis la jeune vingtaine. Née en France, elle est partie étudier et travailler en Angleterre à l’âge de 18 ans. Ce pays était tellement à court d’infirmières qu’il a payé sa formation. Elle a plus tard immigré au Canada avec son mari et sa fille. Mme MARIE a joué du piano et de la guitare jusqu’à l’âge de 13 ans, quand sa mère a décidé qu’elle ne jouerait plus. Adulte et mère à son tour, elle s’est fait plaisir et a « soigné son cœur blessé » par cette interdiction en obtenant, armée de son violon et son archet, un baccalauréat en musique à l’Université de Moncton. Elle a aussi, par la suite, étudié en homéopathie et en naturopathie à Montréal.
« À un moment donné, j’avais pensé que ce serait intéressant de pouvoir utiliser mes connaissances dans les deux domaines ensemble, d’utiliser la musique comme moyen de guérison » , partage Laurence.
Elle est donc retournée aux études pour obtenir son certificat de praticienne de harpe thérapeutique au « International Harp therapy program » de San Diego en 2001 et son certificat de praticienne de harpe thérapeutique vibroacoustique en 2006. Elle a dû faire des stages pratiques dans des hôpitaux et des centres de soins à San Diego, mais aussi à l’hôpital Georges‑L.-Dumont de Moncton et à l’hôpital de Sainte-Anne-de-Kent.
Elle est de l’avis que le milieu hospitalier du Nouveau-Brunswick, à comparer à celui des provinces comme l’Alberta et le Manitoba, est encore fermé aux thérapies alternatives ou complémentaires du genre. Selon Mme MARIE, les infirmières et certains médecins qui l’ont côtoyée appuient son travail. Ils ont vu des malades aux soins palliatifs mourir paisiblement et sans médicaments, les patients et les travailleurs de sections entières de l’hôpital plus calmes et les parents des malades avoir un moment de répit quand elle jouait sa harpe. Elle n’a tout de même pas réussi à obtenir un poste à l’hôpital Georges‑L.-Dumont comme elle aurait souhaité.
« C’est la bureaucratie qui bloque ça. Ce qui n’aide pas c’est qu’on est habitué que tout soit gratuit pour les soins médicaux. Soit le gouvernement ou les assurances payent. Ça ralentit la clientèle comme quand les massothérapeutes et les chiropraticiens ont commencé, mais une fois que les assurances ont réalisé que ça valait la peine, la clientèle s’est faite… et là je suis la seule ici (musicienne thérapeute). C’est pour ça que je suis une pionnière », précise Mme Marie.
La harpe thérapeutique à elle seule ne permet pas à Laurence de gagner sa vie. Elle est aussi traductrice autodidacte. Elle souhaite continuer à être musicienne thérapeutique au moins jusqu’à ce qu’il y ait une relève qui puisse se charger de ses patients. Elle sourit en disant que maintenant qu’elle fait ce travail, elle n’est plus « stressée » ni déprimée par son travail. Elle ajoute que c’est le plus beau travail qu’elle a fait de sa vie.
Laurence Marie
Infirmière
Harpiste
Musicienne thérapeute au Conservatoire de musique Rivière Chocolat
Diplômée de l’Université de Moncton en musique
Lu par Henri MINAREThenri.minaret@orange.fr
Effets durables des substances addictives : un nouveau mécanisme mis au jour
Publié le 01 octobre 2008 à 08:37Article paru dans LE PARKINSONIEN INDÉPENDANT n°34 – septembre 2008
Jean-Antoine Girault, Directeur de l’Institut du Fer-à-Moulin (U839), centre de recherche de l’Inserm et de l’Université Pierre- et Marie-Curie, et ses collaborateurs viennent de mettre au jour un nouveau mécanisme moléculaire qui explique l’influence, sur le cerveau, de substances telles que la cocaïne.
Les substances qui entraînent une dépendance (substances addictives) telles que la cocaïne, la morphine, les amphétamines exercent leurs effets sur le cerveau en détournant un système normal d’apprentissage auquel participe la dopamine, un transmetteur de « messages » chimiques entre neurones. Cet apprentissage fait notamment intervenir des modifications d’expression de gènes dans des régions cérébrales bien précises. Jean-Antoine Girault, Directeur de recherche à l’Inserm et son équipe viennent de mettre en évidence un nouveau mécanisme par lequel la dopamine est à l’origine de ces modifications au niveau du noyau des neurones. Ces travaux, publiés dans la revue Nature à l’adresse http://dx.doi.org/10.1038/nature06994, permettent de mieux comprendre les mécanismes normaux d’apprentissage et leurs « détournements » par les substances psychoactives. Ils pourraient aussi ouvrir, à terme, de nouvelles perspectives pour le traitement de maladies dans lesquelles la dopamine est impliquée.
Les drogues telles que la cocaïne ou la morphine, qui induisent une dépendance, exercent leurs effets addictifs en détournant le circuit cérébral dit “de la récompense”, dont la dopamine est un acteur majeur. La libération de dopamine dans le cerveau est en effet provoquée directement par la consommation de telles substances. Ce « signal dopamine » est alors interprété à tort par le cerveau comme ayant une valeur positive de récompense. En effet, normalement, la libération de dopamine est observée, lors de stimuli annonçant une récompense naturelle, comme la consommation de nourriture appétissante. La dopamine permet le fonctionnement normal de certaines régions du cerveau (le striatum). Elle facilite l’apprentissage de mouvements et joue un rôle dans la motivation. Ainsi, l’augmentation artificielle des taux de dopamine consécutive à la consommation d’une drogue, entraîne une stimulation chimique directe du circuit de la récompense. Cette hyperstimulation participe au besoin sans cesse accru, et irrépressible chez les sujets dépendants, de reproduire les conduites ayant amené à la prise de drogue.
Différents travaux ont montré que les effets durables des drogues sont dus à des changements d’expression de gènes dans les neurones sur lesquels agit normalement la dopamine. C’est pourquoi “la question à laquelle nous nous sommes intéressés est : Comment précisément la dopamine contrôle l’expression des gènes ?”, explique Jean-Antoine Girault.
Dans les travaux publiés aujourd’hui dans Nature, les chercheurs apportent probablement une partie de la réponse. Ils mettent en effet en évidence une nouvelle voie de signalisation impliquant plusieurs enzymes spécifiques, des protéines phosphatases, activée par la dopamine et aboutissant à une modification de la chromatine, ce matériel génétique présent dans le noyau des neurones. Ils montrent en particulier que, dans une région du cerveau appelée striatum, une protéine, la DARPP-32 s’accumule dans le noyau des neurones lorsqu’une souris reçoit une injection de cocaïne, d’amphétamine, ou de morphine. Les chercheurs observent ensuite que, lorsque la séquence d’acides aminés qui compose la protéine DARPP-32 est mutée sur un seul acide aminé, les souris sont moins sensibles aux drogues. De plus, les auteurs montrent que cette protéine n’est pas uniquement mise en jeu par des drogues, mais intervient aussi dans l’apprentissage d’un geste très simple, qui consiste, pour la souris, à mettre son museau dans un petit trou pour obtenir un peu de nourriture. Cet apprentissage suffit en effet à entraîner l’accumulation de DARPP-32 dans le noyau des neurones du striatum. Et, de la même manière, la mutation ponctuelle de la protéine DARPP-32 diminue la motivation pour obtenir de la nourriture après un tel apprentissage.
Ce travail élucide un nouveau mécanisme par lequel la dopamine contrôle l’expression de gènes dans les neurones. Il met en évidence l’importance de ce mécanisme dans les effets durables des drogues et permet également de déterminer la cascade des événements au niveau du neurone, qui président à l’apprentissage normal contrôlé par le circuit de la récompense. Ces résultats suggèrent des approches de recherche nouvelles dans le domaine du traitement de la dépendance aux drogues, et de certaines maladies mentales, pour lesquelles la dopamine est soupçonnée de jouer un rôle. Cette connaissance plus fine des mécanismes d’action de la dopamine au niveau moléculaire vise aussi à améliorer le traitement de la maladie de Parkinson, dans laquelle le rôle de la dopamine est central.
Source : NewsPress
article de La Revue de presse de Première ligne :
http:/premièreligne.ch/blog/2008/05/26
En savoir plus sur le Recherche de la Transmission Neuronale
Publié le 29 septembre 2008 à 12:58Article paru dans LE PARKINSONIEN INDÉPENDANT N°34 – septembre 2008
Dans le cerveau humain, 100 milliards de neurones communiquent via 100.000 milliards de connexions, « les synapses ». C’est à cette jonction que se joue la communication neuronale. Or depuis dix ans, celle-ci pose problème aux spécialistes du cerveau : la vitesse de circulation de l’information apparaît bien supérieure aux capacités de transmission des synapses… Un mystère enfin résolu.
Notre cerveau va très vite, par exemple il faut seulement 120 millisecondes pour répondre à une stimulation visuelle. Le parcours de l’influx nerveux n’est pas de tout repos, notamment au niveau des connexions entre neurones et synapses.
Lorsqu’un neurone émetteur est stimulé par un signal électrique (influx nerveux) il libère des substances chimiques (neurotransmetteurs) dans la synapse. Les neurotransmetteurs se fixent au niveau des récepteurs du neurone qui reçoit le message. Cela provoque un changement de l’activité électrique de ce neurone d’où un nouveau signal qui diffuse à travers l’enchevêtrement des cellules cérébrales.
Or on sait depuis une dizaine d’années que les récepteurs changent de configuration en présence d’un neurotransmetteur et ne peuvent répondre à une deuxième stimulation pendant une centaine de milliseconde. Les synapses transmettent bien l’information mais beaucoup trop vite pour que les récepteurs retrouvent leur activité,
C’est en 2002 que Daniel CHOQUET, directeur du laboratoire Physiologie cellulaire de la synapse de Bordeaux et ses collaborateurs font une importante découverte : au niveau des synapses les récepteurs, sur lesquels se fixent les neurotransmetteurs, ne sont pas figés comme on l’a toujours cru, mais ils bougent sans cesse.
L’équipe de Daniel CHOQUET décide d’observer ce qui se passe dans la fente synaptique, espace de 10 à 40 mm.¹ entre deux neurones. Les neurobiologistes s’associent alors à l’équipe de Brahim LOUNIS du Centre de Physique moléculaire optique et hertzienne également de Bordeaux, afin que celle-ci leur fournisse des techniques de détection et de suivi de molécules individuelles dans les neurones vivants,
Six ans plus tard les résultats sont détonants : les chercheurs ont découvert que la mobilité des récepteurs joue, en réalité, un rôle important dans le transfert de l’information neuronale et qu’elle serait la clé de l’étonnante rapidité avec laquelle le cerveau réagit à la moindre stimulation
Des essais ont été étudiés sur les récepteurs à glutamate du rat et ont permis de démontrer que ces récepteurs ne sont pas statiques et que ces mouvements rapides jouaient peut-être un rôle dans la transmission synaptique.
II fallait s’en assurer. Une série de manipulations fut entreprise : excitations au laser, utilisation d’optiques de très haute qualité et de détecteurs ultrasensibles, puis analyse d’images, L’analyse n’est pas simple du tout dit D. COCHET mais elle a porté ses fruits : les chercheurs découvrent que les récepteurs peuvent se déplacer de plusieurs micromètres à l’intérieur et à l’extérieur de la membrane synaptique. En quelques millisecondes, le récepteur est capable de se mouvoir d’un bout à l’autre de la synapse résume le scientifique.
La découverte de ce rôle des récepteurs est majeure pour la compréhension de certains troubles neurologiques ou psychiatriques comme la maladie d’Alzheimer, de Parkinson, les Tocs, les Dépressions.,. qui sont dus à une mauvaise communication entre neurones
La prochaine étape : Vérifier ces hypothèses dans des conditions plus physiologiques, à plus grande échelle, sur des tranches de cerveaux animaux intacts ou sur des modèles développant ces pathologies, confie Daniel CHOQUET.
Ces travaux ouvrent la voie à de nouvelles pistes de recherche à exploiter. Nous devons également mieux identifier les pathologies concernées.
Les applications médicales ne sont pas pour tout de suite. Il s’agit de maladies humaines, or nous travaillons toujours sur des modèles animaux, rappelle Daniel CHOQUET
¹ nm : mètre divisé par un milliard
Source ; Science et Vie N° 1091 — août 2008 Lu et résumé par
Jacqueline GÉFARD-LE BIDEAU
Propulsé par WordPress et le thème GimpStyle créé par Horacio Bella. Traduction (niss.fr).
Flux RSS des Articles et des commentaires.
Valide XHTML et CSS.